
Физика 4 семестр / Opisania_labotatornykh_rabot_po_fizike / Описание работы №54
.pdf
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ
________________________
МОСКОВСКИЙ ЭНЕРГЕТИЧЕСКИЙ ИНСТИТУТ (ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ)
КАФЕДРА ОБЩЕЙ ФИЗИКИ И ЯДЕРНОГО СИНТЕЗА
А.Н. Седов
Лабораторная работа №54
ИЗУЧЕНИЕ СПЕКТРА ИЗЛУЧЕНИЯ
АТОМА ВОДОРОДА
Методическое пособие
Москва |
2011 |
ЛАБОРАТОРНАЯ РАБОТА № 54
ИЗУЧЕНИЕ СПЕКТРА ИЗЛУЧЕНИЯ АТОМА ВОДОРОДА
Цель работы – измерение длин волн спектральных линий атомарного водорода в видимой части спектра, экспериментальное определение значения постоянной Ридберга.
1. Теоретические основы работы
Характеристика излучения, выражающая его частотный (спектральный) состав называется спектром излучения. Спектры излучения и поглощения атомов являются линейчатыми. Они состоят из отдельных спектральных линий – узких квазимонохроматических пиков интенсивности излучения.
Спектры излучения молекул представляют собой полосы более широкого частотного состава. Линии в спектре излучения атомов располагаются не беспорядочно, а образуют строго определенные группы, которые принято называть сериями. Положение спектральных линий в спектре обычно определяется длиной волны либо частотой.
Закономерности атомных и молекулярных спектров были хорошо изучены экспериментально еще до создания квантовой теории строения атомов. Однако теоретическое объяснение этих закономерностей возможно только на основе квантовых представлений, как о свете, так и о строении атомов и молекул.
Согласно современным представлениям, электроны в атомах могут иметь строго определенные значения полной энергии. Для атома водорода этот дискретный ряд значений энергии определяется формулой
E |
|
= − |
m e4 |
1 |
, (n = 1, 2, 3, ….), |
(1) |
|
n |
2 2 |
|
n 2 |
||||
|
|
|
|
|
|||
где m = масса электрона; е – заряд электрона; - постоянная Планка. В квантовой механике используется не международная система (СИ), а система СГС (точнее – Гауссова система единиц), основными единицами которой являются сантиметр, грамм и секунда. Для квантовой механики международная система не только не нужна, но и крайне неудобна. Целое число n называется главным квантовым числом. Главное квантовое число определяет значение полной энергии электрона в атоме. Состояние электрона с n = 1 называется основным состоянием и характеризуется наименьшим значением энергии. Значения полной энергии En называют энергетическим уровнями .
Таким образом, энергия электрона в атоме дискретна (квантована). Знак минус указывает на то, что полная энергия электрона в атоме меньше, чем в свободном состоянии. За нуль отсчета принимается энергия при n = ∞, когда электрон не связан с ядром, а его кинетическая энергия равна нулю.
Вспектроскопии уровни энергии принято изображать горизонтальными линиями,
апереходы между ними – стрелками (рис. 1). Расстояния между горизонтальными линиями пропорциональны соответствующим разностям энергий.
2
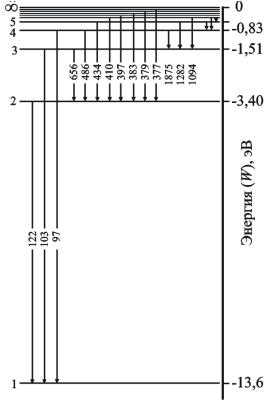
Серия Бальмера
Длины волн указаны в нм (1 нм = 10-9 м)
Рис. 1. Энергетические уровни атома водорода
Переход электрона с одного энергетического уровня на другой может происходить только при изменении его энергии на величину равную разности энергий соответствующих уровней. Переход электрона на более высокие уровни энергии (уровни с большим значение энергии) может происходить за счет соударений, связанных с тепловым движением атомов, соударений атомов с достаточно быстрыми электронами в газовом разряде, или при поглощении атомом фотона. При этом атом оказывается в возбужденном состоянии.
Находиться в возбужденном состоянии длительное время атом не может, поэтому электрон спонтанно (самопроизвольно) переходит на более низкий энергетический уровень. При этом испускается фотон, энергия которого равна разности энергий электрона (правило частот):
ω = En |
2 |
− En , |
(2) |
|
1 |
|
где n1 и n2 – номера соответствующих энергетических уровней.
Подставляя выражения для полных энергий En2 и En1 из (1), получим формулу для частот спектральных линий атома водорода:
ω = |
m e |
4 |
|
1 |
− |
1 |
|
|
||
|
|
. |
(3) |
|||||||
|
|
|
|
|
||||||
2 |
3 |
|
2 |
|
n |
2 |
|
|
||
|
|
n1 |
|
2 |
|
|
||||
С учетом того, что ω = 2πc / λ , имеем:
3

1 |
= |
me |
4 |
|
|
1 |
− |
1 |
|
|
|
|
|
|
|
|
|
. |
(4) |
||
|
|
3 |
|
2 |
2 |
|||||
λ |
|
4π |
|
|
|
|
|
|||
|
|
c n1 |
|
n2 |
|
|
||||
Эта формула часто используется в прикладной спектроскопии. Постоянный множитель, стоящий перед скобкой в последней формуле, обычно обозначают буквой R и называют постоянной Ридберга для атома водорода:
|
|
R |
= |
|
m e 4 |
|
. |
|
(5) |
|
|
|
4 π 3 c |
|
|||||||
Для вычисления R воспользуемся значениями универсальных констант, входящих в |
||||||||||
формулу: |
|
|
|
|
|
|
|
|
|
|
с = 2,99793·1010 см/с, |
|
|
|
|
|
|
=1,0544·10-27 эрг·с, |
|
||
e = 4,8030·10-10 ед. заряда СГСЭ, |
m = 9,10938 10-28 г; |
|
||||||||
формула (5) даст тогда следующее теоретическое значение: |
|
|||||||||
|
R = 109737,34 см–1 . |
|
||||||||
С учетом (5) формула (4) принимает вид (формула Бальмера): |
|
|||||||||
1 |
= |
|
1 |
− |
1 |
|
(6) |
|||
|
|
R |
|
|
. |
|||||
|
λ |
2 |
2 |
|||||||
|
|
n1 |
n2 |
|
|
|||||
В спектроскопии величина k = 1/λ называется волновым числом и обычно выражается в единицах см–1 . Волновое число показывает, сколько раз длина волны укладывается в одном сантиметре.
Совокупность спектральных линий, соответствующих переходам на уровень n1 = 2, образует с ерию Бальмера. Четыре первые спектральные линии этой серии расположены в видимой области спектра, они обозначаются Hα, Hβ, Hγ, Hδ и соответствую переходам электронов с уровней с квантовыми числами 3, 4, 5 и 6.
Для серии Бальмера формула (6) c использованием волнового числа принимает вид
k = |
|
1 |
|
− |
1 |
|
, |
n = 3, 4, 5, ….., |
|
|||||
R |
|
|
|
|
|
|
|
|
|
|||||
2 |
2 |
|
|
n |
2 |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
или |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
k = |
|
|
R |
|
− |
R |
. |
(7) |
||||
|
|
2 2 |
|
n 2 |
||||||||||
|
|
|
|
|
|
|
|
|
|
|||||
Величина T(n) = R называется спектральным термом или просто термом. n2
Из (7) следует, что волновое число спектральной линии равно разности соответствующих термов.
Из формулы (6) видно, что по мере увеличения n разность между волновыми числами соседних линий уменьшается, и при n = ∞ получаем постоянное значение k = R/4. Таким образом, линии должны постепенно сближаться, стремясь к предельному положению k = R/4. Предельное волновое число называется границей серии .
Из формулы (7) также следует выражение, содержащее связь между волновыми числами спектральных линий:
km − kn = T (n) − T (m) ,
разность волновых чисел двух спектральных линий равна разности соответствующих термов. Разность волновых чисел двух спектральных линий является, в свою очередь, волновым числом другой спектральной линии. Это утверждение является современной
4
формулировкой комбинационного принципа , который был установлен эмпирическим путем.
Наблюдать видимые линии спектра излучения атома можно с помощью спектральных приборов (спектрометров, монохроматоров). Измерив длины волн визуально наблюдаемых спектральных линий серии Бальмера – красной, голубой, фиолетово-синей и фиолетовой, можно определить экспериментальное значение постоянной Ридберга R.
2. Описание экспериментальной установки
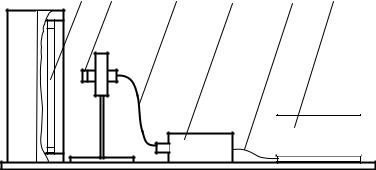
Схематическое изображение экспериментальной установки для исследования спектра излучения атома водорода приведено на рис. 2.
1 |
2 |
3 |
4 |
5 |
6 |
|
Рис. 2 |
Экспериментальная установка |
|
||
Источником излучения является водородная трубка 1, установленная в одном корпусе с источником питания. В водородной трубке под действием высокого напряжения возникает тлеющий разряд. При соударении с электронами, которые ускоряются в электрическом поле и приобретают достаточно большую энергию, атомы водорода возбуждаются. Возбужденные атомы, переходя в состояние с меньшей энергией, излучают несколько спектральных линий, четыре из которых находятся в видимой области спектра, а остальные в ультрафиолетовой области.
Излучение водородной трубки объективом 2 фокусируется на торце световода 3. Через световод излучение попадает в спектрометр 4, где с помощью дифракционной решетки разлагается в спектр. В качестве светочувствительного элемента используется ПЗС линейка (ПЗС – прибор с зарядовой связью), электрический сигнал с которой через кабель 5 подается на USB вход компьютера 6. Специальная программа производит сканирование элементов ПЗС линейки и на дисплее компьютера рисует спектр исследуемого излучения.
3. Порядок выполнения работы
|
|
|
|
|
Таблица 1 |
|
|
Спецификация измерительных приборов |
|
|
|||
|
|
|
|
|
|
|
Название прибора |
|
Пределы |
Цена |
|
Инструментальная |
|
и его тип |
|
измерения |
деления |
|
погрешность |
|
Спектрометр Spectra-1 |
|
400 - 900 нм |
|
|
0,05 нм |
|
5
1. Произведите калибровку спектрометра по известным длинам волн трех спектральных линий гелия, для чего:
–перед объективом спектрометра установите блок с гелиевой трубкой, включите источник питания гелиевой трубки;
–включите компьютер и запустите программу «Spectrometer»;
–произведите калибровку согласно руководству по эксплуатации спектрометра, используя значения длин волн спектральных линий гелия, приведенные в табл. 2;
–выключите источник питания гелиевой трубки.
Таблица 2
Длины волн спектральных линий гелия
Цвет линии |
Длина волны λ, нм |
|
|
Красная |
667,8 |
|
|
Желтая |
587,6 |
|
|
Зеленая |
501,6 |
|
|
2. Определите длины волн спектральных линий излучения водорода, для чего:
–перед объективом спектрометра установите блок с водородной трубкой, включите источник питания водородной трубки;
–в главном окне программы «Spectrometer» нажмите кнопку «Play» и установите флажок «Show peaks». Изменяя расстояние между водородной лампой и объективом спектрометра, добейтесь, чтобы пики спектральных линий, имеющих наибольшую интенсивность, полностью помещались в пределах окна графиков. Запишите длины волн спектральных линий в табл. 3.
Таблица 3
Измерение длин волн спектральных линий атома водорода
Цвета спектральных линий |
Длина волны λ, нм |
Красная |
|
Голубая |
|
Фиолетово-синяя |
|
Фиолетовая |
|
4.Обработка результатов измерений
1.Рассчитайте значения волновых чисел спектральных линий серии Бальмера соответствующие значения величины 1/n2. Результаты запишите в табл. 4.
6

Табл. 4
Зависимость волнового числа от 1/n2
n |
|
1 |
|
k = |
1 |
, см-1 |
|
|
|
|
|||
n2 |
λ |
|||||
3 |
|
|
|
|
|
|
4 |
|
|
|
|
|
|
5 |
|
|
|
|
|
|
6 |
|
|
|
|
|
|
2.Постройте график зависимости волнового числа k от 1/n2.
3.Эта зависимость, как следует из формулы (7), является линейной. Произведите аналитическую или графическую аппроксимацию экспериментальных точек уравнением прямой линии у = A +Bx, где
у = k ; A = |
R |
; |
B = − R ; x = |
1 |
. |
|
|
||||
4 |
|
|
n 2 |
||
6. Найдите среднее значение постоянной Ридберга:
Rср=2A+B/2.
7. Рассчитайте абсолютную погрешность среднего значения постоянной Ридберга
R = |
(2 A) |
2 |
|
B 2 |
|
+ |
. |
||
|
|
|
|
2 |
Запишите окончательный результат в стандартном виде.
5.Контрольные вопросы
1.Что называется спектром излучения, спектральной линией?
2.Опишите спектр излучения водорода, который Вы наблюдали в лабораторной работе. Что Вы измеряли?
3.Расскажите о модели атома водорода, предложенной Резерфордом.
4.Сформулируйте постулаты Бора, которые он ввел при создании теории атома водорода.
5.Какими квантовыми числами описывается состояние электронов в атоме? Квантование каких физических величин они определяют?
6.Изобразите энергетическую диаграмму атома водорода. Какие переходы электронов между энергетическими состояниями приводят к излучению в видимой части спектра?
7.В чем заключается физический смысл Боровских радиусов орбит электронов?
8.Какой смысл имеет главное квантовое число? Что оно определяет?
7
