
- •ГЛАВА 5. АРИТМИИИ БЛОКАДЫ СЕРДЦА........................................…………...
- •ГЛАВА 6. МИОКАРДИТЫ. МИОКАРДИОПАТИИ……………………...………..
- •ГЛАВА 7.ПЕРИКАРДИТЫ. ………………….………………………..…................
- •ГЛАВА 3. АПЛАСТИЧЕСКАЯ АНЕМИЯ..................................................................
- •ГЛАВА 4. ОСТРЫЕ ЛЕЙКОЗЫ………………………………………………………
- •ГЛАВА 5.ХРОНИЧЕСКИЕ МИЕЛО- И ЛИМФОЛЕЙКОЗЫ……………………..
- •Патогенетические механизмы.
- •Классификация гипертонических кризов.
- •Неосложнённый гипертонический криз, несмотря на выраженную клиническую симптоматику, не сопровождается острым клинически значимым нарушением функции органов-мишеней.
- •Примечание.ВNP или NT – pro ВNP -N-концевой предсердный натрийуретический пептид и его предшественник (Национальные клинические рекомендации ВНОК, 2008).
- •Цели лечения острой сердечной недостаточности.
- •Цель неотложного лечения – быстрая стабилизация гемодинамики и уменьшение симптомов (одышки и/или слабости).
- •Диета. Необходимо поддерживать оптимальный баланс калорий и аминокислот, калия и магния в сыворотке крови.
- •Показания к ИВЛ с интубацией трахеи:
- •Медикаментозное лечение.
- •Морфин – показан при раннем лечении тяжелой ОСН, особенно при наличии боли, возбуждении и выраженной одышки. Вводят в/в болюсом 3 мг сразу после катетеризации вены, при необходимости повторно.
- •Примечание.Национальные клинические рекомендации ВНОК, 2008.
- •Ингибиторы ангиотензинпревращающего фермента(ИАПФ)– на начальных этапах лечения ОСН препараты этой группы недостаточно изучены.
- •Для борьбы с устойчивостью к диуретикам:
- •β-адреноблокаторы (БАБ) – лечениеβ-блокаторамипосле ликвидации симптомов ОСН (дозы титруют постепенно) вызывает улучшение клинической картины и прогноза у больных ИМ и ХСН. Дозы титруют постепенно.
- •Показания: сохраняющаяся АГ, ишемия микарда, тахикардия у больных без артериальной гипотонии и признаков периферической гипоперфузии и стандартных противопоказаний (метопролол, эсмолол, бисопролол, карведилол).
- •ГЛАВА 5. АРИТМИИИ БЛОКАДЫ СЕРДЦА.
- •Электрокардиостимуляция.
- •Кардиомиопатии.
- •ГЛАВА 7. ПЕРИКАРДИТЫ.
- •ГЛАВА 8. ВРОЖДЕННЫЕ ПОРОКИ СЕРДЦА У ВЗРОСЛЫХ (ВПС).
- •ГЛАВА 3. АПЛАСТИЧЕСКАЯ АНЕМИЯ.
- •ГЛАВА 4. ОСТРЫЕ ЛЕЙКОЗЫ.
- •ГЛАВА 5. ХРОНИЧЕСКИЕ МИЕЛО - И ЛИМФОЛЕЙКОЗЫ.
- •Возможные этиологические факторы:
- •1. Малые дозы радиации.
- •2. Слабые электромагнитные излучения.
- •3. Гербициды, инсектициды и т.д.
- •4. Химические агенты – бензол.
- •Патогенетические аспекты ХМЛ.
- •Биологический эффект химерного генаBCR-ABL в гемопоэтических предшественниках:
- •Таблица 7-1
- •Стадии ММ
- •Клиническая картина.
- •Дифференциальный диагноз.
- •Лечение осложнений ММ.
- •Лечение и профилактика осложнений.
- •Лечение ХГН.
- •Терминальная почечная недостаточность.
- •Основные причины ТПН:
- •Лечение.
- •Таблица 4-1
- •Классификация амилоидоза
- •Клиническая картина и диагностика.
- •Лабораторные исследования.
- •Инструментальные исследования.
- •Таким образом, в основе развития ХЛС лежит постепенное формирование легочной артериальной гипертензии, которая обусловлена несколькими патогенетическими механизмами.
- •Клиника и диагностика ХЛС.
- •2) дыхательной недостаточности:
- •Плевральная пункция и исследование плевральной жидкости при диагностике плевритов и плевральных выпотов.
Компьютерная томография (КТ) обладает рядом преимуществ по сравнению с рентгенографией: обеспечивает чёткую картину состояния плевральной полости, и в то же время - паренхимы лёгких и средостения, позволяет выявить отдельные плевральные бляшки, изменения плевры и наличие выпота на ранних стадиях (первые дни заболевания). КТ с контрастированием позволяет обнаружить множественные локализованные выпоты при осумкованных плевритах, отличить их от изменений в паренхиме, различать доброкачественные и злокачественные изменения плевры. При КТ можно с высокой точностью определить протяжённость поражения и проконтролировать пункцию или взятие биопсийного материала.
УЗИ плевральной полости. УЗИ может помочь в более точном определении локализации жидкости в плевральной полости в тех случаях, когда возникают затруднения в полной эвакуации выпота во время торакоцентеза. При УЗИ можно обнаружить выпот объёмом до 5 мл, при объёме более 100 мл информативность метода приближается к 100%. УЗИ позволяет отличить плевральный выпот от фиброза плевры или её утолщения, точно определить положение купола диафрагмы, скрытого выпотом. Также УЗИ применяют для определения оптимальной точки вкола при плевральной пункции, установке дренажа.
Плевральная пункция и исследование плевральной жидкости при диагностике плевритов и плевральных выпотов.
Диагностический торакоцентез должен быть выполнен практически у каждого больного, если при рентгенологическом исследовании, проведенном при положении пациента лежа на боку, толщина свободной жидкости превышает 10 мм. У пациентов с сердечной недостаточностью, при гипертермии и/или боли в грудной клетке, и/или если выпот с одной стороны значительно больше, чем с другой – торакоцентез должен быть выполнен без промедления. Удаление транссудата из плевральной полости посредством торакоцентеза в данном случае снижает объем циркулирующей жидкости (крови) и давление в легочных капиллярах, поэтому в современные лечебные рекомендации эта манипуляция включена в качестве обязательной процедуры при ведении больных с застойной сердечной недостаточностью.
Даже при наличии коагулопатии, тромбоцитопении, механической вентиляции с положительным давлением торакоцентез может быть без особого риска выполнен тонкой иглой. Важны правильное положение больного, идентификация уровня и локализации жидкости, адекватная местная анестезия, введение иглы по верхнему краю ребра.
Не рекомендуется удалять за один раз более 1 л жидкости (даже при отсутствии эмпиемы и фибринозных наложений) из-за риска развития отека легкого на фоне его расправления.
Плевральная жидкость в норме имеет следующие параметры: общий объем 0,1–0,2 мл/кг; количество клеток в 1 мл - 1000–5000, мезотелиальных клеток - 3–70%, моноцитов - 30–75%, лимфоцитов - 2–
601
30%, гранулоцитов - 10%; белок - 10–20 г/л, альбумин - 50–70%; уровень глюкозы соответствует таковому в плазме, ЛДГ менее 50% от уровня в плазме; pH не ниже уровня в плазме. Исследование плеврального выпота имеет большое значение для дифференциально диагностики. По показателям клинико-лабораторного, биохимического, цитологического исследований возможно получение ответа о генезе процесса (табл. 5-2).
Таблица 5-2
Вероятные причины изменения плевральной жидкости
(по А.Г. Чучалину, 2007)
Показатели |
Значения |
Наиболее вероятные |
|
|
|
|
причины |
Соотношение |
> 50% |
Гемоторакс |
|
гематокрита в выпоте |
> 1%, но < 50% |
Злокачественная опухоль, |
|
к крови |
|
|
ТЭЛА, травма |
Эритроциты |
> 100 000/мм3 |
Злокачественная опухоль, |
|
|
|
|
травма, ТЭЛА |
Лейкоциты |
|
> 10 000/мм3 |
Эмпиема, |
|
|
|
парапневмонический |
|
|
|
экссудат, панкреатит, ТЭЛА, |
|
|
|
коллагеноз, редко - |
|
|
|
злокачественная опухоль, |
|
|
|
туберкулез |
|
|
< 1000/мм3 |
Транссудат |
Нейтрофилы |
> 50% |
Острый плеврит |
|
Лимфоциты |
> 90% |
Туберкулез, |
|
|
|
|
злокачественная опухоль |
Эозинофилы |
>10% |
Асбестоз, пневмоторакс, |
|
|
|
|
разрешающаяся инфекция |
Мезотелиальные |
отсутствуют |
Туберкулез |
|
клетки |
|
имеют признаки |
Мезотелиома |
|
|
злокачественност |
|
|
|
и |
|
Соотношение концентрации в выпоте к концентрации в плазме |
|||
Белка |
|
> 0,5 |
Критерий экссудата |
Лактатдегидрогеназы |
> 0,6 |
Критерий экссудата |
|
(ЛДГ) |
|
|
|
ЛДГ в выпоте |
> 200 МЕ |
Критерий экссудата |
|
ЛДГ в |
выпоте к |
> 2/3 |
Критерий экссудата |
верхней |
границе |
|
|
нормы в крови |
|
|
|
Глюкоза в выпоте |
< 3,33 ммоль/л |
Парапневмонический |
|
|
|
|
экссудат, туберкулез, |
|
|
|
ревматоидный артрит, |
|
|
|
гемоторакс, парагонимиаз, |
602
|
|
cиндром Чарг–Стросса |
|
> 4,44 ммоль/л |
Системная красная волчанка |
Белок в выпоте |
> 50 г/л |
Туберкулез |
|
< 5 г/л |
Уриноторакс, |
|
|
перитонеальный диализ |
рН в выпоте |
< 7,20 |
Осложненный |
|
|
парапневмонический выпот |
|
|
(эмпиема), повреждение |
|
|
пищевода, туберкулез, |
|
|
злокачественное |
|
|
новообразование, |
|
|
ревматоидный артрит, |
|
|
гемоторакс, системный |
|
|
ацидоз, парагонимиаз, |
|
|
системная красная волчанка, |
|
|
уриноторакс |
Амилаза в выпоте по |
> 1 |
Панкреатит |
отношению к |
более верхней |
Повреждение пищевода, |
концентрации в |
границы нормы |
болезни поджелудочной |
плазме |
концентрации в |
железы, злокачественные |
|
плазме |
опухоли |
|
|
|
У некоторых больных, учитывая предполагаемую причину, целесообразно определять уровень антиядерных антител, ревматоидного фактора, аденозиндеаминазы, липиды и т.д.
Необходимо оценить внешний вид жидкости. Макроскопический вид и запах. Зловонный запах свидетельствует о бактериальной инфекции, возможно анаэробного характера, запах мочи - об уринотораксе. Супернатант плевральной жидкости исследуют на липиды, если он мутный, молочного цвета, осадок - на кристаллы холестерина.
Обязательно отправить жидкость на цитологию.
Провести бактериологические исследования. Культуральные исследования на аэробные и анаэробные бактерии, микобактерии, грибки. Окраска по Грамму. Бактериоскопия. Определение бактериальных антигенов путем иммуноэлектрофореза, латексагглютинации, или бактериальной ДНК с помощью полимеразной цепной реакции (ПЦР).
Другие диагностические тесты плевральной жидкости. Тесты для коллагенозов: антиядерные антитела для СКВ; ревматоидный фактор для ревматоидного артрита. Аденозиндеаминаза повышена при туберкулезе, сохраняет свое диагностическое значение при инфекции вирусом иммунодефицита человека. Может быть повышена при эмпиеме, лимфомах, лейкозах. Интерферон γ повышен при туберкулезе.
Молекулярные методы для диагностики туберкулеза: ПЦР; исследования нуклеиновых кислот для идентификации организма в
603
культуре; исследования полиморфизма фрагментов ограниченной длины; сканирование известных генов лекарственной резистентности.
Транссудативный плевральный выпот часто сопутствует многим заболеваниям. В большинстве случаев первично поражены не плевра или легкие, а другие органы, в первую очередь сердце, печень и почки.
Застойная сердечная недостаточность.
Является наиболее частой причиной транссудативного плеврального выпота.
Патофизиология. Выход легочной интерстициальной жидкости в плевральную полость через проницаемый мезотелий подтверждается высокой частотой выпота у больных с рентгенологически установленным отеком легкого, а также большей корреляцией наличия выпота с легочным венозным давлением, чем с системным венозным или легочным артериальным давлением.
Клиническая симптоматика: симптомы застойной сердечной недостаточности: диспноэ при нагрузке, ортопноэ, никтурия, периферические отеки, растяжение вен шеи, влажные хрипы в нижних отделах легких и ритм галопа; наличие кардиомегалии при рентгенографии грудной клетки. Симптомы дыхательной недостаточности будут превалировать при большом количестве выпота и выраженном отеке легких. Плевральный выпот имеет тенденцию быть двухсторонним.
Диагностика и лечение. Обычно подозрение возникает уже по клинической картине. Торакоцентез показан, если: выпот односторонний или на одной стороне несравнимо больше, чем на другой; у пациента фебрильная температура; боль в грудной клетке; отсутствует кардиомегалия. При отсутствии данных критериев у больного необходимо лечить застойную сердечную недостаточность, а диагностический торакоцентез показан только в случае отсутствия разрешения выпота после назначенной терапии.
При приеме диуретиков биохимические свойства выпота могут измениться так, что он может походить на экссудат по уровню ЛДГ и белка.
Лечение проводится с помощью препаратов, снижающих нагрузку на сердце, диуретиков и, по показаниям, инотропов. Обычно при эффективной терапии сердечной недостаточности выпот исчезает. При выраженном диспноэ необходим лечебный торакоцентез.
Изредка, несмотря на лечение, у больного постоянно накапливается жидкость в большом объеме. При наличии диспноэ и эффективности его купирования торакоцентезом необходимо совместно с торакальным хирургом решать вопрос о выполнении плевродеза доксициклином или тальком.
Заболевания перикарда.
Механизм возникновения плеврального выпота при заболеваниях перикарда до конца не ясен. При констриктивном перикардите объяснением может быть повышение легочного и системного
604
капиллярного давления. При воспалительном заболевании перикарда выпот в основном левосторонний, а возможной его причиной является переход воспаления с перикарда на прилежащую плевру. Лечение должно быть направлено в первую очередь на основное заболевание.
Гидроторакс при циррозе печени.
У 5–6% больных с циррозом печени развивается плевральный выпот. Такая вероятность больше при асците, хотя у некоторых больных с выпотом асцита может не быть.
Патофизиология. Основной механизм - движение асцитической жидкости из брюшной полости через поры в диафрагме в плевральную полость. Поры в диафрагме были продемонстрированы в ряде исследований. Второй фактор — снижение онкотического давления плазмы.
Клиническая симптоматика. Обычно доминируют симптомы цирроза и асцита. При большом количестве жидкости в плевральной полости возникает диспноэ. Обычно выпот справа (у 2/3 больных), но у 1/6
— слева и у 1/6 — двухсторонний.
Диагностика и лечение. Ведущими методами являются рентгенологические исследования плевральной полости, диагностика основного заболевания. При наличии сомнений, проводят сканирование грудной клетки после введения в брюшную полость Тс99 меченного коллоида. Для получения доказательств, что обе жидкости являются транссудатом, необходимы лапароцентез и торакоцентез.
Первичное лечение цирроза с асцитом и плевральным выпотом должно быть направлено на лечение асцита. Показаны низкосолевая диета и диуретики. Дренирования плевральной полости следует избегать в связи с большими потерями жидкости и белка из-за перетока асцитической жидкости в плевральную полость и вытекания ее по дренажу наружу. Если имплантация шунта и трансплантация печени неосуществимы, то лучшей альтернативой может быть торакоскопическая операция под видеоконтролем с закрытием диафрагмальных дефектов и плевродезом. У ряда больных возможно еще проведение перитонеальновенозного шунтирования, хотя его результаты часто остаются неудовлетворительными.
605
Нефротический синдром.
Механизм возникновения плеврального выпота: снижение онкотического давления плазмы и повышение гидростатического давления (на фоне солевой задержки и гиперволемии). Обычно выпот двухсторонний и часто инфрапульмональный. Диагностический торакоцентез должен быть выполнен у всех больных с нефротическим синдромом и плевральным выпотом, чтобы доказать, что жидкость является транссудатом. В связи с высоким риском венозных тромбозов у данной категории больных необходимо исключить ТЭЛА, и если плевральный выпот имеет признаки экссудата, показано проведение сцинтиграфии легких и спиральной КТ.
Лечение направлено на повышение белка в плазме путем снижения его потерь с мочой. Если это неэффективно, то для больных с выраженной симптоматикой из-за плеврального выпота следует рассмотреть вопрос о проведении плевродеза.
Перитонеальный диализ.
Иногда осложняется гидротораксом. Это результат движения диализата из брюшной полости в плевральную. В 90% случаев выпот правосторонний. Уровень глюкозы в выпоте промежуточный между диализатом и плазмой, белок менее 10 г/л, низкая ЛДГ. Хотя сообщение между брюшной и плевральной полостями у некоторых больных закрывается спонтанно, при необходимости продолжения перитонеального диализа показано хирургическое лечение. Методом выбора является торакоскопия с закрытием дефектов в диафрагме и плевродезом. Альтернативой могут быть просто плевродез или торакотомия с ушиванием диафрагмальных дефектов.
Обструкция мочевыводящих путей (уриноторакс).
Обструкция мочевыводящих путей, приводящая к забрюшинному накоплению мочи (уринома), может привести к плевральному выпоту. Механизм неясен, но вероятно, что жидкость поступает вдоль градиента давления в плевральную полость. Выпот представляет собой мочу (уриноторакс) и имеет запах мочи. Диагноз ставится на основании одновременного измерения уровня креатинина в крови и выпоте. Только больные с обструкцией мочевыводящих путей могут иметь креатинин в выпоте выше, чем в крови. Когда обструкция мочевыводящих путей купирована, выпот быстро исчезает.
Микседема.
Большинство больных микседемой и плевральным выпотом имеют сопутствующий перикардиальный выпот. При сочетании плеврального выпота с перикардиальным жидкость обычно имеет характер транссудата. При наличии изолированного плеврального выпота у больных микседемой жидкость имеет пограничный характер между экссудатом и транссудатом. Механизм формирования выпота неизвестен. Возможно, играет роль снижение функциональной активности лимфатической системы из-за низкого уровня тиреоидных гормонов. Лечение направлено на терапию
606
основного заболевания - проводится заместительная терапия тиреоидными гормонами.
Лечение.
Основными принципами лечения плевритов являются:
а) при сухом плеврите наряду с проведением активной терапии по поводу основного заболевания с целью обезболивания назначают анальгетики, вплоть до наркотических и нестероидные противовоспалительные препараты;
б) этиотропная терапия с учетом чувствительности микроорганизма к антибиотикам. До получения результатов бактериологического исследования – клиндамицин 600 мг в/в 3 раза в сутки, бензилпенициллин (натриевая соль) по 2-10 млн. ЕД/сутки в/в в сочетании с метронидазолом по 500-700 мг 4 раза в сутки;
в) дезинтоксикационная терапия при необходимости: в/в капельно раствор Рингера, 5% раствор глюкозы. Для коррекции белкового дефицита проводится переливание 150 мл 10% раствора альбумина, 200 - 400 мл нативной или свежезамороженой плазмы 1 раз в 2-3 дня 2-3 раза, в/м 1 мл ретаболила 1 раз в 2 недели, 2-3 инъекции;
г) при показаниях проводятся процедуры, которые по мере увеличения их инвазивности включают: диагностический торакоцентез, лечебный торакоцентез, дренирование плевральной полости, дренирование плевральной полости с назначением тромболитиков, торакоскопические операции и торакотомия с декортикацией. Метод лечения изменяется при его неэффективности в течение 1–2 суток.
Осложнением терапевтической плевральной пункции является повреждение острым концом иглы расправляющегося легкого, что сопровождается развитием пневмоторакса, гемоторакса. Риск выше у больных после лучевой терапии и предшествующих множественных торакоцентезов. Рекомендовано не более трех торакоцентезов. При невозможности полного удаления жидкости и наличии любого из перечисленных выше факторов необходимо дренирование.
Дренирование плевральной полости. Вопрос о дренировании плевральной полости должен решаться совместно с хирургом (торакальным хирургом).
Видеоторакоскопия.
При неэффективности дренажа показана лечебная торакоскопия. Во время торакоскопии возможно взять биопсию плевры, удалить фибринозные перемычки, разделяющие выпот.
607
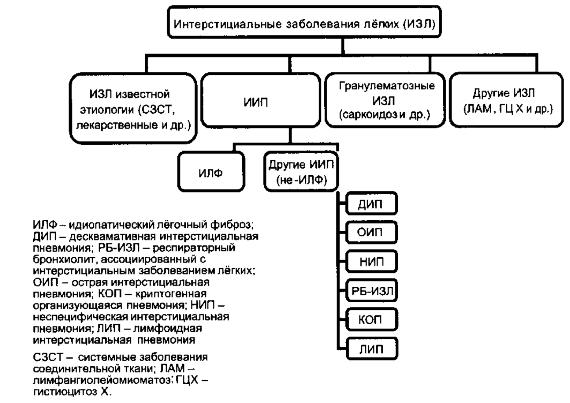
ГЛАВА 6. ИДИОПАТИЧЕСКИЕ ИНТЕРСТИЦИАЛЬНЫЕ ПНЕВМОНИИ
Идиопатические интерстициальные пневмонии (ИИП)
объединяют несколько заболеваний из группы интерстициальных заболеваний лёгких (ИЗЛ), характеризующихся многими сходными признаками:
-неизвестная природа заболеваний;
-прогрессирующая одышка при физических нагрузках;
-кашель, чаще непродуктивный;
-крепитация при аускультации лёгких;
-диффузные изменения на рентгенографии и компьютерной томографии лёгких;
-рестиктивные вентиляционные изменения (снижение лёгочных объёмов), снижение диффузионной способности лёгких, расширение альвеолоартериального градиента (АаРО2).
Классификация ИЗЛ представлена на рисунке 6-1.
Рис. 6-1. Классификация диффузных паренхиматозных
заболеваних лёгких (Пульмонология. Национальные рекомендации, 2009).
Для русскоязычных врачей понятие "интерстициальная пневмония" традиционно связано с воспалительным заболеванием паренхимы легких вирусной или бактериальной природы (атипичные микроорганизмы), что может вносить определенную путаницу при обсуждении проблемы ИИП, поэтому в некоторых согласительных документах подчеркивается, что эквивалентом термина "пневмония"
608

является "пневмонит" – термин, более привычный для употребления в контексте ИЗЛ. В таблице 6-1 представлена классификация ИИП.
Таблица 6- 1
Клинико-патологическая классификация идиопатических интерстициальных пневмоний
Гистологический |
|
|
Клинический диагноз |
|
|||||
паттерн |
|
|
|
|
|
|
|
|
|
Обычная |
интерстициальная |
Идиопатический лёгочный фиброз |
|
||||||
пневмония |
|
|
|
|
|
|
|
|
|
Неспецифическая |
|
|
Неспецифическая интерстициальная |
|
|||||
интерстициальная пневмония |
|
пневмония |
|
|
|
|
|||
Организующаяся пневмония |
|
Криптогенная организующаяся пневмония |
|
||||||
Диффузное |
альвеолярное |
Острая интерстициальная пневмония |
|
||||||
повреждение |
|
|
|
|
|
|
|
|
|
Респираторный бронхиолит |
|
Респираторный бронхиолит, ассоции- |
|
||||||
|
|
|
|
рованный с интерстициальным заболе- |
|
||||
|
|
|
|
ванием лёгких |
|
|
|
||
Макрофагальная |
|
|
Десквамативная интерстициальная |
|
|||||
интерстициальная пневмония |
|
пневмония |
|
|
|
|
|||
Лимфоцитарная |
|
|
Лимфоцитарная интерстициальная |
|
|||||
интерстициальная пневмония |
|
пневмония |
|
|
|
|
|||
Примечание.Пульмонология. |
Национальные рекомендации, 2009. |
|
|||||||
Особенности морфологической картины больных с ИИП пред- |
|||||||||
ставлены в таблице 6-2. |
|
|
|
|
Таблица 6- 2 |
||||
|
|
|
|
|
|
|
|
||
Морфологические особенности больных с идиопатическими |
|
||||||||
|
интерстициальными пневмониями |
|
|
||||||
Морфологический |
Гистологическая картина |
|
|
|
|||||
тип ИИП |
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
ОбИП |
|
Нарушение |
архитектуры |
лёгких, |
фиброз |
с |
|||
|
|
«сотовыми» изменениями, фокусы фибро-бластов. |
|||||||
|
|
Неоднородность данных |
изменений |
в биоптате |
|||||
|
|
(временная гетерогенность) |
|
|
|
||||
НИП |
|
Вариабельное интерстициальное воспаление и |
|
||||||
|
|
фиброз; однородность данных изменений в биоптате; |
|||||||
|
|
фибробластические фокусы очень редки или |
|
||||||
|
|
отсутствуют |
|
|
|
|
|
||
ЛИП |
|
Выраженная |
лимфоцитарная |
инфильтрация |
|||||
|
|
интерстиция |
часто |
ассоциирована |
с |
||||
|
|
перибронхиальными |
лимфоидными |
фолликулами |
|||||
|
|
(фолликулярный бронхиолит) |
|
|
|||||
ДА |
|
Диффузный |
процесс. |
Утолщение |
альвеолярных |
||||
|
|
перегородок, организация альвеол, гиалиновые |
|||||||
|
|
мембраны |
|
|
|
|
|
|
|
609
ОП |
Лёгочная архитектоника сохранена. Пятнистое |
|||||
|
распространение |
|
полиповидной |
грануляционной |
||
|
ткани в дистальных воздухоносных путях |
|
||||
ДИП |
Равномерное |
поражение |
паренхимы |
лёгких. |
||
|
Альвеолярные макрофаги в просвете альвеол, |
|||||
|
минимальное поражение интерстиция |
|
||||
РБ-ИЗЛ |
Бронхоцентричная |
аккумуляция |
альвеолярных |
|||
|
макрофагов, минимальное воспаление и фиброз |
|||||
ОбИП – обычная интерстициальная пневмония; НИП – неспецифическая интерстициальная пневмония; ЛИП – лимфоидная интерстициальная пневмония; ДА – диффузное альвеолярное повреждение; ОП– организующаяся пневмония; ДИП – десквамативная интерстициальная пневмония; РБ-ИЗЛ – респираторный бронхиолит, ассоциированный с интерстициальным заболеванием лёгких.
Примечание:Пульмонология. Национальные рекомендации, 2009.
Идиопатический лёгочный фиброз.
Идиопатический лёгочный фиброз (ИЛФ) является одним из наиболее часто встречающихся заболеваний из группы ИИП. Картину ИЛФ в 1960 г. описал Scadding, и он же впервые ввёл термин «фиброзирующий альвеолит». Возможно, что самое первое описание ИЛФ принадлежит Rindfleisch, описавшим в 1897 г. «кистозный цирроз лёгких»
– заболевание лёгких, характеризующееся уплотнением и сморщиванием паренхимы лёгких и формированием «сотового лёгкого».
В Международном согласительном документе ATS/ERS (2000) предложено следующее определение ИЛФ:ИЛФ является специфической формой хронической интерстициальной фиброзирующей пневмонии, ограниченной лёгкими, и ассоциированной с гистологической картиной обычной интерстициальной пневмонии по данным хирургической (торакоскопической или открытой) биопсии лёгких. \
В нашей стране синонимами ИЛФ являются «идиопатический фиброзирующий альвеолит» (ИФА) и «криптогенный фиброзирующий альвеолит», получивший большее распространение в Великобритании. Понятия «идиопатический» и «криптогенный», несмотря на небольшое смысловое различие, в настоящее время принято считать синонимами, обозначающими скрытую, неясную природу заболевания.
ИФА (синонимы: болезнь или синдром Хаммена - Рича, синдром Скеддинга, диффузный прогрессирующий интерстициальный фиброз легких, фиброзная дисплазия легких и др.) - своеобразный патологический процесс характеризующийся прогрессирующим поражением интерстициальной ткани легких, воспалением и фиброзом легочного интерстиция и воздухоносных пространств, дезорганизацией структурнофункциональных единиц паренхимы, что приводит к развитию рестриктивных изменений легких, нарушению газообмена.
610
Этиология неизвестна. Среди возможных этиологических факторов выделяют курение, определенные виды силикатной пыли. Обсуждается вирусная природа заболевания, генетическая предрасположенность.
Патогенез остается неясным. Основным патогенетическим механизмом, определяющим клиническую картину, является развитие альвеолярно-капиллярного блока. От степени его выраженности во многом зависят степень снижения диффузионной способности легких и, соответственно, степень выраженности артериальной гипоксемии, дыхательной недостаточности и их клинических проявлений.
Снижение диффузионной способности альвеолярно-капиллярной мембраны связано в первую очередь с фиброзом межальвеолярных перегородок и потерей альвеолярным эпителием дыхательных функций в связи с метаплазией его в кубический. Однако сопротивление альвеолярнокапиллярной мембраны газообмену составляет лишь половину общего диффузионного сопротивления. Снижение диффузионной способности легких во многом зависит от степени нарушения перфузии, что обусловливается уменьшением поверхности контакта альвеолярного воздуха с кровью альвеолярных капилляров и сокращением времени контакта. Перечисленные механизмы, а также рефлекторное сужение сосудов легких вследствие эндокапиллярной гипоксии способствуют повышению давления в легочной артерии (рефлекс Эйлера-Лильестранда) и развитию легочного сердца. Доля веноартериального шунта сравнительно невелика - около 6 %.
Предполагается, что в интерстициальной ткани легких снижается распад коллагена и повышается его синтез фибробластами и альвеолярными макрофагами. Повышению синтеза коллагена способствует увеличение числа отдельных субпопуляций лимфоцитов, которые реагируют на коллаген легочной ткани как на чужеродный белок и продуцируют лимфокины, стимулирующие образование коллагена. Имеет значение также снижение продукции лимфоцитами «ингибиторного фактора», тормозящего в обычных условиях синтез коллагена. Многие авторы относят синдром Хаммена — Рича к аутоиммунным заболеваниям, при которых угнетена функциональная активность Т-супрессоров, что приводит к гиперпродукции различных классов иммуноглобулинов В- лимфоцитами. Образующиеся в крови комплексы антиген — антитело (ЦИК) откладываются в стенках мелких сосудов легких. Основной причиной длительного персистирования ЦИК является дефект в функциональной активности Fc-фрагментов IgG. Под влиянием ЦИК, лизосомальных фрагментов альвеолярных макрофагов и нейтрофилов происходит повреждение легочной ткани, уплотнение. утолщение межальвеолярных перегородок, облитерация альвеол и капилляров фиброзной тканью.
В настоящее время наиболее привлекальной является гипотеза, согласно которой ИЛФ – «эпителиально-фибробластическое» заболевание. Согласно данной модели комплексное взаимодействие между
611
повреждением эпителиальных клеток и мезенхиамальными клетками приводит к дезрегуляции механизмов восстановления с избыточной продукцией профибротических цитокинов, экстрацелюллярного матрикса и нарушенным ангиогенезом.
Патологическая анатомия. Гистологические изменения в легочной ткани варьируют, что зависит не только от особенностей самого процесса у конкретного больного, но и от фазы (стадии) заболевания.
Различают 5 степеней патоморфологических изменений в легочной ткани у больных ИЛФ:
Iстепень: отек межальвеолярпых перегородок, клеточная инфильтрация, извилистость капилляров.
IIстепень: экссудация серозно-фиброзной жидкости (богатой белком и окрашивающейся эозином) и клеточная экссудация в альвеолы, что приводит к облитерации альвеолярного пространства (внутриальвеолярный фиброз). Другой путь организации альвеолярного экссудата - резорбция его в межальвеолярные перегородки с уплотнением
ифиброзом последних. Оба эти варианта могут сосуществовать.
IIIстепень: вовлечение в процесс бронхиол с образованием мелких кист и разрушением структуры альвеол.
IV степень: нормальная структура легочной ткани полностью нарушается, кистозные полости постепенно увеличиваются.
V степень: образование так называемого «сотового (или ячеистого) легкого». Кисты достигают 1 см в диаметре.
Клиническая симптоматика: наиболее часто ИФА встречается в возрастном диапазоне от 40 до 49 лет. Соотношение мужчин и женщин 2:1 Патогномоничных, характерных только для ИФА, признаков болезни нет. Начало может быть незаметным или связывается больными с перене-
сенной острой респираторной инфекцией, гриппом и проявляется возникновением одышки при умеренной физической нагрузке. Неуклонно прогрессирующая одышка - один из наиболее характерных и постоянных признаков ИФА. Иногда, как первый признак болезни, пациенты отмечают кашель (сухой или со скудной слизистой мокротой), к которому затем присоединяется прогрессирующая одышка. По мере прогрессирования заболевания кашель может усиливаться и сопровождаться болями в грудной клетке неврологического характера. Характерна жалоба на невозможность глубокого вдоха.
У некоторых больных первым проявлением болезни может быть повышение температуры тела до 38-39°С, лишь потом возникает одышка и кашель. Около 5% больных отмечают периодическое кровохарканье.
Одним из признаков болезни, свидетельствующих (наряду с другими) о прогрессировании патологического процесса в легких, является похудание.
Артралгии (в том числе утренняя скованность суставов), мышечные боли, перемежающееся повышение температуры тела до субфебрильных или фебрильных цифр, синдром Рейно отмечаются у половины больных
612
ИФА. Такая высокая частота поражения суставов является дополнительным аргументом участия аутоиммунных нарушений в патогенезе данной патологии. У всех больных отмечается слабость и быстрая утомляемость.
При осмотре больного обращает на себя внимание цианоз различной степени выраженности (от акроцианоза до диффузного). Степень его выраженности зависит от тяжести заболевания. На ранних этапах хронического течения болезни цианоз может появляться только при физической нагрузке, но по мере прогрессирования болезни он усиливается. При острых формах заболевания цианоз является одним из ранних признаков.
У пациентов обращает на себя внимания изменение ногтевых фаланг, связанных с хронической гипоксией (симптом «барабанных палочек» и «часовых стекол»). Скорость формирования этих симптомов зависит от активности, длительности патологического процесса и выраженности дыхательной недостаточности.
При перкуссии легких над областью поражения отмечается притупление перкуторного тона (чаще это нижние отделы легких).
При аускультации выслушивается крепитация на вдохе (чаще на высоте вдоха). Этот звуковой феномен в литературе называют «треском целлофана». Часто это двусторонняя крепитация, лучше выслушивается по задней и средней подмышечным линиям, а также между лопатками. Крепитация не всегда являетя постоянным симптомом ИФА. При острой форме болезни крепитация может выслушиваться даже при нормальной рентгенологической картине, в то же время ее может не быть при хроническом течении и имеющих место изменениях на рентгенограмме; она может исчезать и при адекватной терапии.
Характерным аускультативным признаком ИФА является ослабленное везикулярное дыхание (укорочение фазы вдоха и выдоха). Жесткое дыхание, сухие хрипы могут возникать при присоединении эндобронхита.
При наличии легочной гипертензии наблюдается акцент П тона над легочной артерией.
По мере прогрессирования заболевания появляются признаки дыхательной недостаточности и лёгочного сердца: диффузный серопепельный цианоз, акцент П тона над лёгочной артерией, тахикардия, ритм галопа, набухание шейных вен, периферические отёки (появляются все признаки недостаточности кровообращения по правожелудочковому типу). Снижение массы тела больных вплоть до развития кахексии является характерным признаком терминальной стадии ИЛФ.
613
Критерии диагноза идиопатического фиброзирующего альвеолита
(ATS/ERS, 2000).
Большие критерии.
1. Исключение других интерстициальных заболеваний легких, вызванных известными причинами, такими как прием лекарств, экспозиция к вредным факторам внешней среды, системные заболевания соединительной. ткани
2.Изменения функции внешнего дыхания, включающие
рестриктивные |
изменения |
и |
нарушение |
газообмена. |
3.Двусторонние ретикулярные изменения в базальных отделах легких
сминимальными изменениями по типу "матового стекла", по данным
компьютерной томографии высокого разрешения. 4. По данным трансбронхиальной биопсии или бронхоальвеолярного лаважа, нет признаков, свидетельствующих об альтернативном диагнозе.
Малые критерии.
1.Возраст старше 50 лет.
2.Незаметное, постепенное появление диспноэ при физической нагрузке.
3.Длительность заболевания более 3 месяцев.
4.Инспираторная крепитация в базальных отделах легких.
Должны присутствовать все 4 большие критерия и как минимум 3 из 4 малых критериев.
Проведение хирургической биопсии лёгких может быть рекомендовано больным с атипичными клиническими и КТВР-признаками ИЛФ при взвешенном риске инвазивного характера данной процедуры
Каких-либо характерных изменений со стороны крови не выявлено. Лейкоцитоз со сдвигом влево, увеличение СОЭ, диспротеинемия в основном за счет увеличения фракции γ-глобулинов, умеренное увеличение сиаловых кислот могут указывать на воспалительную стадию заболевания (стадию альвеолита). Показатели гематокрита, как правило, в пределах нормы.
У больных ИЛФ может быть повышен сывороточный уровень общей лактатдегидрогеназы (ЛДГ), возможным источником которой являются альвеолярные макрофаги и альвеолоциты II типа.
К числу сывороточных маркёров при ИЛФ относятся протеины сурфактанта А и D и муцин-антигены KL-6, альвеоломуцин 3EG5.
Функциональные легочные тесты.
ИФА относится к рестриктивным легочным заболеваниям, поэтому его характерными функциональными особенностями являются снижение легочного комплаенса и статических легочных объемов (общей емкости легких, функциональной остаточной емкости, остаточного объема). Соотношение ОФВ1/ЖЕЛ (коэффициент Тиффно) находится в пределах нормы или даже повышено. Одним из ранних признаков заболевания
614
является снижение DLCO(диффузионная способность легких для окиси углерода). Выраженное снижение DLCO (<50%), как правило, ассоциировано с развитием легочной гипертензии и расширением альвеолоартериального градиента АаРО2 при физической нагрузке.
Реже при оценке ИФА используют анализ кривой давление–объемна начальных этапах, при заболеваниях данной группы она смещена вправо и вниз, что отражает снижение растяжимости легких и уменьшение объема легких.
На ранних этапах заболевания газовый анализ артериальной крови,
выполненный в покое, практически не изменен, хотя при физической нагрузке уже происходит десатурация, что отражается снижением парциального напряжения кислорода артериальной крови РаО2 и расширением АаРО2. По мере прогрессирования заболевания гипоксемия появляется и в покое и сопровождается гипокапнией, отражающей особенности дыхательного паттерна больных – частого поверхностного дыхания (rapid shallow breathing), гиперкапния появляется только на терминальных этапах ИЛФ. Основным механизмом гипоксемии при ИЛФ является вентиляционно-перфузионный дисбаланс.
Бронхоальвеолярныйлаваж.
Бронхоальвеолярный лаваж (БАЛ), позволяет оценить течение, прогноз и мониторирование воспаления при терапии заболевания. Характерными находками БАЛ при ИЛФ являются повышение общего числа клеток, увеличение числа нейтрофилов и эозинофилов. Однако данные признаки встречаются и при других ИЗЛ (асбестоз, лекарственнообусловленные легочные фиброзы, силикозы), что ограничивает диагностическую ценность БАЛ. Эозинофилия БАЛ, как абсолютное число, так и процент эозинофилов, может быть связана с неблагоприятным прогнозом ИЛФ.
При рентгенологическом исследовании легких на ранних этапах обнаруживается усиление легочного рисунка за счет интерстициального компонента. Эти изменения чаще локализуются на периферии базальных отделов легких. По мере прогрессирования заболевания интерстициальные изменения становятся все более выраженными, распространяясь без четкой границы в апикальном и центральном направлениях. Появление на рентгенограммах небольших участков просветления свидетельствует об образовании кистозных полостей. На заключительных этапах болезни при рентгенологическом исследовании выявляются просветления (кисты) размером до 1 см в диаметре - переход в ячеистое легкое. Изменения в паренхиме легких сопровождаются значительным ограничением подвижности куполов диафрагмы и высоким их стоянием, что некоторыми авторами считается одним из характерных (но не патогномоничных) рентгенологических признаков ИЛФ (рис. 6-2, 6-3).
Локализация поражений может быть самой различной: в нижних легочных полях, в средних, иногда в верхних участках легких. У большинства больных поражение легких симметричное.
615
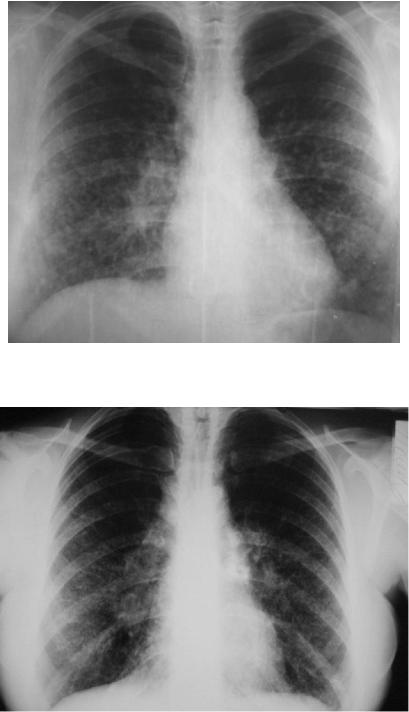
Рис. 6-2. Типичная рентгенографическая картина ИЛФ. Двусторонние изменения в нижних отделах легких.
Рис. 6-3. Типичная рентгенологическая картина ИФЛ: двустороннее поражение, признаки легочной гипертензии.
КТВР (компьютерная томография высокого разрешения).
Более ценную информацию можно получить при помощи КТВР (highresolution computed tomography). Характерными находками при КТВР являются нерегулярные линейные тени, кистозные просветления, фокальные очаги снижения прозрачности легочных полей по типу "матового стекла" (не более 30% от общей площади легких), утолщение и иррегулярность бронхиальных стенок. Кроме того, в областях с наиболее выраженными изменениями часто выявляют признаки дезорганизации легочной паренхимы
итракционные бронхоэктазы. Наибольшие изменения выявляют в базальных
исубплевральных отделах легких. КТВР-паттерн и распределение
616
изменений в большинстве случаев являются патогномоничными для ИЛФ. КТВР позволяет исключить другие ИЗЛ, имеющие сходную
клиническую картину: хронический гиперчувствительный пневмонит (центролобулярные узелки, отсутствие "сотовых" изменений, преимущественное поражение верхних и средних отделов легких), асбестоз (плевральные бляшки, паренхиматозные ленты фиброза), ДИП (протяженные изменения по типу "матового стекла").
КТВР-признаки отражают морфологические признаки фиброзирующего альвеолита: ретикулярный паттерн соответствует фиброзу, а паттерн "матового стекла" клеточной инфильтрации.
Показания к хирургической биопсии лёгких у больных с ИЗЛ:
-клиническая картина, не типичная для ИЛФ;
-возраст менее 50 лет;
-системные признаки заболевания;
-рентгенологическая картина, не характерная для ИЛФ;
-«нормальная» рентгенологическая картина;
-быстрое прогрессирование заболевания;
-рецидивирующие пневмотораксы;
-польза от правильного диагноза превышает риск хирургической манипуляции.
Открытая биопсия легких является "золотым"
диагностическим стандартомпри ИЛФ и позволяет не только установить диагноз, но и предсказать прогноз заболевания и возможный ответ на терапию. Менее инвазивным методом биопсии, является торакоскопическая биопсия легких (ТСБЛ).
Трансторакальная пункционная биопсия противопоказанапри легочной гипертензии, выраженной дыхательной и сердечной недостаточности.
Дифференциальная диагностика ИФА проводится со следующими заболеваниями: экзогенным аллергическим альвеолитом, токсическим фиброзирующим альвеолитом,острой двусторонней пневмонией; саркоидозом легких II-III стадии,гематогенно-диссеминиро ванным туберкулезом легких, поражением легких при дифферинциальных болезнях соединительной ткани, таких как системная красная волчанка, ревматоидный артрит, ревматизм, системная склеродермия, узелковый периартериит, дерматомиозит; раковым лимфангитом; бронхиоло-альвеолярным раком, идиопатическим гемосидерозом легких,синдромом Гудпасчера,альвеолярным протеинозом легких, лейомиоматозом, гистиоцитозом X, пневмокониозами и пневмомикозами.
Лечение. Противовоспалительная терапия.
Современная терапия ИФА построена в основном на противовоспалительной терапии (кортикостероиды и цитостатики): монотерапия глюкокортикостероидами (ГКС), комбинация ГКС с азатиоприном и комбинация ГКС с циклофосфаном.
617
Современные рекомендации терапии идиопатического фиброзирующего альвеолита (ATS/ERS, 2000).
Кортикостероиды(преднизолон или другие стероидные препараты в дозе, эквивалентной преднизолону) 0,5 мг/кг "тощей" массы тела в сутки в течение 4 нед.; 0,25 мг/кг идеальной массы тела в сутки в течение 8 недель.
Снижать дозу до 0,125 мг/кг в сутки или 0,25 мг/кг через день плюс Азатиоприн 2–3 мг/кг "тощей" массы тела в сутки Максимальная доза 150 мг в сутки.
Начальная доза составляет 25–50 мг в сутки, дозу повышают на 25 мг каждые 1–2 нед до достижения максимальной дозы
или Циклофосфамид
2 мг/кг "тощей" массы тела в сутки. Максимальная доза 150 мг в сутки.
Начальная доза составляет 25–50 мг в сутки, дозу повышают на 25 мг каждые 1–2 нед до достижения максимальной дозы
Терапия проводится как минимум в течение 6 месяцев. Ответ на терапию определяется клиническими симптомами, данными рентгенографии и функциональными показателями.
Обязательно тщательное мониторирование побочных эффектов терапии. Основой медикаментозной терапии ИЛФ по-прежнему остаются
таблетированные ГКС.
Обычно начальная суточная доза преднизолона составляет 1,0 мг/кг идеального веса/сутки (максимум до 80 мг/с). Чаще всего всю суточную дозу назначают в один приём, после завтрака. Через 4 недели проводится оценка переносимости такой терапии. Критерии оценки эффективности терапии при ИЛФ представлены в таблице 6-3. Если произошло улучшение или стабилизация функциональных показателей, то в течение последующих трёх месяцев суточную дозу преднизолона уменьшают до 0,5 мг/(кг х сут). В течение дальнейших 6 месяцев при улучшении или стабилизации течения заболевания дозу преднизолона постепенно уменьшают до 0,25 мг/(кг х сут). При отсутствии ответа на ГКС – добавление азатиоприна. Наиболее частые побочные эффекты – повышение веса, кожные изменения, раздражительность, артериальная гипертензия, кушингоид, гипергликемия, катаракта, глаукома, тревога, депрессия, остеопороз, миопатия. Соотношение «польза/риск» при назначении преднизолона больным ИЛФ смещено в пользу риска при возрасте старше 70 лет, ожирении (ИМТ >35 кг/м2), остеопорозе, сахарном диабете.
618
Таблица 6-3
Оценка ответа на терапию у больных с идиопатическим лёгочным фиброзом
|
Улучшение |
Стабилизация |
Ухудшение |
Симптомы |
↓ одышки и |
Нет изменений |
↑ одышки и |
|
кашля |
|
кашля |
Rh-графия и КТ |
↓ изменений |
Нет изменений |
↑ изменений |
ЖЁЛ |
↑>10% |
Изменения ±10% |
↓>10% |
DLoo |
↑>15% |
Изменения ±15% |
↓>15% |
АаРО2 |
↓>10 мм рт.ст. |
Изменения ±10 мм рт.ст. |
↑>10 мм рт.ст. |
Примечание.Пульмонология. Национальные рекомендации, 2009.
Антифиброзная терапия.
Альтернативный подход, сфокусированного на снижении избыточной депозиции матрикса (коллагена) в лёгких или ускорению распада коллагена. К числу антифиброзных препаратов относятся D- пеницилламин, колхицин, интерферон-γ-lb, пирфенидон.
D-пеницилламинредко блокирует образование поперечных связей коллагена и препятствует дальнейшему фиброзообразованию. Препарат, как правило, более эффективен при лечении интерстициальных пневмоний на фоне СЗСТ. В настоящее время D-пеницилламин применяют довольно редко, так как препарат обладает серьёзными побочными эффектами (в том числе нефротический синдром). терапия больных ИЛФ комбинацией D-пеницилламином (600 мг/сут) с преднизолоном по своему клиническому эффекту не имела отличий от монотерапии преднизолоном(В Selman и соавт).
Колхицинспособен уменьшать продукцию макрофагами фибронектина, инсулиноподобного фактора роста, снижать конверсию проколлагена в коллаген, ингибировать миграцию и пролиферацию фибробластов. Препарат назначается в дозе 0,6–1,2 мг/сут, обычно в комбинации с низкими дозами преднизолона (10 мг/сут). Побочные эффекты: диарея, миопатия.
Интерферон-γ-1b подавляет пролиферацию фибробластов и продукцию матричного протеина соединительной ткани и трансформирующего фактора роста β (TGF-β): 200 мкг подкожно 3 раза в неделю) в сочетании с преднизолоном (7,5 мг/сут) в течение года. Основными побочными эффектами интерферона являются ознобы, лихорадка и мышечные боли.
Перспективным антифиброзным препаратом является пирфенидон(в дозе до 3,6 г/сут). Препарат блокирует митогенные эффекты профибротических цитокинов, снижает синтез экстрацеллюлярного матрикса и ингибирует эффекты TGF-β.
Антиоксидантная терапия.
N-ацетилцистеин (NAC) per os в дозе 1,8 г/сут в течение 12 нед у больных, уже получающих иммуносупрессивную терапию, приводит к
619
достоверному улучшению функциональных лёгочных показателей и повышению уровня глютатиона в жидкости БАЛ. NAC (352 мг/с) у больных ИЛФ может быть использован в виде ингаляций.
В настоящее время ведущие эксперты при терапии ИЛФ отдают предпочтение схеме терапии, включающей три препарата (преднизолон, азатиоприн и NAC).
Новые препараты для терапии ИЛФ представлены в таблице 6-4. Таблица 6-4
Новые препараты для терапии идиопатического лёгочного фиброза
Препарат |
|
Обоснование и безопасность |
Босентан |
|
Эндотелии-1, секретируемый эндоте-лиальными и |
|
|
гладкомышечными клетками, обладает вазоактивным, мито-генным |
|
|
и иммуномодуляторным эффек-тами. Он повышает продукцию TGF- |
|
|
р и обладает независимым стимуляторным эффектом на |
|
|
фибробласты. Босентан является антагонистом рецепторов |
|
|
эндотелина А и В |
Каптоприл, |
|
Ангиотензин II – вазоактивный пептид с митогеным эффектом в |
лозартан |
|
отношении фибробластов. Пролиферация фибро-бластов, |
|
|
активированная ангиотензинном II, может быть связана с |
|
|
аутокринной продукцией TGF-p. Препараты ингибируют АПФ и |
|
|
предотвращают Fas-индуцированый аполтоз альвеолярных |
|
|
эпителиальных клеток человека. Препараты ингибируют |
|
|
пролиферацию фибробластов in vitro и уменьшают фиброз лёгких in |
|
|
vivo |
Циклоспорин |
Ингибиторный эффект Т-лимфоцитов. Подавляет отсроченные |
|
|
|
аллергические реакции, отторжение аллографта и продукцию |
|
|
антител на Т-клетки-зависимые антигены |
Этанерсепт |
|
Этанерсепт – антагонист ФНО-а; |
|
|
ФНО-а – цитокин с митогенным эффек-том на фибробласты и синтез |
|
|
коллагена |
Иматиниб |
|
Ингибитор нескольких протеинтиро-зиновых киназ, которые играют |
|
|
роль в пролиферации опухолевых клеток и мезенхимальных клеток, |
|
|
в том числе и фибробластов; Ингибирует передачу сигнала PDGF, |
|
|
что, как показано на животных моделях, уменьшает фибро- |
|
|
пролиферативный ответ |
Фактор |
роста |
Индуцирует пролиферацию альвеоло-цитов II типа (анормальная |
кератиноцитов |
стимуляция альвеолярных эпителиальных клеток может приводить к |
|
|
|
неблагоприятным последствиям, повышая интраальвеоляр-ную |
|
|
антифибринолитическую активность и секретируя фиброгенные |
|
|
цитокины). |
|
|
Усиливает реэпителизацию ран без индукции формирования рубца |
|
|
или фиброза |
Ловастатин |
|
Блокирует формирование грануляцион-ной ткани путём индукции |
|
|
апоптоза фибробластов in vitro и in vivo |
Микофенолата |
Нарушает функцию лимфоцитов путём блокирования биосинтеза |
|
мофетил |
|
пуринов через ингибирование фермента |
(CellCept) |
|
инозинмонофосфатдегидрогеназы |
620
Сиролимус |
Иммуносупрессивный агент, исполь-зуемый при трансплантации, с |
(Rapamycin) |
антипро-лиферативнми свойствами. |
|
Ингибирует пролиферацию звёздчатых клеток, что снижает |
|
потенциальный фибротический ответ при рецидивиру-ющих забо- |
|
леваниях печени |
Примечание. Пульмонология. Национальные рекомендации, 2009.
Трансплантация лёгких является на сегодняшний день наиболее радикальным способом терапии ИЛФ. Выживаемость больных в течение 3 лет после трансплантации по поводу ИЛФ составляет около 60%.
Показания к трансплантации лёгких:
•диспноэ III-IVкласса по NYHA;
•гипоксемия при физической нагрузке;
•снижение ЖЁЛ или ФЖЁЛ 60–70% от должных;
•снижение DLCО< 50% от должных.
Ограничивающим фактором для трансплантации часто является пожилой возраст больных ИЛФ и быстрое прогрессирование заболевания.
621
ЛИТЕРАТУРА
1.Белоусова, Е.А. Язвенный колит и болезнь крона /
Е.А.Белоусова. – М.: «Триада», - 2004. – 128с.
2.Белялов, Ф.И. Аритмии сердца/ Ф.И.Белялов. – М.:МИА, – 2006.
–352 с.
3.Биохимия / Под ред. Е.С. Севериной. – М.: Медицина, 2003г.
4.Болезни сердца / Под ред. Р.Г. Оганова, И.Г. Фоминой. – М.: ЗАО издательство «Литтера», 2006. – 1326 с.
5.Внутренние болезни: учеб. для студентов мед. вузов : в 2 т./ Под ред. Н.А. Мухина, В.С. Моисеева, А.И. Мартынова.-2-е изд., испр. и доп. –
Т.2. – М.:ГЭОТАР-Медиа. Т. 2 .-2006- 581 с.:ил.
6.Внутренние болезни: учеб. для студентов мед. вузов: в 2 т./ Под ред. Н.А. Мухина, В.С. Моисеева, А.И. Мартынова .-2-е изд., испр. и доп. –
Т.1. – М.:ГЭОТАР-Медиа,– 2006. – 649 с.:ил.
7.Воробьев, П.А. Анемический синдром в клинической практике / П.А.Воробьев. – М.: Медицина, 2001г.
8.Гастроэнтерология: нац. рук-во / Под ред. акад. РАМН В.Т. Ивашкина, к.м.н. Т.Л. Лапиной. – М.:ГЭОТАР-Медиа, 2008. – 704 с.
9.Гиляревский, С.Р. Диагностика и лечение заболеваний перикарда: современные подходы, основанные на доказательной медицине и собственном опыте/ С.Р.Гиляревский. – М: МедиаСфера, 2004. – 132 с.
10.Глобальная стратегия лечения и профилактики бронхиальной астмы (пересмотр 2011) / Под ред. А.С. Белевского – М.: Рос. респ.
общество, 2012. – 108с.
11.Глобальная стратегия диагностики, лечения и профилактики хронической обчтруктивной болезни легких (пересмотр 2011) / Пер. с англ. под ред. А.С. Белевского. – М.: Рос. респ. общество, 2012. – 80с.
12.Горбаченков А.А. Клапанные пороки сердца/ А.А. Горбаченков, Ю.М. Поздняков. М.: ГЭОТАР – Медиа, 2007 – 112 с.
13.Гринхальх, Т. Основы доказательной медицины:учеб. пособие для студентов мед. вузов и системы послевуз. проф.образования / Т.Гринхальх. – М.: ГЭОТАР-Медиа, 2006. – 240с. – Гриф УМО.
14.Дворецкий, Л.И. ЖДА./ Л.И.Дворецкий. – М.: Ньюдиамед, – 2001
–168 с.
15.Дедов, И.И. Эндокринология: учеб. для студентов мед.вузов / И.И. Дедов, Г.А. Мельниченко, В.В. Фадеев.-М.: Медицина, 2000. – 631 с.: ил. - (Учеб. лит. для студентов мед.вузов). Гриф МЗ РФ
16. Диагностика и лечение болезней почек / Н.А. Мухин, И.Е. Тареев, Е.М. Шилов и др. – М.: ГЭОТАР-Медиа, 2011. – 384 с.: ил.
17.Европейские рекомендации по профилактике сердечнососудистых заболеваний в клинической практике (пересмотр 2012г.). «Российский кардиологический журнал», 2012; 4 (96) Приложение 2. стр. 1-84.
622
18. Кардиология: нац. рук-во |
/ |
под |
ред. |
акад. |
РАМН |
Ю.М. Беленкова, Р.Г. Оганова. – М.: ГЭОТАР-Медиа, 2008. |
– 1232 с. |
||||
19.Кардиология: нац. рук-во |
/ |
под |
ред. |
акад. |
РАМН |
Ю.М. Беленкова, Р.Г. Оганова. – М.: ГЭОТАР-Медиа, 2012. |
– 864 |
с. |
|||
20.Клиническая онкогематология: рук-во для врачей / Под ред. М.А. Волковой. – 2-е изд., перераб. и доп. – М.: ОАО «Издательство Медицина», 2007. – 1120 с.
21.Клинические рекомендации. Пульмонология / Под ред. А.Г. Чучалина – 2-е изд., перераб. и доп. – М.: ГЭОТАР-Медиа, 2011. – 336 с.: ил.
22.Клиническая фармакология: учеб. для студентов мед. вузов / Под pед. В.Г.Кукеса.-3-е изд., пеpеpаб. и доп. – М.: ГЭОТАР-Медиа, 2006. – 936 с.: ил.
23.Клинические рекомендации (стандарты ведения больных). - М.: ГЭОТАР-Медиа, 2008. - 1376 с.
24.Клинические рекомендации. Гастроэнтерология / Под ред. акад. РАМН В.Т. Ивашкина, 2 изд., испр. и доп. – М.:«ГЭОТАР-Медиа», 2009. – 208с.
25.Кушаковский, М.С. Аритмии сердца./ М.С.Кушаковский. - СПб.: Фолиант, – 2007. – 672 с.
26.Маколкин, В.И. Внутpенние болезни: учебник. – 6-е изд., пеpеpаб. и доп / В.И. Маколкин, С.И. Овчаренко, В.А. Сулимов. – М.: «ГЭОТАР-Медиа», 2011. – 768с.: ил.
27.Национальные клинические рекомендациии (ВНОК) – М.: Силицея-полиграф, 2010. – 512 с.
28.Национальные рекомендации ВНОК и ОСН по диагностике и лечению ХСН (третий пересмотр). // Сердечная недостаточность, 2010. – Т.11, №1., 2009. с.62-103.
29.Нефрология: нац. рук-во / Под ред. Н.А. Мухина. – М.: ГЭОТАРМедиа, 2009 г. – 720 с.
30.Нефрология: рук-во для врачей / под ред. И.Е.Тареевой. – М.: Медицина, 2000. – 688 с.
31.Нефрология: Учеб. пособие для послевузовского образования под. ред. Е.М. Шилова. – М.: ГЭОТАР-Медиа, 2007. – 688 с.
32.Программное лечение лейкозов / Под ред. Савченко В.Г.- М., 2008. - 484 с.
33.Рациональная фармакотерапия в нефрологии / Под общ. ред. Н.А. Мухина, Л.В. Козловской, Е.М. Шилова. – М.: Литтерра, 2008. – 640 с.
34.Ревматические болезни / Под ред. В.А. Насоновой, И.В. Бунчука. – М.: Медицина, 1997-523 с.
35.Ревматология: клинические рекомендации / Под ред. акад. РАМН Е.Л. Насонова. 2-е издание испр. и доп. – М.: ГЭОТАР – Медиа, - 2010. – 752 с.
623
36.Ревматология: нац. рук-во / Под ред. Е.Л. Насонова, В.А. Насоновой. - М.: ГЭОТАР-Медиа, 2008. – 720 с.
37.Респираторная медицина: нац. рук-во. в 2х тт. / Под ред. Чучалина А.Г. - М.: ГЭОТАР-Медиа, 2007. - 1616 с.
38.Российский терапевтический справочник. – 2-е издание.– М.: ГЭОТАР-Медиа, 2007 - 976 с.
39.Руководство по гематологии. В 3-х тт. – Т.1 / Под ред., А.И.Воробьева,М.:Ньюдиамед, - 2002. – 280 с.
40.Руководство по гематологии. В 3-х тт. Т.2 / Под ред., А.И.Воробьева,М.:Ньюдиамед, - 2003. – 277 с.
41.Руководство по гематологии / Под ред. А.И. Воробьева. В 3-х тт.
-М.: Ньюдиамед, 2005. – Т.3. – 416 с.
42.Справочник-путеводитель практикующего врача «2000 болезней» / Под ред. акад. РАМН И.Н.Денисова, Ю.Л.Шевченко. - М.: ГЭОТАР-Медиа, 2008. – 1319 с.
43.Циммерман, Ф. Клиническая электрокардиография / Ф.Циммерман. – М.: БИНОВ, - 2008. – 424 с.
44.Чучалин, А.Г. Хронические обструктивные болезни легких / А.Г.Чучалин. – М.: ЗАО « Издательство БИНОМ; СПБ.: Невский диалект; 1998 – С. – 192-216.
45.Шейман, Дж. А.Патофизиология почки / Д.А.Шейман; пер. с англ. д.м.н. Л.З. Певзнера под ред. акад. Ю.В. Наточина
46.Федеральное руководство по использованию лекарственных средств (формулярная система) под ред. А.Г. Чучалина, выпуск XI, М., 2010. – 940 с.
47.Hamm,C.W.Асlassificationofinstableangina revisied / C.W.Hamm, E.Braunwold // Circulation, - 2000. – V.102(1). – P.118-22.
48.Jenborn,L. Ингибиторы фибринолиза при лечении геморрагических расстройств / L.Jenborn // Лечение гемофилии.- 2007. - №42. - С. 5-11.
49.Malfertheiner P, Megraud F, O'Morain C et al. Management of Helicobacter pylori infection – the Maastricht IV. Florence Consensus Report Gut 2012; 61: 646–64.
50.Provan D., Stasi R.,Newland A., Blanchette V. et all/ International consensus report on the ivestigation and managment of primary immune thjmbothitopenia. Blood – 2010 - № 115б - р 168-186.
624
