
- •Методы фракционирования
- •Хроматография
- •Основные понятия хроматографии
- •Основные виды хроматографии
- •Виды хроматографии (продолжение)
- •Виды хроматографии (продолжение)
- •Виды хроматографии (продолжение)
- •Приборы для хроматографического анализа
- •Сорбенты хроматографического
- •Влияние размера частиц сорбента
- •Материалы для хроматографии
- •Газовая хроматография
- •Жидкостная хроматография ВЭЖХ
- •Ионообменная хроматография
- •Гель-фильтрация
- •Сорбенты гель фильтрации
- •Аффинная хроматография
- •Аффинная хроматография
- •Электрофорез
- •Носители, используемые для электрофореза
- •Применение электрофореза в клинике
- •Анализ электрофореграмм:
- •Иммуноэлектрофорез
- •Схема иммуноэлектрофореза
- •Ракетный электрофорез
- •Схема ракетного электрофореза
- •Встречный электрофорез
- •Капиллярный электрофорез
- •БЛАГОДАРЮ ЗА ВНИМАНИЕ !!!

 Материалы для хроматографии
Материалы для хроматографии
В качестве материалов сорбентов используют вещества природного происхождения и синтетические – органические и неорганические полимеры.
Самые распространенные сорбенты - на основе целлюлозы, агарозы, окиси алюминия,
силикагели.
Химическая модификация сорбента - введение каких-либо функциональных групп. При этом можно получить сорбент с требуемыми свойствами, сродством к определенным классам соединений. Пример: силикагель можно легко модифицировать, получая частицы с заданным размером частиц, размером пор, разной удельной поверхностью и т.д.

Газовая хроматография
 Применяется для определения состава лекарственных препаратов, примесей вредных веществ в воздухе, воде, почве, промышленных продуктах; а также в криминалистике и т.д. Позволяет разделить несколько см3 газа или мг жидких (твёрдых) веществ; время анализа от нескольких секунд до нескольких часов.
Применяется для определения состава лекарственных препаратов, примесей вредных веществ в воздухе, воде, почве, промышленных продуктах; а также в криминалистике и т.д. Позволяет разделить несколько см3 газа или мг жидких (твёрдых) веществ; время анализа от нескольких секунд до нескольких часов.
Для газо-адсорбционного варианта хроматографии в качестве сорбента (частицы диаметром 0,1-0,5 мм)используют силикагели, алюмогели, молекулярные сита, пористые полимеры и др. сорбенты с удельной поверхностью 5-500 м2/г.
Для газо-жидкостной хроматографии (ГЖХ) сорбент готовят нанесением жидкости в виде плёнки (высококипящие углеводороды, сложные эфиры, силоксаны и др.) толщиной несколько мкм на твёрдый
носитель с удельной поверхностью 0,5-5 м2/г и более.

 Жидкостная хроматография ВЭЖХ
Жидкостная хроматография ВЭЖХ
Используется для анализа, разделения и очистки синтетических полимеров, лекарственных препаратов, детергентов, белков, гормонов и др. биологически важных соединений. Использование высокочувствительных детекторов позволяет работать с очень малыми количествами веществ (10-11-10-9 г). Часто применяется молекулярно-ситовая хроматография и хроматография по сродству (основана на способности молекул биологических веществ избирательно связываться друг с другом).

Ионообменная хроматография
 Широко распространенный вариант жидкостной хроматографии.
Широко распространенный вариант жидкостной хроматографии.
Используется в аналитических целях и для препаративного разделения веществ, позволяет отделять и разделять заряженные частицы - аминокислоты, белки, карбоновые кислоты. Основа метода – использование в качестве сорбента ионообменника – полимера, модифицированного
введением ионогенных групп. Если матрица имеет отрицательный заряд - катионо-обменник, положительный - анионообменник. Разделение основано на электростатическом взаимодействии ионов подвижной фазы с неподвижными ионогенными группами ионообменника.
Катионо- и анионо-обменники бывают сильными и слабыми.  Сильные ионизированы во всем интервале pH , а слабые лишь в определенном интервал. Ионизацией слабых
Сильные ионизированы во всем интервале pH , а слабые лишь в определенном интервал. Ионизацией слабых
ионообменников можно управлять, меняя pH среды.

Гель-фильтрация
Позволяет разделять молекулы в зависимости от их молекулярных масс. Очень эффективен для разделения белков и других высоко-молекулярных соединений.
Основа метода - различная скорость диффузии молекул с разной молекулярной массой (различными размерами).
Сорбент - гель (мелкие частицы, внутри пронизанные нитями (фибриллами). Диффузия внутрь этих частиц лимитируется подвижностью молекул, которая зависит от их молекулярной массы. Мелкие молекулы легко проникают вовнутрь гранул геля и способны надолго задерживаться внутри гранул, а крупные - не проникают в гранулы и быстро выходят из колонки. Т.е. скорость продвижения мелких молекул будет
меньше скорости движения более тяжелых молекул

Сорбенты гель фильтрации
 Полидекстрановые гели:
Полидекстрановые гели:
Сефадекс – гидрофильный гель, выпускается в сухом
виде, имеет маркировку G и номер, означающий пористость матрицы (количество воды в мл, которое
связывает 10 грамм сухого геля).
Сефакрил – поставляется в набухшем виде (густая
водная суспензия). Достоинства - более высокая (по сравнению с сефадексом) жесткость частиц (можно вести хроматографический процесс при больших
скоростях), более химически стойки. |
Выпускают 5 |
типов с маркировкой S ( от S-200 до |
S-1000 ). |
Гели агарозы: |
|
 Сефароза – поставляется в виде суспензии. Гели её
Сефароза – поставляется в виде суспензии. Гели её
довольно жесткие, но менее чем у сефакрила.

Аффинная хроматография
 Позволяет разделять отдельные ферменты, белки, вирусы.
Позволяет разделять отдельные ферменты, белки, вирусы.
Основа метода - специфические взаимодействия частиц подвижной фазы с сорбентом.
 Сорбент - гель типа агарозы, к которому
Сорбент - гель типа агарозы, к которому
ковалентно привязаны подходящие лиганды (например, антитела или субстрат какого- либо фермента). При прохождении через сорбент подвижной фазы из нее будет сорбироваться только соответствующий фермент (или антиген), который прочно связывается с сорбентом. Удаление фиксированного вещества - избытком растворителя.
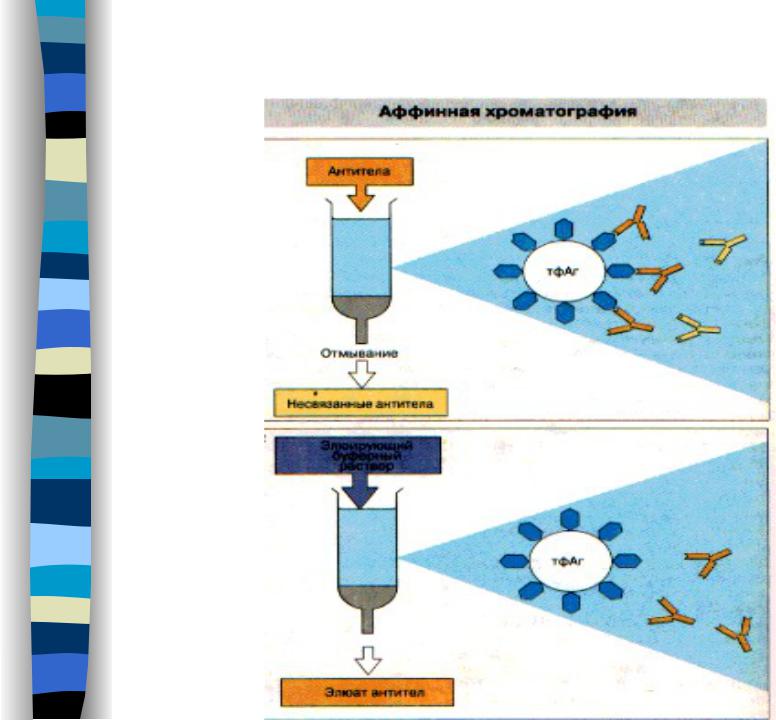
Аффинная хроматография

Электрофорез
Процесс разделения заряженных частиц в электрическом поле. Явление электрофореза обнаружено Рейсом в 1809 г. Применение в клинико-диагностических лабораториях
– с 50-х г. XX в.
Теоретические основы (на примере белка): молекулы белка имеют положительно и отрицательно заряженные группы. Суммарный заряд молекул зависит от рН буфера, в котором растворен белок. При щелочном рН белки выступают как анионы, а в кислой среде - каккатионы (движутся, соответственно, к аноду или катоду). Каждый белок характеризуется определенным значением рН, при котором он не мигрирует, поскольку при этом значении сбалансированы противоположно заряженные группы - изоэлектрическая точка. Изменяя значения рН буфера можно производить разделение белков в электрическом поле.
Применение: разделение белков, липопротеинов, аминокислот (высоковольтный э/ф).

 Носители, используемые для электрофореза
Носители, используемые для электрофореза
Среда-носитель может оказывать влияние на условия электрофореза, изменяя эффективность разделения, так как имеет собственный заряд (процесс электроэндосмоса).
В клинических лабораториях используют 2 типа носителей:
Ацетатцеллюлоза, агар, агароза. Это инертные материалы с порами больших размеров, которые не препятствуют миграции частиц. Степень электроэндосмоса разная, выбирают в соответствии с условиями проводимого разделения.
Крахмальные и акриламидные гели. Эти носители содержат поры, сравнимые по размерам с размерами белковых молекул, что обеспечивает комбинирование эффекта молекулярного сита с электрофоретическим разделением, основанным на распределении заряда. Электрофореграммы, нолученные на таких носителях
содержат больше фракций, чем на ацетатцеллюлозе, агаре и агарозе.
