
- •7.Применения интерференции:
- •8. Дифракция – явление отклонения света от прямолинейного направления распространения при прохождении вблизи препятствий.
- •9.Дифракция Фраунгофера на щели:
- •19. Явище зовнішнього фотоефекту. Рівняння Енштейна.
- •27. Співвідношення невизначеностей Гейзенберга
- •28. Хвильова функція та її властивості. Фізичний зміст.
- •29.Рівняння Шредингера для стаціонарного стану
- •30. Частица в одномерной потенциальной яме.
- •31. Прохождение частицы сквозь потенциальный барьер. Туннельный эффект.
- •1) Коэффициент прозрачности
- •2) Коэффициент отражения
- •33. Опыты Штерна и Герлаха. Спин. Спино-орбитальное взаимодействие.
- •35. Спонтанные и вынужденные переходы
- •36.Вимушене випромінювання. Оптичні квантові генератори та їх застосування.
- •37.Газові лазери. Властивості лазерного випромінювання.
- •42. Собственная проводимость полупроводников.
- •43. Примесная проводимость полупроводников.
- •44. Фотопроводимость полупроводников. Внутренний фотоэффект.
- •46. Принцип роботи напівпровідникового транзистора.
- •47. Контактна різниця потенціалів.
- •48. Явища Заєбека, Пельтьє, Томсона.
27. Співвідношення невизначеностей Гейзенберга
Співвідношення невизначеностей Гейзенберга: добуток невизначеностей значень двох спряжених величин не може бути за порядком величини менше постійної Планка h
![]()
28. Хвильова функція та її властивості. Фізичний зміст.
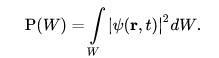 де
|ψ(x)|2 =
ψ*ψ,
а ψ* — функція, комплексно спряжена
з ψ.
де
|ψ(x)|2 =
ψ*ψ,
а ψ* — функція, комплексно спряжена
з ψ.
Властивості:
![]()
В
такому випадку R є модулем функції, а
![]() називають
фазовим множником.
називають
фазовим множником.
Фізичний зміст : Квадрат модуля псі-функції визначає ймовірність того, що частка буде виявлена в межах об'єму dv - фізичний зміст має не сама псі-функція, а квадрат її модуля.
29.Рівняння Шредингера для стаціонарного стану
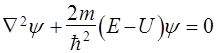
![]() -
набла - оператор Лапласа , Е - повна
енергія частки, постійна у випадку
стаціонарного поля,U - потенційна
функція частки в силовому полі,
-
набла - оператор Лапласа , Е - повна
енергія частки, постійна у випадку
стаціонарного поля,U - потенційна
функція частки в силовому полі,
Є нескінченно багато розв'язків. За допомогою накладення граничних умов відбирають розв'язку, що мають фізичний зміст.
Граничні умови:
хвильові функції повинні бути регулярними, тобто
1) кінцевими;
2) однозначними;
3) безперервними.
Розв'язки, що задовольняють рівнянню Шредингера, називаються власними функціями, а відповідні їм значення енергії - власними значеннями енергії. Сукупність власних значень називається спектром величини. Якщо Еn приймає дискретні значення, то спектр - дискретний, якщо безперервні - суцільний або безперервний.
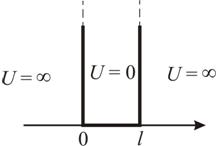
30. Частица в одномерной потенциальной яме.
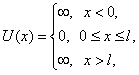
![]()
![]()
Уравнение
Шредингера в пределах ямы (
![]() )
)
![]()
![]()
Общее решение дифференциального уравнения:
![]() .
.
А
если
![]() , то B = 0. Тогда
, то B = 0. Тогда![]()
Уравнение
![]() выполняется только при
выполняется только при![]() , где n – целые числа, т.е. необходимо,
чтобы
, где n – целые числа, т.е. необходимо,
чтобы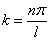
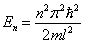 ,
n = 1, 2, 3…
,
n = 1, 2, 3…
Энергия частицы в потенциальной яме является дискретной величиной.
Микрочастица в «потенциальной яме» с бесконечно высокими стенками может находиться только на определенном энергетическом уровне En

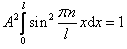 Условие
нормирования пси функции.
Условие
нормирования пси функции.
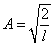

31. Прохождение частицы сквозь потенциальный барьер. Туннельный эффект.
Туннельный эффект - это явление прохождения микрочастицы сквозь потенциальный барьер конечной ширины.

Решение уравнения для 3ох областей
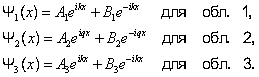
![]()
![]()

Характеристики:
1) Коэффициент прозрачности
2) Коэффициент отражения
Коэффициенты связаны между собой соотношением R + D = 1.
32.
Механический и магнитный моменты
электрона в атоме.
![]() l
– орбитальное квантовое число,
l
= 0, 1, 2, … n-1.
Таким образом, момент импульса электрона
принимает дискретные
значения.
Заметим, что при (l
>>1)
l
– орбитальное квантовое число,
l
= 0, 1, 2, … n-1.
Таким образом, момент импульса электрона
принимает дискретные
значения.
Заметим, что при (l
>>1)
![]() .
.
Проекция
момента импульса электрона на какое-либо
заданное направление в пространстве
z
также квантуется
по правилу:![]() m
=
0, ± 1, ± 2, …± l
–магнитное
квантовое число.
m
=
0, ± 1, ± 2, …± l
–магнитное
квантовое число.
Магнитный момент pm . Очевидно, что он пропорционален механическому моменту импульса L. Отношение магнитного момента pmэлектрона к механическому моменту импульса L называется гиромагнитным
отношением.
Для электрона в атоме водорода ("-" показывает, что вектора
противоположны). Отсюдаорбитальный
магнитный момент
электрона:
("-" показывает, что вектора
противоположны). Отсюдаорбитальный
магнитный момент
электрона: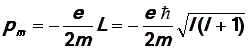
Единица
магнитного момента - это магнетон Бора
(const) mв =
![]()
33. Опыты Штерна и Герлаха. Спин. Спино-орбитальное взаимодействие.
Опыт: пучок атомов Ag пропускали через сильно неоднородное магнитное поле (постоянный магнит). При прохождении атомов через поле на них действовала сила, отклонявшая летящие между магнитами атомы от их первоначального направления движения. Причём, если предположить, что магнитные моменты атомов ориентированы хаотично (непрерывно), то тогда на расположенной далее по направлению движения атомов пластинке должна была проявиться размытая полоса. Однако вместо этого на пластинке образовались две достаточно чёткие узкие полосы, что свидетельствовало в пользу того, что магнитные моменты атомов вдоль выделенного направления принимали лишь два определённых значения, что подтверждало предположение квантово-механической теории о квантовании магнитного момента атомов.
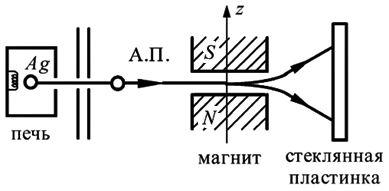
Спин - собственный момент импульса электрона.
Результирующий
полный момент импульса,
![]() в котором
в котором![]()
Так
как спин электрона
![]() ,
то получаем полуцелые значения
,
то получаем полуцелые значения![]()
Спин-орбитальное взаимодействие – взаимодействие магнитного момента электрона с его орбитальным движением, т.е. внешним магнитным полем.
Если
![]() ,
то квантовое число
,
то квантовое число![]() имеет только одно значение, равное
имеет только одно значение, равное![]() .
При
.
При![]() ,
отличном от нуля, возможны два значения
,
отличном от нуля, возможны два значения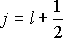 и
и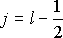 ,
которые соответствуют двум различным
ориентациям спинового момента относительно
орбитального.
,
которые соответствуют двум различным
ориентациям спинового момента относительно
орбитального.
34.Квантові числа. Принцип Паулі. Періодична система елементів Менделєєва. Квантовые числа - энергетические параметры, определяющие состояние электрона и тип атомной орбитали, на которой он находится.
Главное квaнтовое число n определяет общую энергию электрона и степень его удаления от ядра; оно принимает любые целочисленные значения, начиная с 1 (n = 1, 2, 3, . . .)
Орбитальное квантовое число l определяет форму атомной орбитали. Оно может принимать целочисленные значения от 0 до n-1 (l = 0, 1, 2, 3,..., n-1). Каждому значению l соответствует орбиталь особой формы. Орбитали с l = 0 называются s-орбиталями, l =1 - р-орбиталями l = 2 - d-орбиталями l = 3 - f-орбиталями .
Магнитное квантовое число m определяет направление орбитали в пространстве. Его значения изменяются от +l до - l, включая 0. Например, при l = 1 число m принимает 3 значения: +1, 0, -1, поэтому существуют 3 типа р-АО: px, py, pz.
Принцип Паули В одном и том же атоме или двойной квантовой системе не может быть 2-х элементов имеющих одинаковую совокупность квантовых чисел.

Периоди́ческая систе́ма хими́ческих элеме́нтов(табли́ца Менделе́ева) — классификация химических элементов, устанавливающая зависимость различных свойств элементов от их заряда атомного ядра. Система является графическим выражением периодическогозакона, открытого русским учёным-химиком Д. И.Менделеевым в 1869 году.
