
- •Классификация
- •Классификация
- •По направлению и конечному результату
- •По механизму
- •Основные понятия
- •Примеры реагентов
- •Виды π-связи
- •Виды π-связи
- •Правило Хюккеля
- •Электронные эффекты заместителей
- •Электронные эффекты заместителей
- •Э.Д. и Э.А. заместители
- •Примеры влияния Э.Д. и Э.А. заместителей на химические свойства соединений
- •Спасибо за внимание!

Классификация
органических реакций. Сопряжение. Взаимное влияние атомов в молекуле на реакционную способность соединения.
Лекция 11
Лектор: Иванова Надежда Семёновна кандидат химических наук, доцент
1

Классификация
реакций
2

По направлению и конечному результату
Реакции присоединения – А;Реакции замещения – S;
Реакции отщепления – Е (элиминирования);
Реакции перегруппировки; |
|
|
Окислительно-восстановительные |
3 |
|
реакции. |
||
|

По механизму
реакции радикальные - участвуют радикалы (R.), образующиеся за счёт гомолитического типа разрыва связей
Х : У Х. + У.
реакции ионные - участвуют электрофильные и нуклеофильные реагенты, образующиеся за счёт гетеролитического типа разрыва связей
E : N E + + :N– 4

Основные понятия
РАДИКАЛЫ – свободные атомы или |
|
частицы с неспаренным электроном. |
|
ЭЛЕКТРОФИЛЫ – частицы или |
|
фрагменты молекул, содержащие |
|
свободную, доступную орбиталь. |
|
НУКЛЕОФИЛЫ – частицы или |
|
фрагменты молекул, содержащие |
|
подвижную электронную пару на |
|
внешнем электронном уровне. |
5 |
|

Примеры реагентов
R.
.Вr
.NO2
.Cl
.СН3
.С2Н5
SR
Е+
δ+SO3 δ+NO2
Н+ Вr+ Н3С+
AE, SE
N–
H2Oδ– NH3δ–
R2Sδ–
Н– Вr– НО– НS–
AN, SN
6
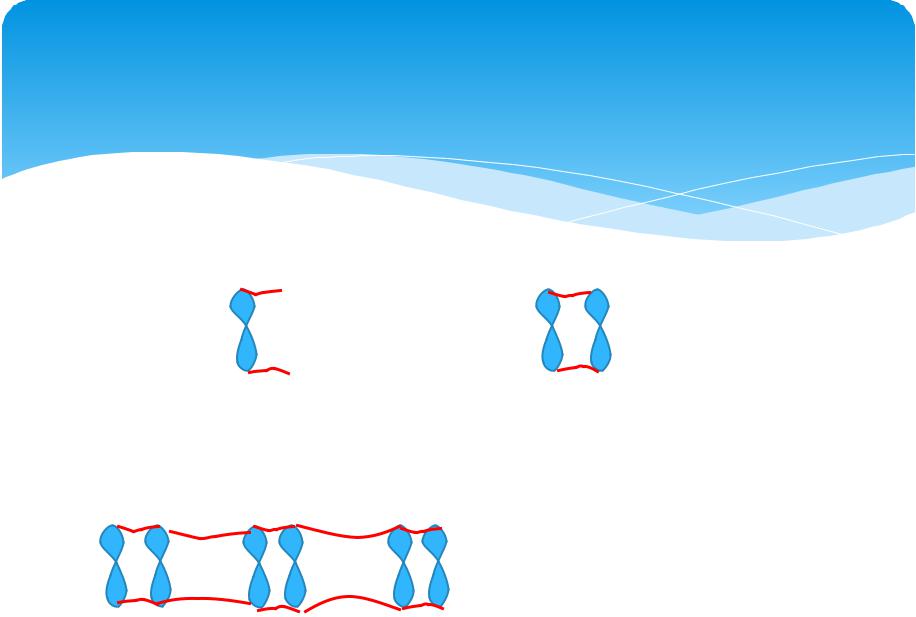
Виды π-связи
А) Локализованная: электроны π- связи поделены между двумя атомами
Н3С—СН  СН—СН2—СН = СН2
СН—СН2—СН = СН2
Б) Делокализованная: электроны π- связи поделены между более чем двумя атомами
С = С—С = С—С = С
7

Виды π-связи
Сопряжение – перераспределение электронной плотности в системе π- связей, приводящее к стабилизации системы
Н2С = СН— Сl – пример р,π- сопряжения
8
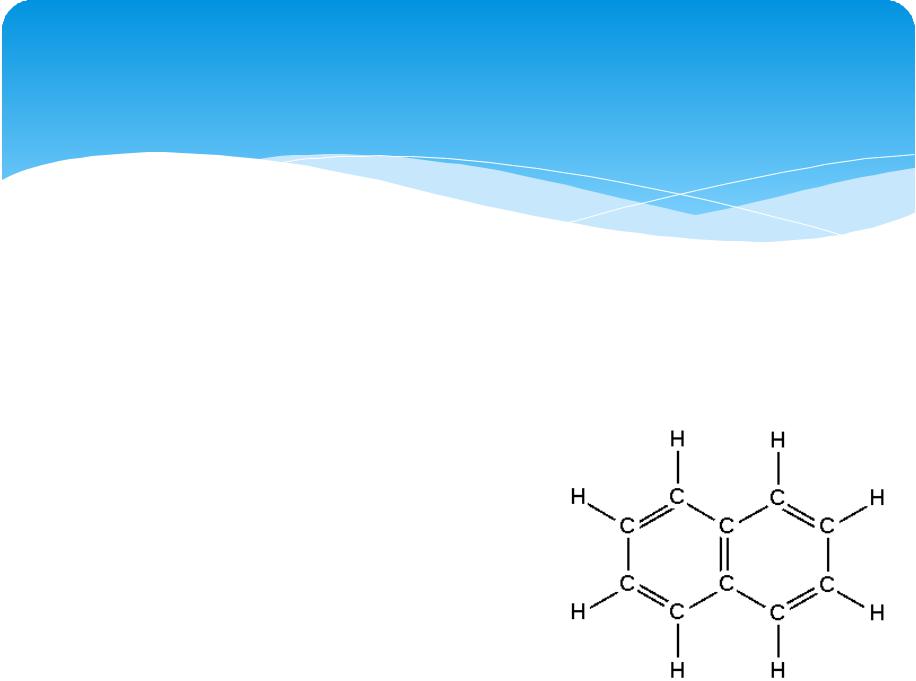
Правило Хюккеля
Выполняется для сопряжённых систем с замкнутой цепью.
Органическое соединение имеет плоский замкнутый цикл (Сsp2, σ-связи в одной плоскости);
р-электроны образуют делокализованнюу π-связь;
Их количество определяется
формулой 4n+2, где n от 0 до ∞
9

Электронные эффекты заместителей
приводят к неравномерному распределению электронной плотности в ОС и возникновению реакционных центров.
Индуктивный эффект – передача электронного влияния заместителей
по цепи σδ-связей:
+
СН3→СН2→СН←СНδ- |
2←СН3 |
NH |
10 |
