
- •Кто спал, когда
- •Протолитическая теория кислот и оснований.
- •Синквейн
- •Основная литература
- •Основная литература
- •Основная литература
- •Основная литература
- •Основная литература
- •Дополнительная
- •Дополнительная
- •Дополнительная
- •Дополнительная
- •Дополнительная
- •Дополнительная
- •Введение
- •Тогда протолитическое равновесие может быть выражено схемой:
- •Типы кислот и оснований Б-Л
- •Типы протолитических реакций
- •Физиологические механизмы поддержания рН крови
- •Физико-химические механизмы поддержания рН крови
- •Буферные системы – …
- •Состав буферных систем
- •Типы буферных систем
- •Расчёт рН буферных систем. Уравнение Гендерсона – Гассельбаха
- •Выводы
- •Механизм действия буферной системы …
- •Механизм действия буферной системы
- •Механизм действия бикарбонатного буфера
- •Основные характеристики буферной системы
- •Факторы, влияющие на β
- •Основные характеристики буферной системы
- •рН биожидкостей в норме
- •Совмещённые протолитические равновесия …
- •Совмещённое протолитическое равновесие
- •Спасибо за внимание!
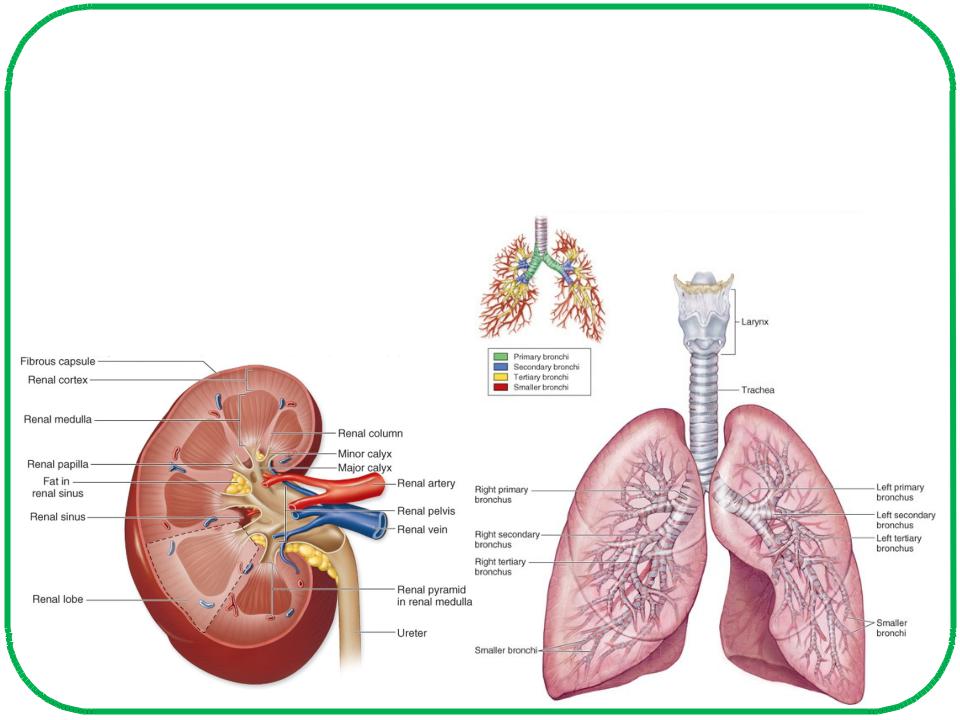
Физиологические механизмы поддержания рН крови
Реагируют на изменение рН через
Реагируют на 10 – 18 часов изменение рН через 2
– 3 суток

Физико-химические механизмы поддержания рН крови
Буферное действие
проявляется практически мгновенно (10 – 15 мин).
Ионный обмен.
эозинофил
нейтрофил |
базофил |
гранулоцит
ы
агранулоци
ты
лимфоцит |
моноцит |

Буферные системы – …
… раствор, содержащий протолитическую равновесную систему, способную поддерживать практически постоянный рН при разбавлении или добавлении небольших количеств кислоты и щёлочи.
… система, состоящая из слабого протолита и избытка сопряжённого с ним основания или кислоты. рН буферных систем незначительно изменяется при добавлении сильного протолита и разбавления.

Состав буферных систем
Из определения в состав буферной системы входит слабый протолит:
НА + Н2О ↔ Н3О+ + А– |
|
кисл |
с. |
Избыток сопряжённого основания (А–) образуется за счёт соли этой кислоты с сильным основанием.
МеА Ме+ + А–
с.
осн

Типы буферных систем
1.кислая буферная система: слабая кислота и её соль с сильным основанием
СН3СООН + СН3СООNa;
2.основная буферная система: слабое основание и его соль с сильной кислотой
NH4OH + NH4Cl.

Расчёт рН буферных систем. Уравнение Гендерсона – Гассельбаха
кислая буферная система
|
1 |
|
|
|
|
|
1 |
|
Vsal |
|
n |
con.bas |
|
c |
|
sal |
|||
pH pKa lg |
z |
|
|
pKa lg |
|
z |
|
|
|
|
1 |
|
|
1 |
|
|
Vacid |
||
|
|
|
|||||||
|
n |
|
acid |
|
c |
|
acid |
||
|
z |
|
|
z |
|
|
|
||
основная буферная система
|
|
1 |
|
|
|
|
|
1 |
|
Vsal |
|
||
|
n |
|
con.acid |
|
c |
|
|
sal |
|
||||
pH 14 pKb lg |
z |
|
|
|
|
14 pKb lg |
z |
|
|
|
|||
|
|
|
|
|
|
|
|||||||
|
|
1 |
|
|
|
1 |
|
|
|
||||
|
|
n |
bas |
|
|
|
c |
|
bas |
Vbas |
|||
|
|
z |
|
|
|
|
z |
|
|
|
|
||

Выводы
Из уравнения очевидно:
1.рН буферной системы определяется Ка или Кb слабого протолита:
рКа = –lgKa pKb = –lgKb
2.рН зависит от соотношения количеств компонентов буферной системы.
3.рН зависит от температуры, т.к. величины рКа и рКb зависят от температуры.

Механизм действия буферной системы …
… и основные свойства буфера (противостоять изменению рН при добавлении сильных протолитов и разбавлению) заключаются в совмещении нескольких протолитических равновесий:
HB + H2O ↔ B‒ + H3O+
кисл |
с.ос |
B‒ + H2O ↔ HB + OH‒ |
|
. |
н |
с.ос |
кисл |
Вывод: в протолитической буферной системе |
|
н |
. |
имеет место совмещённое равновесие процессов ионизации и гидролиза.

Механизм действия буферной системы
При добавлении HCl
СН3СООН
СН3СОО– + Н+ ↔ СН3СООН
HCl заменяется эквивалентным количеством СН3СООН, что приводит к незначительному уменьшению рН буфера.
При добавлении NaOH
СН3СОО–
СН3СООН + OН- ↔ СН3СОО– + H2O
NaOH заменяется эквивалентным количеством СН3СООNa, что приводит к незначительному увеличению рН буфера.
Разбавление буферной системы до концентрации компонентов буфера ≈ 0,01 моль/дм3 практически не
влияет на рН буфера.

