
- •1.Классификация органических соединений. Важнейшие функциональные группы. Примеры.
- •2. Понятие о взаимном влиянии атомов в молекуле, электронные эффекты (положительные и отрицательные индуктивный и мезомерный эффекты).
- •3. Классификация органических реакций (по механизму и по конечному результату). Гомолитический и гетеролитический способы разрыва связей. Электрофильные и нуклеофильные реакции. Примеры.
- •5.Особенности многоатомных спиртов. Биологическая роль этиленгликоля и глицерина.
- •6.Химические свойства фенолов: кислотно-основные, окислительно-восстановительные.
- •7. Карбонильные соединения: альдегиды, кетоны. Строение, классификация. Примеры.
- •8.Тип гибридизации атомных орбиталей карбонильного атома углерода. Распределение электронной плотности в молекулах. Реакционные центры альдегидов и кетонов: электрофильный, основный, сн-кислотный.
- •10.Взаимодействие альдегидов а) со спиртами (образование ацеталей и полуацеталей); б) с водой; в) с аммиаком, аминами (образование иминов-оснований Шиффа); г) с циановодородной кислотой.
- •11. Окислительно-восстановительные свойства альдегидов и кетонов: реакции альдольной и кротоновой конденсации, окисление альдегидов, кетонов, биологическое окисление.
- •14.Образование сложных эфиров, тиоэфиров, амидов, ангидридов, галогенгидридов карбоновых кислот. Ацетилкофермент а in vivo как переносчик ацильных групп на нуклеофильные субстраты.
- •16.Гетерофункциональные органические соединения (кетокислоты, гидроксикислоты, аминокислоты, аминофенолы, аминоспирты. Привести примеры.
- •17. Α-Аминокислоты. Строение, классификация α-Аминокислот по природе радикала: алифатические, ароматические, гетероциклические. Заменимые и незаменимые α-Аминокислоты. Привести примеры.
- •18. Свойства α-Аминокислот. Кислотно-основные свойства. Понятие об изоэлектрической точке (рI).
- •21. Липиды как сложная по составу группа органических веществ. Классификация липидов: химическая и функциональная. Биологическая роль липидов.
- •22. Высшие жирные кислоты (вжк): строение, конфигурация двойных связей, биологическая роль.
- •23. Омыляемые простые липиды: а) воски (спермацет, пчелиный воск); б) жиры, масла. Триаглицерины: общая структура, твердые, жидкие. Примеры. Свойства липидов: гидролиз, реакция
- •24. Омыляемые сложные липиды. Фосфолипиды, классификация. Фосфатидные кислоты. Фосфатидилэтаноламин, фосфатидилхолин, фосфатидилсерины, фосфатидилинозиты, плазмагены.
5.Особенности многоатомных спиртов. Биологическая роль этиленгликоля и глицерина.
Кислотность многоатомных спиртов выше, чем одноатомных, что объясняется наличием в молекуле дополнительных гидроксильных групп, обладающих отрицательным индуктивным эффектом. Поэтому многоатомные спирты, в отличие от одноатомных, реагируют со щелочами, образуя соли. Например, этиленгликоль реагирует не только с щелочными металлами, но и с гидроксидами тяжелых металлов.

При взаимодействии гидроксида меди (II) с глицерином и другими многоатомными спиртами происходит растворение гидроксида и образуется комплексное соединение ярко-синего цвета. В отсутствие щелочи многоатомные спирты не реагируют с |гидроксидом меди (II) — их кислотность для этого недостаточна.
Многоатомные спирты взаимодействуют с кислотами, образуя сложные эфиры При взаимодействии глицерина с азотной кислотой в присутствии концентрированной серной кислоты образуется нитроглицерин (тринитрат глицерина):
![]()
Для спиртов характерны реакции, в результате которых образуются циклические структуры
![]()
Этиленгликоль используется главным образом для производства лавсана и для приготовления антифризов — водных растворов, замерзающих значительно ниже 0°С (использование их для охлаждения двигателей позволяет автомобилям работать в зимнее время).
Глицерин широко используется в кожевенной, текстильной промышленности при отделке кож и тканей и в других областях народного хозяйства. Наиболее важной областью применения глицерина является производство тринитрата глицерина (неверно называемого нитроглицерином) — это сильное взрывчатое вещество, которое взрывается от удара, а также лекарство (сосудорасширяющее средство). Сорбит (шестиатомный спирт) используется как заменитель сахара для больных диабетом.
6.Химические свойства фенолов: кислотно-основные, окислительно-восстановительные.


Окислительно-восстановительные реакции. Реакции этого типа свойственны двухатомным фенолам с орто- и пара-положением гидроксильных групп в бензольном кольце. Среди продуктов окисления таких двухатомных фенолов особый интерес представляют хиноны
![]()
Хиноны содержат своеобразную систему сопряженных связей, называемую хиноидной группировкой, включающую две двойные связи в цикле и двойные связи двух карбонильных групп.
1,2-Бензохинон (о-бензохинон) и 1,4-бензохинон (п-бензохинон) - простейшие представители хинонов, образующиеся при окислении пирокатехина и гидрохинона соответственно. Наиболее важны 1,4-хиноны, обычно называемые просто хинонами.
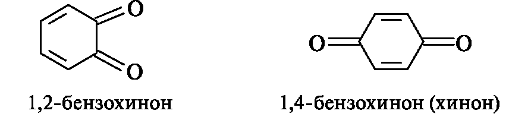
Окисление гидрохинона в хинон in vivo происходит с участием пероксида водорода под действием фермента.
При окислении нафталина образуется 1,4-нафтохинон, являющийся структурным фрагментом витаминов группы K

Хиноны - сильные окислители. Принимая два электрона и два протона, они восстанавливаются в соответствующие гидрохиноны.

Окислительно-восстановительная система хинон-гидрохинон играет важную роль в организме. По отношению к большинству органических субстратов эта система выступает в роли окислителя.
С химической точки зрения производными 1,4-бензохинона являются убихиноны, называемые еще коферментом Q. Функционирование убихинонов в организме основано на их способности легко и обратимо превращаться в восстановленные формы
Структурный фрагмент о-хинона содержится в составе окисленной формы флавоноидов. Пирокатехиновая группировка в структуре
таких важных биологически активных веществ, как флавоноиды, обусловливает их способность к участию в окислительно-восстано- вительных реакциях в организме
