
- •- Этилхлорид из этилового спирта.
- •- Этанол и этилен из этилхлорида.
- •- Пропанол и из соответствующего галогеналкана.
- •- Пропилхлорид из пропанола.
- •- Соответствующие спирты из пропилхлорида и аллилхлорида;
- •- Метилйодида с водным раствором гидроксида натрия.
- •- Этилат натрия с этилйодидом.
- •- Пропилбромид с этоксидом натрия.
- •- Реакции этилирования аммиака.
- •- Этаналь
- •- Пропаналь
- •- Бутаналь
- •- Полный этиловый эфир бутандиовой кислоты из бутандиовой кислоты
- •- Метилацетат
- •- Этиловый эфир пропановой кислоты
- •- N-метиламид уксусной кислоты
- •- Метилбутаноат
1.Напишите уравнения реакций получения:
- этилхлорида из этилового спирта;
- этанола и этилена из этилхлорида;
- пропанола из соответствующего галогеналкана;
- пропилхлорида из пропанола;
- соответствующих спиртов из пропилхлорида и аллилхлорида;
Опишите механизмы реакций. Какие условия необходимы для их проведения?
Решение
- Этилхлорид из этилового спирта.
![]()
Хлористый цинк усиливает H-кислотность хлороводорода, причем в результате образуется более сильная кислота, чемHCl. Кроме того, хлорид цинка образует комплекс со спиртом.

Реакция протекает по механизму бимолекулярного нуклеофильного замещения SN2.
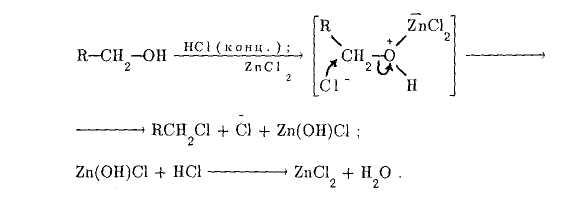
С первичными спиртами хлористоводородная кислота малоактивна, поэтому создают по возможности более высокую концентрацию хлористого водорода, путем насыщения спирта газообразным HClи даже проводят реакцию в запаянной ампуле при повышенной температуре и давлении. Прибавление безводного хлорида цинка повышает реакционную способность, как спирта, так и соляной кислоты. На практике на 1 моль первичного спирта добавляют 2 моль концентрированной соляной кислоты и 2 моль безводного хлорида цинка. Но можно в растворZnCl2в этаноле пропускать сухой газообразныйHClи получать хлористый этил (в виде газа).
- Этанол и этилен из этилхлорида.
В водной щелочи протекает гидролиз алкилгалогенидов. Нуклеофильность и основность гидроксил-иона гораздо выше, чем молекул воды. Кроме этого в щелочной среде одновременно смещается положение равновесия в сторону продуктов омыления, так как обратная реакция невозможна.
![]()
В горячем спиртовомрастворе щелочи протекает реакция элиминирования, приводящая к этилену:
![]()
Гидролиз этилхлорида протекает по механизму бимолекулярного нуклеофильного замещения SN2.
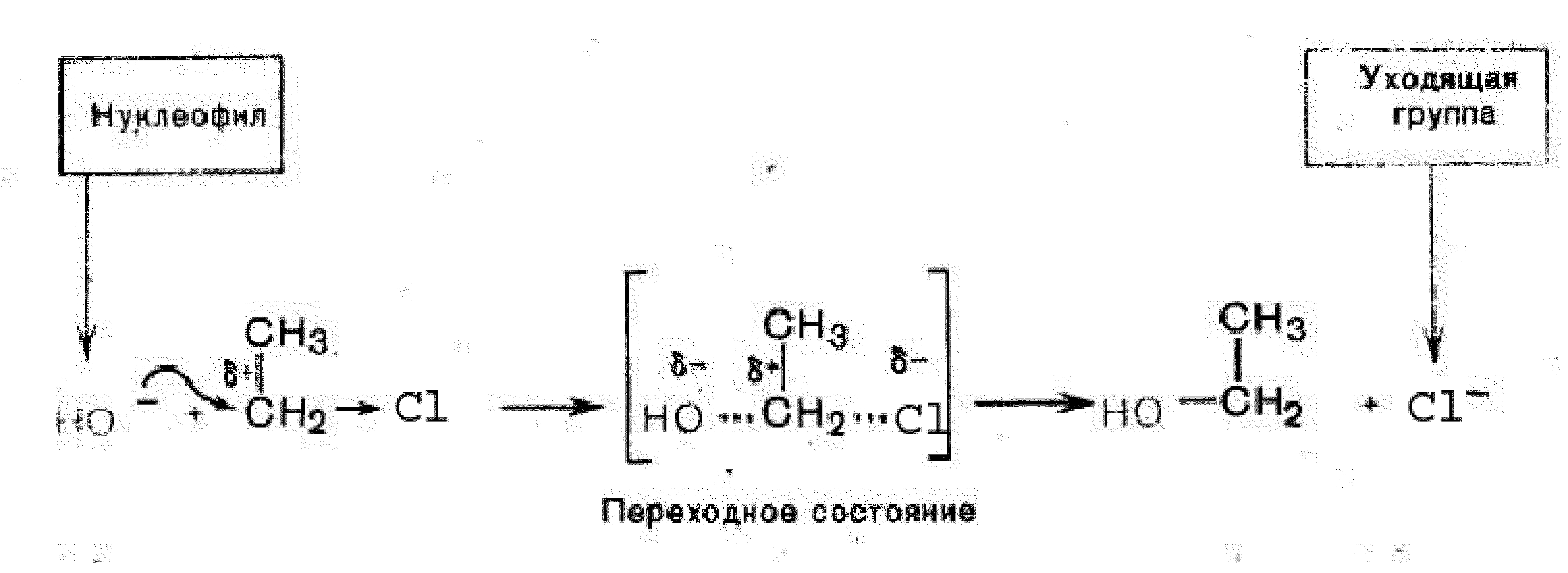
Реакция образования этилена протекает по механизму бимолекулярного элиминирования E2, когда две группы отщепляются одновременно, при этом протон выталкивается основанием:

Реакция происходит в одну стадию и характеризуется кинетикой второго порядка: первым по субстрату и первым по основанию. Она аналогична реакциям, протекающим по механизму SN2, и часто обе эти реакции конкурируют друг с другом.
- Пропанол и из соответствующего галогеналкана.
![]()
Реакцию ведут кипячением алкилгалогенида с водными щелочами или с суспензиями карбонатов щелочноземельных металлов. Гидролиз может протекать только на поверхности раздела фаз, так как алкилгалогениды нерастворимы в воде.
Механизм — бимолекулярное нуклеофильное замещение SN2.
Оба компонента — галогенпроизводное и нуклеофильный реагент — вступают в реакцию одновременно:

В реакциях SN2 происходит обращение конфигурации у атома углерода. Скорость реакции определяется как концентрацией и типом нуклеофильного реагента, так и концентрацией галогенпроизводного.
- Пропилхлорид из пропанола.
![]()
На 1 моль первичного спирта добавляют 2 моль концентрированной соляной кислоты и 2 моль безводного хлорида цинка, реакционную смесь кипятят.
Реакция протекает по механизму бимолекулярного нуклеофильного замещения SN2.

- Соответствующие спирты из пропилхлорида и аллилхлорида;
![]()
Реакцию ведут кипячением алкилгалогенида с водными щелочами или с суспензиями карбонатов щелочноземельных металлов. Гидролиз может протекать только на поверхности раздела фаз, так как алкилгалогениды нерастворимы в воде.
Механизм — бимолекулярное нуклеофильное замещение SN2, приведен выше.
![]()
Аллилхлорид является очень активным субстратом, поэтому легко может быть гидролизован водой. Часто используют растворы или суспензии карбонатов или слабые растворы щелочей.
Высокая реакционная способность алллильного галогена связана с большой устойчивостью (благодаря сопряжению) карбониевого иона, возникающего при диссоциации галогенпроизводного.
Реакция протекает в две стадии по мономолекулярному механизму SN1.
Первая стадия — ионизация галогенпроизводного — является медленной стадией. В результате ионизации могут образоваться ионные пары (тесные или сольваторазделенные):
![]()
Вторая стадия — взаимодействие с нуклеофильным реагентом протекает быстро:
![]()
Общую скорость реакции SN1 лимитирует медленная стадия — ионизация. Поэтому скорость реакции не зависит от концентрации и типа нуклеофильного реагента.
2.Напишите уравнения реакций взаимодействия:
- метилйодида с водным раствором гидроксида натрия;
- этилата натрия с этилйодидом;
- пропилбромида с этоксидом натрия;
- реакции этилирования аммиака;
Опишите механизмы реакций. К какому классу органических соединений относятся полученные вещества?
Решение
