
- •Химия элементов.d- элементы I –II групп
- •d- элементы I группы
- •Степень
- •Соединения Cu (I), Ag (I), Au (I)
- •Соединения Ag (I) проявляют основные свойства
- •Соединения Au (I)
- •Соединения Cu (II)
- •Медь
- •При болезни Вильсона содержание меди увеличивается практически в 100 раз по сравнению с
- •d- элементы II группы
- •Cвойства Zn, Cd
- •Свойства Hg
- •Цинк




 Химия элементов.
Химия элементов.





 d- элементы I –II групп
d- элементы I –II групп 

Лекция №17
d- элементы I группы
3d104s14p0
4d105s15p0
5d106s16p0
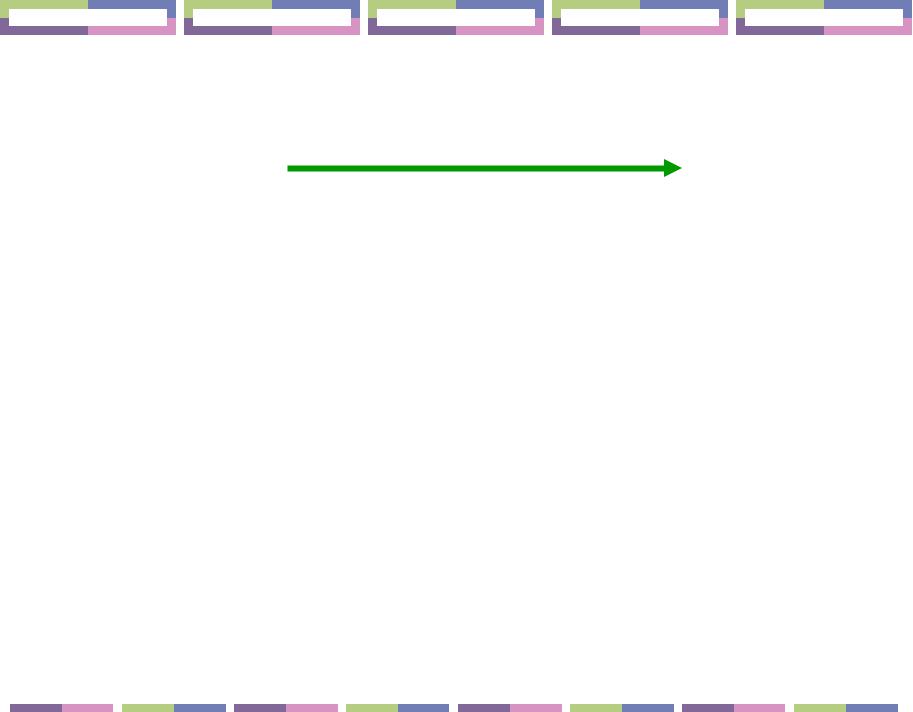
Cu Ag Au
активность уменьшается
2Cu O2 2CuO
4Cu O2 2Cu2O
4Ag 4O3 Ag2O Ag2O3 4O2
Cu S Cu2S Ag S Ag2S
Взаимодействуют с галогенами
|
|
Cu |
|
|
Ag |
Cu + Hal |
2 |
CuHal (Cl |
,Br ,F ) |
Ag + Hal2 Ag2Hal |
|
|
2 |
2 |
2 |
|
|
Cu + I2 Cu2l
Au
Au + Hal2 AuHal
2Au + I2 2KI 2K[Au2l]

2Cu + O2 + CO2 + H2O (CuOH)2 CO3
4Ag + O2 + 2H2S 2Ag2S + 2H2O
Взаимодействие с кислотами
2Cu + O2 + 2H2SO4(p) 2CuSO4 + 2H2O 2Cu + 2H2SO4(k) CuSO4 + SO2 + 2H2O
3Cu + 8HNO3(p) 3Cu(NO3 )3 + 2NO + 4H2O Cu + 4HNO3(k) 3Cu(NO3 )3 + 2NO2 + 2H2O
2Ag + 2H2SO4(k) Ag2SO4 + SO2 + 2H2O 3Ag + 4HNO3(p) 3AgNO3 + NO + 2H2O

Степень |
Координаци |
Электронная |
Примеры соединений |
окислени |
онное число |
конфигураци |
|
я |
|
я |
|
+1 |
2 |
d10 |
Cu2O, Ag2O, AgCN - линейная |
+2 |
3 |
|
K[Cu(CN)2] – плоская треугольная |
|
4 |
d9 |
CuHal – тетраэдрическая, CuО |
|
|
|
-квадратная |
|
6 |
|
AgHal - октаэдрическая |
+3 |
4 |
d8 |
AuHal3, KCuO2 - квадратная |

Соединения Cu (I), Ag (I), Au (I)
Соединения Cu(I) проявляют основные свойства
Cu2O + 2HCl 2CuCl + H2O
Cu2S + As2S3 2Cu[AsS2 ]
Cu2O + 6HNO3 2Cu(NO3 )2 + 2NO2 + 3H2O
окислитель
Cu2O + H2 2Cu + H2O
восстановитель
Cu2O + H2SO4 2CuSO4 + Cu + H2O
Соединения Ag (I) проявляют основные свойства
Ag2O + 2HClO4 2AgClO4 + H2O
Ag2O + CO2 Ag2CO3
Окислительные свойства соединений серебра (I)
2K[Ag(CN)2 ]+ Zn K2[Zn(CN)4 ]+ Ag
2[Ag(NH3 )2 ]OH + RCH = O 2Ag + NH4 RCOO + 3NH3 + H2O
Восстановительные свойства соединений серебра (I)
4Ag + 4O3 Ag2O× Ag 2O 3 + 4O 2

Соединения Au (I)
AuCl, AuCN, Au2S
3AuCl + H2O H[AuCl3OH]+ 2Au
2K[Au(CN)2 ]+ Zn K2[Zn(CN)4 ]+ 2Au

Соединения Cu (II)
CuO + 2HBr CuBr2 + H2O
CuO + Na2O Na2CuO2 |
Кислотно-основные |
|
|
|
свойства |
Cu(OH)2 |
2HBr CuBr2 + 2H2O |
|
Cu(OH)2 |
+ KOH K2[Cu(OH)4] |
|
Окислительные свойства соединений меди (II)
2Cu2+ + 4I- 2CuI + I2
2Cu(OH)2 + RCH = O + OH Cu2O + RCOO + H2O

|
Соединения Аu (III) |
|
- амфотерные соединения |
AuHal3 , |
с преобладанием кислотных |
Au2O3 , Au (OH )3 признаков |
|
2NaOH Au2O3 3H2O 2Na[Au(OH )4 ] |
|
Au2O3 8HNO3 |
2H[Au(NO3 )4 ] 3H2O |
