
- •2. Трансаминирование аминокислот: химизм, значение. Характери-стика трансаминаз. Непрямое дезаминирование аминокислот.
- •3. Окислительное дезаминирование аминокислот: химизм, характери-стика ферментов. Восстановительное аминирование альфакетоглу-тарата, значение.
- •4. Декарбоксилирование аминокислот. Образование биогенных ами-нов, их роль в регуляции метаболизма и функции.
- •6.Трансметилирование. Метионин и s-аденозилметионин (участие в синтезе креатина, адреналина, фосфатидилхолина, метилировании чужеродных соединений). Участие тетрагидрофолиевой кислоты в метилировании.
- •10. Активация и окисление высших жирных кислот: химизм, энергети-ка, физиологическая роль.
- •2. Окисление глицерина
- •11. Биосинтез и использование кетоновых тел.
- •Реакции 3 этапа
- •13. Биосинтез триацилглицеринов, лицерофосфолипидов.
- •14. Обмен и функции холестерина. Прямой и обратный транспорт хо-лестерина. Биосинтез холестерина: химизм, регуляция.
4. Декарбоксилирование аминокислот. Образование биогенных ами-нов, их роль в регуляции метаболизма и функции.
Декарбоксилирование - Превращения аминокислот по карбоксильной группе.
В тканях животных процесс декарбоксилирования аминокислот протекает под действием декарбоксилаз с образованием аминов.

Декарбоксилазы аминокислот – сложные ферменты, коферментом которых является пиридоксальфосфат. Обнаружены процессы декарбоксилирования гистидина, триптофана, 5-гидрокситриптофана, тирозина, глутаминовой, аспарагиновой, цистеиновой кислот с образованием соответствующего амина: гистамина, триптамина, серотонина, тирамина, γ-аминомасляной кислоты, β-аланина, таурина. Их называют биогенными аминами, так как в малых дозах это биологически активные вещества с мощным фармакологическим действием, в больших дозах – фармакологические яды. Декарбоксилазы ароматических аминокислот, гистидина, глютаминовой кислоты и других не отличаются строгой специфичностью. Ферменты мало активны, и процесс протекает с малой скоростью.
При декарбоксилировании тирозина образуется тирамин, проявляющий сосудосуживающее действие.

Н2N - CН - COOH
тирозин тирамин
Декарбоксилирование триптофана сопровождается образованием триптамина, также обладающего сосудосуживающим действием.

триптофан триптамин
При декарбоксилировании производного триптофана - 5- гидрокситриптофана образуется 5- гидрокситриптамин или серотонин.

5-гидрокситриптофан серотонин
Серотонин преимущественно образуется в нервной ткани и кишечнике. Обладает сильным сосудосуживающим действием, является нервным медиатором, поддерживает нормальную психическую деятельность, участвует в центральной регуляции артериального действия, температуры тела, дыхания, в почечной фильтрации, способствует развитию аллергической реакции, токсикоза беременности.
Декарбоксилирование гистидина приводит к образованию гистамина.
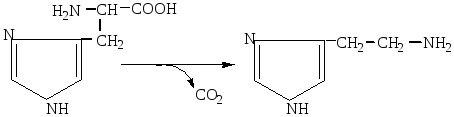
гистидин гистамин
Декарбоксилирование гистидина гистидиндекарбоксилазой происходит главным образом в тучных клетках, которые имеются в соединительной ткани (практически во всех органах). Гистамин накапливается и хранится в этих клетках в соединении с белками в специальных секреторных гранулах и может освобождаться и выделяться в кровь при разнообразных механических воздействиях (травма, ожог, электрическое раздражение), действии эндогенных веществ.
Физиологическое действие гистамина на сосуды отличается от действия других биогенных аминов: он расширяет сосуды и поэтому снижает кровяное давление. В большом количестве гистамин образуется в месте травмы, в очаге воспалительного процесса, вызывает расширение сосудов, повышает проницаемость капилляров, способствует выходу лейкоцитов, развитию воспалительной реакции. Является медиатором нервных процессов, медиатором боли. Укусы насекомых (комары, клопы, осы и др.) вызывают зуд, боль, отечность, что связано с выделением гистамина. Гистамин стимулирует секрецию желудочного сока и слюны (поэтому его используют в клинике при исследовании секреторной функции желудка - гистаминовый завтрак). Если слизистая желудка на введение гистамина не усиливает секрецию сока, то это свидетельствует о повреждении секреторных клеток - атрофическом гастрите. Гистамин сокращает гладкие мышцы легких, что проявляется приступом удушья. Гистамин способствует сенсибилизации организма и развитию аллергических реакций.
Обезвреживание гистамина происходит путем его метилирования с образованием 1-метилгистамина, который выводится с мочой.
При α-декарбоксилировании глутаминовой кислоты образуется γ-аминомасляная кислота.

глутаминовая γ- аминомасляная кислота
кислота (ГАМК)
ГАМК в большом количестве содержится в сером веществе мозга, в то время как в белом веществе мозга и периферической нервной системе ее почти нет. Является тормозным фактором в нервных клетках. В опытах с изолированной петлей кишечника показано, что ГАМК вызывает прекращение перистальтики даже в присутствии ацетилхолина, стимулирующего перистальтику. Используется в клинике при лечении заболеваний центральной нервной системы, связанных с резким возбуждением коры головного мозга (эпилепсия).
Цистеин окисляется в цистеиновую кислоту, которая в тканях животных декарбоксилируется с большой скоростью с образованием таурина.
![]()
цистеин цистеин-диокси- цистеиновая таурин
геназа кислота
Таурин используется в реакциях конъюгации с желчными кислотами для увеличения их гидрофильности. Непосредственное декарбоксилирование цистеина, протекающее в организме с небольшой скоростью, сопровождается образованием цистеамина.
![]()
цистеин цистеамин
Цистеамин оказывает защитное действие при лучевой болезни, однако его действие является непродолжительным, поэтому были синтезированы его производные, аналоги, которые нашли применение в терапии лучевых поражений.
В животных тканях с большой скоростью протекает декарбоксилирование 3,4-диоксифенилаланина - производного фенилаланина. При этом образуется ДОФ-амин, оказывающий мощное сосудосуживающее действие. ДОФ-амин является промежуточным продуктом в синтезе катехоламинов норадреналина и адреналина.
 H2N
- CH- COOH H2N
- CН
- COOH H2N
- CН-COOH
CH2NH2
H2N
- CH- COOH H2N
- CН
- COOH H2N
- CН-COOH
CH2NH2
фенилаланин тирозин 3,4-диоксифенилаланин ДОФ-амин
Под действием декарбоксилаз из диаминокарбоновых кислот образуются диамины: из орнитина – путресцин, лизина – кадаверин.
2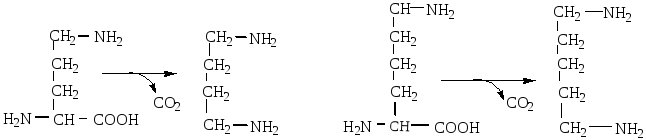
орнитин путресцин лизин кадаверин
Путресцин является предшественником полиаминов – спермина и спермидина. Последние несут большой положительный заряд и легко ассоциируются с ДНК и РНК, стабилизируют структуру ДНК, стимулируют синтез ДНК и РНК, влияют на процессы пролиферации. В сутки в организме взрослого человека образуется около 0,5 ммоль спермина. Фармакологические дозы полиаминов вызывают понижение температуры и артериального давления. Кроме этого они способны ингибировать ферменты.
Таким образом, биогенные амины, являясь сильными фармакологически активными веществами, влияют на различные функции организма. Знание их физиологического действия, механизмов их образования и обезвреживания является важным для врачей, так как их накопление может привести к ряду серьезных нарушений.
Обезвреживание аминов происходит под действием ферментов моноаминоксидаз (МАО) и диаминооксидаз (ДАО). Это сложные ферменты, локализованы в митохондриях. Простетическая группа МАО – ФАД, ДАО – пиридоксальфосфат и медь.
Амины подвергаются окислительному дезаминированию:


 R
R
R
R
R
R
+ФАД +H2O



 CH2NH2
CH=
NH
C=
0+ NH3
CH2NH2
CH=
NH
C=
0+ NH3
 ФАД•Н2
ИМИН Н
ФАД•Н2
ИМИН Н
+О2
ФАД + Н2О2
Образовавшиеся альдегиды далее окисляются в жирные кислоты, которые окисляются до конечных продуктов.
В клинике широко используются антигистаминные препараты: димедрол, пипольфен, тавегил, супрастин, бикарфен, диазолин, кетотифен, зиртек, гисманал, терфенадин.
Также используются фармпрепараты, ингибирующие моноаминооксидазы: ипрониазид, ниаламид, пиразидол, сиднофен, индопан, гармин, паргилин. Все они активные антидепрессанты и используются для лечения депрессивных состояний.
5. ИСТОЧНИКИ И ПУТИ ОБЕЗВРЕЖИВАНИЯ АММИАКА В ОРГАНИЗМЕ: МЕСТНЫЕ И ОБЩИЕ. ГИПЕРАММОНИЕМИЯ. ОСТАТОЧНЫЙ АЗОТ.
Обезвреживание аммиака в организме
Различают механизмы местного и общего обезвреживания аммиака. Местное обезвреживание сводится к временному связыва-нию аммиака с образованием его транспортных форм,в составе ко-торых он доставляется к органам, где происходит общее обезврежи-вание. Последнее заключается в образовании инертных,ненужных организму соединений, которые выводятся с мочой.
Местное обезвреживание аммиака
Осуществляется в тканях(мозг, мышцы, сетчатка и др.), где происходит непосредственное образование NН3, по нескольким ме-ханизмам.
1. Главным путем обезвреживания аммиака является его связы-вание с глутаминовой (у животных) и аспарагиновой (больше у рас-тений) кислотами, т.е. их амидирование. Протекает в мышечной ткани,
мозгу, печени, почках с затратой АТФ.Катализируется глута-минсинтетазой, локализованной в ЭПС.
Образовавшиеся глутамин и аспарагин являются главными транспортными формами аммиака, в виде которых он доставляется в печень и почки, где происходит общее обезвреживание.
Глутамин и аспарагин являются и главными резервными фор-мами аммиака.
O
|
COOH |
|
|
|
|
|
|
|
|
|
|
| |||||||||||||||
|
+ NН3 |
+ АТФ |
C |
|
|
NH2 |
| ||||||||||||||||||||
|
|
|
|
|
|
| |||||||||||||||||||||
|
|
|
|
|
| ||||||||||||||||||||||
|
|
|
|
|
|
|
|
| |||||||||||||||||||
|
|
CH2 |
|
|
|
|
|
|
|
|
| ||||||||||||||||
|
|
|
|
CH2 |
| ||||||||||||||||||||||
|
|
|
|
|
|
| |||||||||||||||||||||
|
|
CH2 |
|
|
|
|
CH2 + АДФ + Н3РО4 |
| |||||||||||||||||||
|
|
CH |
|
NH2 |
|
|
|
CH |
|
|
NH2 |
| |||||||||||||||
|
|
|
|
|
|
|
|
| |||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
| ||||||||||||||
|
|
COOH |
|
|
|
|
COOH |
| |||||||||||||||||||
|
|
ГЛУ |
|
|
ГЛН |
| |||||||||||||||||||||




![]()
Обезвреживание аммиака в тканях происходит также путем амидирования остатков глутаминовой и аспарагиновой кислот в бел-ках.
Восстановительное аминирование (ретрансаминирование) a-кетоглутарата. В мышечной ткани этот процесс приводит к образованию еще одной транспортной формы аммиака. Аммиак связывается с кетоглутаровой кислотой под действием глутаматдегидрогеназы. Образуется глутамат:
НАДФ×Н + Н+ ® НАДФ
NН3 + a-кг глутаматдегидрогеназа ГЛУ
![]()
Глутаминовая кислота вступает в переаминирование с пируватом, образующимся при интенсивной мышечной работе в результате распада гликогена или глюкозы.Образующийся аланин является
транспортной формой аммиака, доставляемой кровью в печень, где он вступает в переаминирование aс-кетоглутаратом, в результате чего получаются
пируват и глутамат. Глутаминовая кислота через аспартат включает свою NН2-группу в мочевину. Пируват используется в глюконеогенезе для синтеза глюкозы, которая поставляется печенью мышцам. Этот ме-ханизм имеет важной значение для выведения аммиака из мышечной ткани и получил название глюкозо-аланинового цикла.
Общее обезвреживание аммиака
Происходит в печени и почках, где образуются инертные соединения, которые выводятся с мочой. В печени синтезируется мочевина, в почках – аммонийные соли.
Синтез мочевины
Синтез мочевины представляет собой циклический процесс, открытый Г.Кребсом в 1932 году. В печень с кровотоком поступают транспортные формы аммиака глутамин и аланин, и ,по воротной вене аммиак, всосавшийся в кишечнике. Глутамин под действием глутаминазы распадается на глутаминовую кислоту и аммиак.
В митохондриях гепатоцитов из аммиака, СО2 с затратой АТФ под действием карбамоилфосфатсинтетазы (1) синтезируется карба-моилфосфат.
O

 NH3+CO2+2АТФ+Н2О
®H2N
C O ~ PO3H2+2АДФ+Н3РО4
NH3+CO2+2АТФ+Н2О
®H2N
C O ~ PO3H2+2АДФ+Н3РО4

 карбамоилфосфат
карбамоилфосфат
Карбамоилфосфат взаимодействует с орнитином при участии орнитинкарбамоилтрансферазы (2) с образованием цитруллина.
|
|
|
O |
|
|
|
NH |
|
|
NH2 |
|
|
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
(2) |
C |
|
|
|
O |
|
|
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
H2N |
|
C |
|
|
|
O ~ PO3H2 + |
CH2 |
|
|
|
|
|
|
|
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
NH |
|
|
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(CH2)3 |
|
|
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HC |
|
|
|
|
NH2 |
HC |
|
|
|
|
|
|
NH2 |
|
|
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
COOH |
|
|
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
орнитин |
|
|
|
|
|
|
|
|
|
|
|
|
|
цитруллин |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
NH |
|
|
|
|
|
|
|
|
|
|
|
NH |
COOH |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
C |
|
|
OH |
|
|
|
COOH |
C |
HN |
|
CH |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2N |
|
|
|
+ АТФ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
NH |
|
|
CH |
|
NH |
|
CH |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
(3) |
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH (4) |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
(CH2)3 |
|
|
|
|
|
(CH2)3 |
|
|
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
COOH |
|
|
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
HC |
|
|
|
|
NH2 |
|
|
|
|
HC |
|
|
NH2 |
|
|
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
АСП |
АМФ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
COOH |
|
|
|
+Н4Р2О7 |
COOH |
|
|
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||







 ¯+Н2О
аргининсукцинат
¯+Н2О
аргининсукцинат![]()
![]()
![]()
2Н3РО4
Цитруллин вступает в конденсацию с аспарагиновой кислотой под действием аргининсукцинатсинтетазы (3) с затратой АТФ. Об-разуется аргининянтарная кислота, которая аргининсукцинатлиазой
(4) расщепляется на аргинин и фумаровую кислоту.
Аргинин расщепляется аргиназой (5) на орнитин и мочевину, которая простой диффузией выходит из клеток в кровь и выделяется с мочой. В сутки в норме выделяется от 20 до 40г мочевины.
Фумаровая кислота является промежуточным продуктом цикла трикарбоновых кислот и фумаратгидратазой превращается в малат, который окисляется малатдегидрогеназой в щавелевоуксусную –кислоту.
. Оксалацетат вступает в реакцию переаминирования с глута-миновой кислотой и превращается в аспарагиновую,которая вновь используется в синтезе мочевины. Образовавшийся из глутамата α-кетоглутарат вступает в реакцию переаминирования с любыми ами-нокислотами печени.
NH2
CNH COOH
NH + CH
(CH2)3 CH
HC NH2 COOH COOH фумарат аргинин
+ Н2О¯ (5)
NH2
NH2 (CH2)3 + C O
|
HC |
|
NH2 |
NH2 |
| |||
|
|
| ||||||
|
|
|
|
|
| |||
|
COOH |
| ||||||
|
|
| ||||||
Процесс синтеза мочевины– циклический и требует орнитина и затраты АТФ.
Синтез аммонийных солей
Глутамин, доставляемый кровотоком в почки,расщепляется глутаминазой, активируемой протонами и самим глутамином,на глутаминовую кислоту и аммиак. Аммиак взаимодействует с прото-нами, образуя ион аммония, который соединяется с анионами раз-личных кислот: фосфорной, серной, угольной, соляной, щавелевой, мочевой.
NН3 + Н+ → NН4+
Образуются соли аммония– фосфаты, сульфаты, карбонаты, хлориды, оксалаты, ураты, которые выводятся с мочой. Всего в сутки у здорового человека выделяется 1-1,2 г таких солей.
Процесс имеет важное значение, т.к. является не только меха-низмом общего обезвреживания аммиака, но участвует в поддержа-нии кислотно-щелочного равновесия в организме, а также сберегает от выведения с мочой катионы натрия и калия.
