
- •Теория метода измерений и описание установки
- •Порядок выполнения работы
- •Контрольные вопросы.
- •Лабораторная работа 2 Определение коэффициента вязкости жидкости по методу Стокса
- •Теоретическое введение
- •Теория метода измерений и описание установки
- •Порядок выполнения работы
- •Теория метода измерений и описание установки
- •Порядок выполнения работы
- •Теория метода измерений
- •Теория метода измерений и описание установки
- •Порядок выполнения работы
- •Контрольные вопросы
- •Лабораторная работа 5 Определение универсальной газовой постоянной
- •Теоретическое введение
- •Теория метода измерений и описание установки
- •Порядок выполнения работы
- •Теория метода измерения и описание установки
- •Порядок выполнения работы
- •Контрольные вопросы
- •Лабораторная работа 7 Определение удельной теплоты плавления твердых тел
- •Теоретическое введение
- •Описание метода измерений и установки
- •Порядок выполнения работы
- •Описание метода измерений и установки
- •Порядок выполения работы
- •Контрольные вопросы
Лабораторная работа 7 Определение удельной теплоты плавления твердых тел
Цель работы: определение удельной теплоты плавления олова по скорости охлаждения.
Необходимые приборы и принадлежности: электроплитка, фарфоровый тигель с оловом, термометр, штатив, технические весы.
Теоретическое введение
Плавлением твердых тел называется их переход из твердого состояния в жидкое. За счет энергии, которая подводится к твердому телу при плавлении, амплитуды смещений частиц, колеблющихся в узлах кристаллической решетки, возрастают, становятся сравнимыми с периодом кристаллической решетки. Плавление происходит при определенной температуре, называемой температурой плавления - Тпл. У большинства твердых тел плавление сопровождается увеличением их удельного объема. Температура плавления возрастает с увеличением внешнего давления, так как давление препятствует увеличению равновесных состояний между частицами в кристаллической решетке необходимому для начала плавления тела и затрудняет процесс ее разрушения. Исключение составляют лед и висмут, у этих тел возрастание внешнего давления приводит к уменьшению температуры плавления. В процессе плавления твердого тела, вещество существует одновременно в твердом и в жидком состояниях. Все количество теплоты, подводимое твердому телу при температуре плавления, расходуется на разрушение кристаллической решетки (это означает, что, для того чтобы высвободить молекулы из их относительно жестко фиксированных положений в твердом состоянии, нужно совершить работу против действующих между молекулами сил притяжения) и на работу против внешних сил. При этой температуре энергии молекул становится достаточным для отрыва от оседлого состояния на узлах кристаллической решетки и молекула начинает совершать поступательное движение за счет в дальнейшем подводимой теплоты. Для превращения вещества из жидкого состояния в твердое необходимо только охлаждение, т.е. отвод от вещества некоторого количества теплоты. Переход вещества из жидкого в твердое состояние означает не столько сближение молекул, сколько дальнейшее связывание их между собой, ограничение свободы их теплового движение в пределах объема вещества.
Известны два различных процесса перехода вещества из состояния в твердое: 1. Затвердевание вследствии кристаллизации вещества. В этом случае в жидкости сначала появляются мельчайшие кристаллики, содержащие небольшое число молекул, правильно расположенных друг относительно друга и прочно связанных между собой. Затем по мере отвода тепла, эти кристаллики начинают расти за счет прилипающих к ним молекул жидкой фазы до полного исчезновения этой фазы. 2. Затвердевание вследствии постепенного увеличения вязкости жидкости. При этом у некоторых веществ кристаллизация совсем не происходит. Такие вещества называются аморфными: к ним относятся воск, сургуч, смолы, стекло, дерево и т.д.
Особенностью аморфных тел является отсутствие у них определенной точки плавления, другими словами невозможно указать определенную температуру, выше которой можно было бы констатировать жидкое состояние, а ниже- твердое. У других веществ ( способных к кристаллизации), от быстрого и сильного возрастания вязкости при охлаждении затвердевание наступает до кристаллизации; процесс кристаллизации весьма медленно может

происходить после затвердевания. Различие между указанными выше процессами затвердевания обнаруживается если вычертить кривую , изменения температуры со временем ( рис. 1).
У
кристаллических тел температура
уменьшается по кривой
в направлении
 .
На участке 1-2 одновременно существуют
обе фазы-
жидкая и твердая. Как только процесс
кристаллизации заканчивается ( точка
2), дальнейший отвод теплоты сопровождается
понижением температуры образовавшегося
твердого тела. Постоянство температуры
при кристаллизации объясняется
образованием и ростом кристаллов,
которые возможны если от молекул жидкости
отнимается некоторое количество энергии.
В кристалле жестко связанная молекула
совершает только колебательное движение,
тогда как при той же температуре в
жидкости молекула совершает еще и
поступательное движение. Поэтому при
кристаллизации от вещества необходимо
отвести теплоту соответствующую
поступательному движению молекул.
.
На участке 1-2 одновременно существуют
обе фазы-
жидкая и твердая. Как только процесс
кристаллизации заканчивается ( точка
2), дальнейший отвод теплоты сопровождается
понижением температуры образовавшегося
твердого тела. Постоянство температуры
при кристаллизации объясняется
образованием и ростом кристаллов,
которые возможны если от молекул жидкости
отнимается некоторое количество энергии.
В кристалле жестко связанная молекула
совершает только колебательное движение,
тогда как при той же температуре в
жидкости молекула совершает еще и
поступательное движение. Поэтому при
кристаллизации от вещества необходимо
отвести теплоту соответствующую
поступательному движению молекул.
При
нагревании кристаллических тел процесс
протекает в обратном направлении
 В точке 2 достигается такая температура
В точке 2 достигается такая температура
 - температура
плавления,
при которой становится возможным отрыв
молекул от поверхности нагревших
кристаллов. В дальнейшем вся подводимая
теплота передается отрывающимся
молекулам. Эти молекулы получив
дополнительную энергию, могут при той
же температуре совершать уже не только
колебательное, но еще и поступательное
движение в пределах объема вещества.
Так постепенно образуется жидкая фаза
за счет разрушения твердой фазы.
- температура
плавления,
при которой становится возможным отрыв
молекул от поверхности нагревших
кристаллов. В дальнейшем вся подводимая
теплота передается отрывающимся
молекулам. Эти молекулы получив
дополнительную энергию, могут при той
же температуре совершать уже не только
колебательное, но еще и поступательное
движение в пределах объема вещества.
Так постепенно образуется жидкая фаза
за счет разрушения твердой фазы.
Согласно
первому закону термодинамики

где
 –
количество теплоты переданное системе;
–
количество теплоты переданное системе;
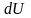 -
изменение внутренней энергии системы;
-
работа, совершаемая системой. Плавление
начинается тогда, когда внутренняя
энергия тела в твердом состоянии
сравнивается с внутренней энергией
этого тела в жидком состоянии, т.е. когда
-
изменение внутренней энергии системы;
-
работа, совершаемая системой. Плавление
начинается тогда, когда внутренняя
энергия тела в твердом состоянии
сравнивается с внутренней энергией
этого тела в жидком состоянии, т.е. когда
 ,
,
 .
Следовательно,
.
Следовательно,
 т.к. вся теплота сообщаемая телу
расходуется на разрушение твердой фазы.
т.к. вся теплота сообщаемая телу
расходуется на разрушение твердой фазы.
Известно,
что изменение внутренней энергии во
всех процессах определяется по формуле:

где
-
масса вещества;
-
удельная теплоемкость при постоянном
объеме. Если в данной формуле
,
то
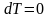 ,
т.е.
,
т.е.
 .
Это значит, что пока плавится тело его
температура не изменяется. Эта постоянная
температура при которой плавится твердое
тело, называется температурой
или точкой плавления.
.
Это значит, что пока плавится тело его
температура не изменяется. Эта постоянная
температура при которой плавится твердое
тело, называется температурой
или точкой плавления.
Точка плавления есть лишь у кристаллических твердых тел, а у аморфных тел такой точки нет, есть точка перегиба ( рис. 1 в). Это объясняется тем, что по структуре амофорное тело не отличается от жидкости ( в аморфном теле в отличии от жидкости, частицы не движутся поступательно, хотя расположены так же, как и в жидкости).
Кроме точки плавления, у каждого кристалла есть еще одна характерная физическая величина, так называемая теплота плавления. Эту физическую величину определяют для единицы массы тела и называют удельной теплотой плавления λ.
Удельная теплота плавления равна скрытой теплоте, которую нужно сообщить телу при температуре плавления, чтобы его единицу массы превратить в жидкость:
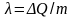 (1)
(1)
-
называют
скрытой теплотой плавления,
потому, что ее нельзя измерить явно, как
 ,
ибо
,
ибо
 .
Для ее измерения существует калориметрический
метод. В системе
удельная
теплота плавления измеряется в
.
Для ее измерения существует калориметрический
метод. В системе
удельная
теплота плавления измеряется в
 .
.
