
9edef0be_hasledstvennost_2009-2-2
.pdf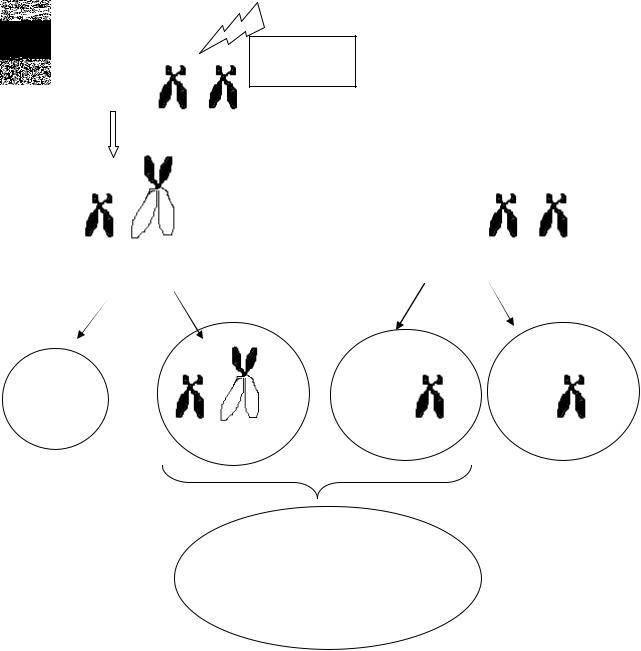
Вследствие этого происходит или неравномерное распределение хромосом (в одной половой клетке оказывается материал 22-х хромосом, а в другой — 24- х) или эти хромосомы распадаются с образованием новых хромосом, одна из которых состоит из двух длинных плеч хромосом-предшественниц, а другая — их двух коротких плеч. Так возникают частичные моносомии и трисомии по той или иной паре хромосом. Фрагмент одной хромосомы может присоединиться к хромосоме другой группы.
Транслокационный синдром Дауна. В родительской гамете (обычно ма-
теринской) возникает сбалансированная робертсоновская транслокация (21/13, 21/14, 21/15). При этом, у одного из родителей обнаруживается фенотипически непроявляющаяся транслокация 21 хромосомы на 13, 14 или 15 (т.н. сбалансированная транслокация, при которой хромосомного дисбаланса в клетках нет, но порядок расположения некоторых участков хромосом отличается от нормального). У такого человека с вероятностью в 1/4 образуются гаметы с двумя 21 хромосомами (одна свободная и одна транслоцированная). При слиянии такой гаметы с нормальной формируется трисомия по 21 хромосоме. Это заболевание отличается от синдрома Дауна, связанного с трисомией по 21 паре тем, что носит более стертый характер и не связано с возрастом матери.
1-я гамета |
2-я гамета |
Мутагенный фактор
гамета с робертсоновской |
|
|
нормальная гамета |
||||
транслокацией |
|
|
|
|
|
|
|
|
|
МЕЙОЗ |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
оплодотворение
11

Зигота с избытком хромосомного материала по 21 паре
Рис. 3 Механизм формирования транслокационного синдрома Дауна. Белым цветом обозначена 13 (14 или 15) пара хромосом, черным – 21. В одной из гамет находится избыток генетического материала из 21 пары, что после оплодотворения приведет к частичной трисомии по данной паре. Во второй зиготе будет недостаток (делеция) 21 пары.
Филадельфийская хромосома — транслокация между 9 и 22 хромосомами, приводящая к переносу длинного плеча 22-й хромосомы на 9-ю. В 95 % случаев эта мутация является причиной одной из форм хронической лейкемии.
III. Генные мутации
Генные мутации — это изменения структуры наследственного вещества на молекулярном уровне.
Мутационные изменения генов могут происходить в одной точке (односайтовые, моногенные мутации) либо в нескольких разных точках (многосайтовые, полигенные мутации).
Выделяют два основных механизма генных мутаций: — это замена нуклеотидов и сдвиг рамки считывания. Мутации вследствие сдвига рамки считывания встречаются более часто.
A.Виды мутаций
1)Мутации с заменой пар оснований (субституции)
Существуют 2 типа замены нуклеотидов: транзиции и трансверсии.
а) Транзиция заключается в замене одного пиримидинового основания на другое пиримидиновое основание. Возможны 4 варианта транзиций.
б) При трансверсии пурин меняется на пиримидин и наоборот. Возможны 8 вариатнов трансверсий.
Вследствие этих мутаций происходит замена какой-либо аминокислоты в
структуре белка, синтез которого кодирует данный ген и, следовательно, меняется биохимический фенотип (например, образуются патологические варианты молекулы гемоглобина — серповидно-клеточная анемия, талассемия).
2) Мутации, вызывающие сдвиг рамки считывания
Выделяют вставки (аддиции) и делеции.
а) Вставка — добавление нуклеотидной пары в ДНК (плюс-мутация). б) Делеция — выпадение нуклеотида из последовательности ДНК (ми- нус-мутация).
Мутации этого типа автоматически приводят к сдвигу рамки считывания нуклеотидной последовательности при трансляции кода.
12
B. Патогенез генных мутаций
Генные мутации приводят к изменению структурных или функциональных генов и, в конечном счете, к изменению структуры или количества белка. Возможны следующие варианты:
−синтез аномального белка;
−выработка избыточного количества белка;
−отсутствие синтеза белка;
−недостаточный синтез белка.
Клинические проявления генных болезней, тяжесть и скорость их развития зависят от особенностей генотипа организма (время действия мутантного гена, гомо- и гетерозиготность и др.), возраста больного, условий внешней среды (питание, охлаждение, стрессы, переутомление) и др. факторов.
Особенностью генных болезней является их гетерогенность, т.е. одно и то же фенотипическое проявление болезни может быть обусловлено мутациями в разных генах или разными мутациями внутри одного гена.
C. Типы наследования генных мутаций
Различают аутосомно-доминантные, аутосомно-рецессивные и сцепленные с половыми хромосомами генные болезни.
С.1. Аутосомно-доминантный тип
Данный тип наследования характеризуется следующими особенностями:
−Один или оба родителя больны и это проявляется фенотипически;
−патологический признак проявляется в каждом поколении;
−если болен один из родителей, то вероятность рождения больного ребенка составляет 50%;
−мужчины и женщины болеют одинаково часто.
Патология формируется в результате образования аномального продукта, а не недостаточности каких-либо ферментов.
Примеры доминантных наследственных заболеваний: Ахондроплазия: карликовость, седловидный нос, макроцефалия, иногда
гидроцефалия. Короткие конечности при нормальной длине туловища. Нейрофиброматоз (болезнь Реклингаузена): множественные пятна на
коже цвета "кофе с молоком", пигментные пятна радужки, фибромы, невриномы, нейрофибромы кожи, псевдоартрозы и др.
Синдром Марфана: рост выше среднего, длинные тонкие конечности, кифосколиоз, воронкообразная грудь, миопия (близорукость) высокой степени, аневризмы аорты, аортальная недостаточность.
Брахидактилия: укорочение (отсутствие средних фаланг).
С.2. Аутосомно-рецессивный тип
Данный тип наследования характеризуется следующими особенностями:
−проявляется не в каждом поколении, а только в том случае, если ребенок гомозиготен по патологическому гену;
13
−больные дети рождаются, как правило, от фенотипически здоровых родителей (носителей патологического гена);
−мужчины и женщины болеют одинаково часто.
Рецессивно наследуются наследственные заболевания, при которых отсутствует нормальный продукт гена (определенный фермент, фактор свертывания или другой белок),. Например, ферментопатии: фенилкетонурия, алкаптонурия, альбинизм и др.
Сцепленный с полом тип наследования болезней
Связан с дефектом генов Х- и У-хромосом.
Х-сцепленный доминантный тип наследования.
Заболеваниям, наследуемым по этому типу, присущи следующие особенности:
1.Все сыновья пораженных отцов и здоровых матерей не несут патологических генов, и их дети здоровы.
2.Все дочери пораженных отцов больны.
3.Среди детей пораженных матерей половина здорова, половина больна. Примеры болезней:
Фолликулярный кератоз (аномалии волосяных фолликулов). Заболевание, которое приводит к полной или частичной потере ресниц, бровей и волос на голове. Тяжелые формы этой болезни наблюдаются только у мужчин.
Устойчивый к витамину Д рахит с гипофосфатемией. Описаны редкие аномалии, сцепленные с Х-хромосомой и встречающиеся почти только у лиц женского пола, так как поражение мужских зигот оказывается настолько сильным, что они погибают еще до рождения.
Х-сцепленный рецессивный тип наследования
Основные формальные характеристики этого типа следующие:
1.Обычно пораженными являются мужчины.
2.Все их фенотипически здоровые дочери являются гетерозиготными носительницами.
3.Среди сыновей гетерозиготных матерей соотношение пораженных
инепораженных 1:1.
Рецессивными Х-хромосомными заболеваниями являются: дальтонизм, гемофилия А и В, синдром Вискотта-Олдриджа.
Гемофилия — нарушение коагуляционного гемостаза, вследствие отсутствия факторов VIII, IX. Ген проявляется фенотипически лишь в гомозиготном состоянии у мужчин (родословная потомков королевы Виктории в европейских королевских домах).
Синдром Вискотта-Олдриджа — Х-сцепленный иммунодефицит, связанный с мутациями гена мембранного сиалопротеина, участвующего в формировании цитоскелета. Аномалии цитоскелета отражаются на форме и функции клеток крови (тромбоцитов, фагоцитов, лимфоцитов), межклеточных взаимодействиях и процессах передачи межклеточных сигналов при контакте Т- клеток с антигенпредставляющими клетками и В-лимфоцитами. Проявления: геморрагический синдром капиллярного типа, обусловленный тромбоцитопе-
14
нией и тромбоцитопатией, инфекционный синдром, отсутствие В-клеток, экспрессирующих и синтезирующих IgM; прогрессирующее снижение количества Т-лимфоцитов.
У-сцепленный тип наследования
Болеют только мужчины. Примеры:
Ихтиоз – редкое заболевание, характеризующееся нарушением процесса слущивания кожного эпителия. В результате кожа приобретает вид, сходный с чешуйками рыб или земноводных.
Также с У-хромосомой передается избыточная волосатость ноздрей и ушных раковин.
IV. Митохондриальные мутации
У человека митохондрии являются единственным хранилищем внеядерного генетического материала. Источником митохондрий в зиготе, вероятно, служит только яйцеклетка. Хотя 95 % мито-хондриальных белков кодируются в ядре, мутации мт-ДНК происходят в 10 раз чаще, чем в ядерных генах.
Чаще всего преобладает вклад материнского организма. Яйцеклетка — это крупная клетка с большим объемом цитоплазмы, в которой с помощью электронного микроскопа обнаруживают все органеллы, в том числе и множество митохондрий (около 25 000 митохондрий). Сперматозоид же, хотя и имеет упакованные специальным образом в области шейки четыре митохондрии, утрачивает их вскоре после того, как проникает внутрь яйцеклетки, поскольку его хвостовая часть быстро растворяется. Следовательно, генетический материал, локализованный в кольцевых молекулах митохондриальной ДНК, наследуется по материнской линии. В митохондриях окислительные процессы, связанные с синтезом АТФ, сопровождаются образованием большого количества свободных радикалов, которые могут вызывать мутации в митохондриальнои ДНК, а процесс репарации митохондриальнои ДНК развит, вероятно, не так хорошо, как ДНК ядерной. Так, частота мутаций в митохондриальнои ДНК примерно в 10 раз выше, чем в ядерной. Для митохондриальнои ДНК известны точечные мутации: делеции и вставки. Современные исследователи предполагают, что мутации в митохондриальной ДНК являются причиной более ста болезней: диабета, некоторых видов миопатии, кардиомиопатии, энцефаломиопатии, кислотного ацидоза, динамического нарушения мозгового кровообращения, эпилепсии и др.
Для митохондриальной наследственности характерны следующие при-
знаки
1.Болезнь передаётся только от матери.
2.Больны и девочки, и мальчики.
3.Больные отцы не передают болезни ни дочерям, ни сыновьям.
15
Фенотипическое проявление мутаций мт-ДНК во многом зависит от уровня потребления АТФ той или иной тканью. Поскольку наиболее энергозависимыми являются нервная и мышечная системы, то такие мутации часто проявляются в форме различных невропатий и миопатий.
Недавно обнаружено, что в редких случаях встречается отцовская наследственность митохондриальной ДНК. По-видимому, это возможно тогда, когда, после оплодотворения яйцеклетки, содержащий митохондрии хвост сперматозоида не лизируется.
Частота классических митохондриальных болезней доходит до 5,7 на 100 000 населения. Номенклатура их заболеваний насчитывает 200 нозолоческих единиц.
Выделяют митохондриальные болезни с нарушением транспорта субстратов в митохондрии (дефицит карнитина), запасания АТФ (дефицит АТФазы), дефектами дыхательной цепи (дефицит цитохромов). Наиболее ярко клинически значимые нарушения проявляются в тканях с высокой потребностью в кислороде (мышечной, нервной).
Относительно хорошо изучены митохондриалъные миопатии. Характерные повреждения митохондрий при этих болезнях придают мышечным волокнам изорванный вид. Органоиды увеличены, содержат кристаллические включения и кристы искаженной формы. При специальной гистологической окраске скопления митохондрий приобретают красный цвет, вследствие чего мышечные волокна при митохондриальных болезнях описывают в литературе, как «красные изорванные волокна». Характерно компенсаторное увеличение количества митохондрий в клетках.
Наиболее часто, наследственные митохондриопатии выражаются в поражении головного мозга. При дефиците цитохрома С или пируватдегидрогеназы преобладают явления подострой некротической энцефалопатии (синдром Лея): развиваются симметричные некрозы в головном и спинном мозге, что ведет к атаксии, судорогам, задержке умственного развития и гипотонии. Имеется метаболический ацидоз с накоплением в мозге лактата и пирувата. Это обусловливает рвоту.
Методы изучения наследственной патологии.
Генеалогический метод (составления родословных) позволяет установить тип наследования генетического дефекта, время появления первого мутантного гена, вероятность рождения ребенка с наследственным заболеванием. Родословная должна охватывать не менее 4 поколений, быть по возможности полной, включать все данные, которые могут представлять интерес: спонтанные аборты, мертворожденные, гибель детей в неонатальном периоде, бесплодные браки.
Наличие аналогичного поражения в нескольких поколениях одной семьи у родителей и детей свидетельствует об аутосомно-доминантном типе передачи. Сходные болезни у детей здоровых родителей позволяют предположить
16
аутосомно-рецессивное наследование. Кровное родство и эндогамия также указывают на аутосомно-рецессивный тип передачи. Появление заболевания только у мужчин или только у женщин может быть при наследовании, сцепленном с полом.
Популяционный метод используется для установления частоты тех или иных пороков развития в популяции. Популяция - совокупность особей данного вида, населяющих определенную территорию в течение длительного периода на протяжении многих поколений.
Основная закономерность генетической популяции была установлена в 1908 году независимо друг от друга английским математиком Г. Харди и немецким врачом В. Вайнбергом. Их закон гласит, что в популяции устанавливается равновесие частот генотипов, которое сохраняется из поколения в поколение. Эта зависимость основывается на математическом расчете.
Если частоту гена обозначить р, а его аллеля - q и если в локусе нет других аллелей, то р+q=1. При наличии панмиксии (случайные браки, без подбора партнера по генотипу), отсутствии притока аллелей, вызываемого отбором, равной плодовитости гетеро- и гомозигот, непрерывности поколений и достаточно большой численности популяций распределение генотипов при скрещивании особей можно описать следующей формулой:
(p+q) x (p+q)=1 (100%), при этом частота гомозигот будет равна соответственно р2 (АА) и q2 (аа), а гетерозигот (Аа) - 2рq. Для аутосомных генов при отсутствии каких-либо нарушений указанных условий эти пропорции сохраняются во всех последующих поколениях.
Практическое применение данного закона можно пояснить на следующем примере. Допустим, в городе с населением 1 млн человек зарегистрировано 200 больных с фенилкетонурией. Данное заболевание наследуется аутосомнорецессивно, т.е. у данных больных дефектный ген находится в гомозиготном состоянии. То есть:
q2 (частота аа) = 200: 1 000 000 = 0,0002 (или больных из всех жителей
0,02%)
q (частота рецессивного аллеля) = √0,0002 = 0,014
р+q=1, следовательно р (частота доминантного аллеля) = 1-0,014 = 0,986. Отсюда можно сделать следующий вывод:
р2 (частота АА, не имеют дефектного гена) = 0,9862 = 0,97 (97% населения города)
2рq (здоровые носители патологического гена) = 2х0,986х0,014 = 0,027 (2,7% населения города)
Редкие гены встречаются преимущественно в гетерозиготном состоянии. В результате близкородственных браков (инбридинг) резко повышается вероятность встречи двух редких одинаковых аллелей. Двоюродные брат и сестра получают 1/8 общих генов от одного и того же предка, в том числе и патологических. В связи с этим в большинстве стран запрещены браки между близкими родственниками. Самые дальние родственники, которые учитываются при оценке кровного родства двух индивидов, - троюродные сибсы. Это объясняется тем, что при переходе за третье поколение рост коэффициента инбридинга
17

индивида с увеличением числа кровнородственных браков между предками происходит очень медленно.
Частота кровнородственных браков велика в изолятах подгруппы популяций, которые размножаются обособленно. Пропорция гомозиготных доминантов, гетерозиготных доминантов и гомозиготных рецессивных пораженных лиц оказывается совершенно отличной от пропорции, господствующей во всей популяции. Высокая частота изолятов в Японии, Южной Индии, племенах Египта и т.д., что связано с религиозными, географическими и этническими особенностями.
Близнецовый метод позволяет выявить роль генетических факторов и факторов внешней среды в возникновении наследственных заболеваний. С этой целью изучают конкордантность (сходство, наличие аналогичного заболевания у обоих близнецов) и дискордантность (наличие болезни только у одного близнеца) у однояйцевых (однояйцевые близнецы развиваются из одной зиготы и имеют одинаковые генотипы) и разнояйцевых (разнояйцевые близнецы дизиготны и генотип у них схож не более, чем у обычных братьев и сестер) близнецов. У однояйцевых близнецов разница признаков зависит только от внешних условий. Если признак отличается у разнояйцевых близнецов, но тождествен у однояйцевых – следовательно, заболевание генетически детерминировано (сахарных диабет, эпилепсия и др., см. таблицу). Если признак показывает одинаковую степень конкордантности и у тех, и у других – ведущую роль играют факторы внешней среды (инфекции).
заболевание |
Частота |
заболевание |
|
Частота |
||
|
|
заболевания |
|
заболевания |
||
|
|
обоих |
близ- |
|
обоих близне- |
|
|
|
нецов |
|
|
цов |
|
|
|
ОБ |
РБ |
|
ОБ |
РБ |
туберкулез |
|
7 |
23 |
эпилепсия |
56 |
10 |
пилоростеноз |
|
67 |
3 |
идиотия |
97 |
37 |
сахарный диабет |
|
65 |
18 |
шизофрения |
96 |
19 |
косолапость |
|
32 |
3 |
корь |
98 |
94 |
заячья губа |
|
33 |
5 |
коклюш |
96 |
93 |
ревматизм |
|
47 |
17 |
маниакально- |
96 |
19 |
|
|
|
|
депрессивный психоз |
|
|
врожденный |
вывих |
41 |
3 |
эндемический зоб |
71 |
70 |
бедра |
|
|
|
|
|
|
ОБ – однояйцевые близнецы, РБ – разнояйцевые близнецы.
Методы диагностики наследственных заболеваний.
Цитологический метод - исследование кариотипа в ядрах делящихся клеток. Кариотип определяют либо в делящихся клетках красного костного мозга, либо искусственно культивируют любые доступные клетки (например, лимфоциты, эпителиоциты плода из амниотической жидкости). К культуре клеток добавляют митоген (фитогемагглютинин) и через 2-3 суток останавли-
18
вают процесс их деления с помощью колхицина. Далее клетки обрабатываются гипотоническим расвором натрия хлорида, в результате цитолемма разрывается и получается «россыпь хромосом». В стадию метафазы хромосомы максимально спирализованы и хорошо видны под микроскопом. Их подсчитывают и идентифицируют. Таким образом можно диагностировать геномные и грубые хромосомные мутации.
Для выявления количественных изменений половых хромосом определяют половой хроматин (тельца Барра, Х-хроматин). Он представляет собой гетерохроматизированную, инактивированную Х-хромосому, которая видна как глыбка треугольной или округлой формы на периферии ядра. У женщин такие тельца в норме видны в 20-60% клеток (это определяется фазой клеточного цикла и функциональной активностью данной клетки), у мужчин их быть не должно, но до 13% клеток могут содержать т.н. псевдохроматин – конденсированные участки аутосом и Y-хромосомы. Половой хроматин можно обнаружить в эпителии слизистой оболочки рта, влагалища, ядрах эпителия канальцев почек. Для более точной диагностики пола используется определение Y- хроматина. С этой целью клетки окрашивают флюорохромами, и конденсированный участок Y-хромосомы при микроскопии в ультрафиолетовых лучах виден как светящаяся глыбка.
Отсутствие полового хроматина у женщин указывает на моносомию (ХО). Наличие полового хроматина по женскому типу у мужчин, два и более тельца у мужчин и женщин свидетельствуют о наличии полисомии Х (ХХХ, ХХY, ХХХY). В ядрах лейкоцитов половой хроматин обнаруживается в виде барабанных палочек.
Деpматоглифика - установление диагноза по линиям ладоней, пальцев и подошв. Hаибольшее значение имеет этот метод при изучении хромосомных заболеваний. Довольно характерными изменениями кожного узора сопровождается трисомия 13, 18, 21 пар. Hапример, при болезни Дауна отмечается одна поперечная складка на пятом пальце, поперечная линия на ладони ("обезьянья линия") и др. Hадо отметить, что дерматоглифика может служить только вспомогательным диагностическим тестом, так как аномальные признаки могут встречаться и у здоровых людей.
Биохимический метод часто используется при диагностике генных болезней. Биохимические показатели (первичный белковый продукт гена, накопление патологических метаболитов внутри клетки) отражают сущность болезни более адекватно, чем клинические симптомы. С помощью биохимических методов описано более 1000 наследственных болезней обмена веществ. Дефекты ферментов устанавливают путем определения содержания в биологических средах (например, моче и крови) продуктов метаболизма, являющихся продуктом функционирования данного белка. Например, с помощью тонкослойной хроматографии мочи и крови можно диагностировать нарушения обмена аминокислот, олигосахаридов и гликозаминогликанов (мукополисахаридов). Газовая хроматография применяется для выявления наследственных болезней обмена органических кислот. С помощью электрофореза гемоглобинов диагностируется вся группа гемоглобинопатий.
19

Но решающим методом, особенно при установлении генной патологии, является молекулярно-генетический метод. Это группа методик для исследования структуры ДНК (блот-гибридизация с использованием ДНК-зондов, ПЦР-амплификация отдельных фрагментов, аллель-специфическая гибридизация, секвенирование гена или его фрагмента), что позволяет диагностировать заболевание на уровне первичного патологического гена уже в первом триместре беременности. В некоторых случаях такая пренатальная диагностика позволяет провести дородовую профилактику и лечение заболевания.
Сущность ДНК-зондовой диагностики (рис.4):
сначала ДНК, выделенная из любой ткани, подвергается расщеплению ферментамирестриктазами, которые «узнают» строго определенную последовательность нуклеотидов, причем набор фрагментов для каждого индивида всегда постоянен. Данный этап необходим, т.к. ДНКдиагностика весьма дорого стоит, а количество генов во всех хромосомах велико. Поэтому при подозрении на генетическое заболевание из хромосом вы-
деляется тот участок ДНК, который содержит предполагаемый дефектный ген.
далее осуществляется полимеразная цепная реакция (ПЦР), с помощью которой в течение нескольких часов этот фрагмент ДНК размножается в количестве, превышающем исходное в 109 раз. Это облегчает работу с минимальными количествами образцов ДНК. ПЦР настолько чувствительна, что позволяет исследовать единичную копию гена в исходном материале.
смесь фрагментов подвергают электрофорезу и они разделяются по размеру. Местоположение определенных участков всегда постоянно.
зафиксированные на фильтре фрагменты подвергаются гибридизации с т.н. зондом – олигонуклеотидом, меченным радиоактивным изотопом. Зонд – это клонированный генно-инженерным методом конкретный ген, функция которого известна. Он связывается с соответствующим ему геном по принципу комплементарности.
20
