
- •Основные признаки металлического состояния. Нормальные и переходные металлы.
- •Осн. Типы кристалл. Решеток металлов. Плотность упаковки, координ. Число, число узлов на элем. Ячейку.
- •Различие понятий: кристаллическая решетка и кристаллическая структура. Кристаллографические индексы узлов, направлений, плоскостей.
- •Реальные строения металлических кристаллов. Точечные и линейные дефекты в кристаллах и их влияние на свойства кристаллов.
- •Влияние нагрева на строение и свойства холоднодеф. Металла. Возврат и рекристаллизация.
- •Твердые растворы. Основные типы твердых растворов.
- •Металлические соединения. Электронные соединения, фазы внедрения, фазы Лавеса.
- •Связь между свойствами сплавов и типом диаграммы состояния.
- •Фазы и структурные составл. Диаграмме .
- •Углеродистые стали обыкн. Качества. Качественные углеродистые стали. Маркировка, применения.
- •Серые, высокопрочные чугуны. Чугуны с вертикальным графитом. Маркировка, структура, свойства, применения.
- •Ковкие и антифрикционные чугуны. Чугуны с верт. Графитом. Маркировка, структура, свойства, применения.
- •Обозначение критических точек стали. Осн. Виды то.
- •Образование аустенита. Диаграмма изометрического превращения перлита в аустенит. Крупно и мелко зер.Стали.
- •Распад аустенита. Диаграмма изометрического и термического превращения переохлажденного аустенита.
- •Мартенситные превращения в стали, его особенности. Кристаллогеометрия мартен. Превращения по схеме Бейна.
- •Превращения при отпуске стали.
- •Влияние термической обработки на свойство стали.
- •Закалка стали. Способы закалки.
- •Режимы закалки
- •Прокаливемость и закаливаемость стали.
- •Отжиг и нормализация стали.
- •Термомеханическая обработка стали.
- •Хто. Связь диаграммы состояния со структурой диффузионного слоя (на примере диаграммы ).
- •Цементация стали. Термической обработка после цементации. Стали для цементации.
- •Азотирование. Стали для азотирования.
- •Нитроцементация стали. Термическая обработка после нитроцементации. Стали для нитроцементации.
- •Диффузионная металлизация.
- •Влияние легирующих элементов на полиморфизм железа. Распределение легирующих элементов в стали.
- •Влияние легирующих элементов на свойства феррита. Карбидная фаза в легированных сталях.
- •Влияние лэ на кинетику расплава переохлажденного аустенита, интервал мартенситного превращения.
- •Влияние лэ на рост зерна а. Наследственно мелкозерн. Стали. Влияние лэ на превращение при отпуске стали.
- •Классификация и маркировка легированных сталей.
- •Маркировка легированных сталей.
- •Пружинные стали общего и специального назначения.
- •Подшипниковые стали общего и специального назнач..
- •Автоматные стали. Мартенситстар. Стали.
- •Рельсовые стали. Износостойкая сталь Гатфильда.
- •Основные группы коррозионностойких сталей.
- •Жаростойкость. Осн. Группы жар. Сталей и сплавов.
- •Жаропрочность, хар. Жаропрочности. Теплоуст. Стали.
- •Ауст. Жаропр. Стали. Жаропр.Е сплавы на основе никеля.
- •Углеродистые и легированные не теплостойкие стали для режущего инструмента.
- •Теплостойкость. Быстрорежущие стали с особенности их термической обработки.
- •Металлокерамические твердые сплавы.
- •Штамповые стали для хол. Деформирования металлов.
- •Штамповые стали для горячего деформ.Металлов.
- •Алюминий. Примеси (железо, кремний) в алюминии и их влияние на свойства алюминия. Классификация алюминиевых сплавов (литейные, деформируемые).
- •Термическая обработка сплавов алюминий-медь. Деформируемые алюминиевые сплавы, упрочняемые термической обработкой (дюралюмины).
- •Деформируемые алюминиевые сплавы, не упрочняемые термической обработкой.
- •Алюминиевые сплавы для фасонного литья.
- •Медь. Влияние примесей (висмут, свинец) на свойства меди. Сплавы меди с цинком (латуни), их маркировка.
- •Сплавы меди с оловом и другими элементами (бронза). Маркировка бронз. Бериллиевая бронза.
- •Материалы для подшипников скольжения
-
Основные признаки металлического состояния. Нормальные и переходные металлы.
Металлы – один из классов конструкционных материалов, характеризующийся определённым набором свойств:
-
«металлический блеск» (хорошая отражат. способность);
-
пластичность;
-
высокая теплопроводность;
-
высокая электропроводность.
Металлическое состояние – основная хар-ка: положительного температурного коф. эл.сопр.
Нормальные: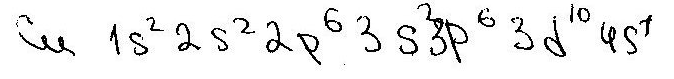
Переходные: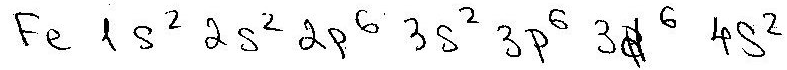
Данные свойства обусловлены особенностями строения металлов. Согласно теории металлического состояния, металл представляет собой вещество, состоящее из положительных ядер, вокруг которых по орбиталям вращаются электроны. На последнем уровне число электронов невелико, и они слабо связаны с ядром. Эти электроны имеют возможность перемещаться по всему объему металла, т.е. принадлежать целой совокупности атомов.
Таким образом, пластичность, теплопроводность и электропроводность обеспечиваются наличием «электр. газа».
Все металлы, затвердевающие в нормальных условиях, представляют собой кристаллические вещества, то есть укладка атомов в них характеризуется определенным порядком – периодичностью, как по различным направлениям, так и по различным плоскостям. Этот порядок определяется понятием кристаллическая решетка.
-
Осн. Типы кристалл. Решеток металлов. Плотность упаковки, координ. Число, число узлов на элем. Ячейку.
В зависимости от расположения атомов в ячейке различают простые, кубические, объемно-центрированные кубические, гранецентрированные кубические, гексагональные решетки.
1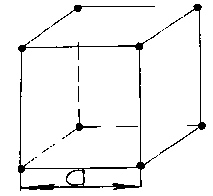
 .Простая
решетка
представляется
в виде куба, в узлах которой располагаются
атомы. Простейшая решетка опис. одним
параметром, это ребро куба а.
.Простая
решетка
представляется
в виде куба, в узлах которой располагаются
атомы. Простейшая решетка опис. одним
параметром, это ребро куба а.
2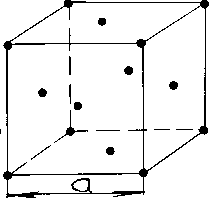 .Объемно-центрированная
кубическая решетка (ОЦК)
представляет собой также куб, внутри
которого дополнительно расположен еще
один атом. Параметры решетки длина ребра
куба а.
.Объемно-центрированная
кубическая решетка (ОЦК)
представляет собой также куб, внутри
которого дополнительно расположен еще
один атом. Параметры решетки длина ребра
куба а.
3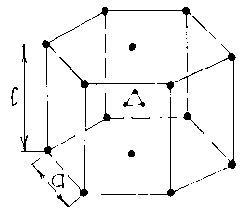 .Гранецентрированная
кубическая решетка (ГЦК)
представляет собой куб, В центре каждой
грани которого расположены допол. по
одному атому.
.Гранецентрированная
кубическая решетка (ГЦК)
представляет собой куб, В центре каждой
грани которого расположены допол. по
одному атому.
4.Гексагональная плотно упакованная решетка. В отличие от кубической хар. двумя параметрами а и с.
В случае, если отношение с/а=1,666, то решетка считается плотноупакованной, а иначе – неплотно упакованной.
Примеры: ОЦК – вольфрам, молибден, железо Fe; ГЦК – алюминий, медь, никель, железо Fe; ГПУ – бериллий. Некоторые металлы индий, имеют тетрагональную решетку.
П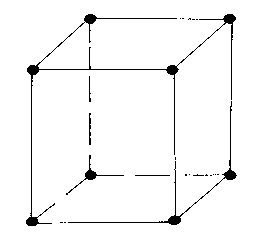 лотность
упаковки
атомов в кристаллической решетке –
объем, занятый атомами, которые условно
рассматриваются как жесткие шары. Ее
определяют как отношение объема, занятого
атомами к объему ячейки (для ОЦК– 0,68,
для ГЦК – 0,74)
лотность
упаковки
атомов в кристаллической решетке –
объем, занятый атомами, которые условно
рассматриваются как жесткие шары. Ее
определяют как отношение объема, занятого
атомами к объему ячейки (для ОЦК– 0,68,
для ГЦК – 0,74)
Элементарная ячейка – элемент объема из минимального числа атомов, многократным переносом которого в пространстве можно построить весь кристалл.
Координационное число (К) указывает на число атомов, расположенных на ближайшем одинаковом расстоянии от любого атома в решетке.
-
Различие понятий: кристаллическая решетка и кристаллическая структура. Кристаллографические индексы узлов, направлений, плоскостей.
Кристаллическая структура – конкретное расположение матер. частиц (атомов, ионов) в пространстве.
Кристаллическая решетка – условно точечное построение, с помощью которого мы описываем кристаллическую структуру.
Кристаллическая решетка бесконечна по строению, а кристаллическая структура конечна.
П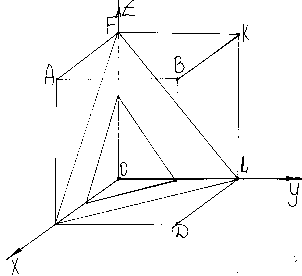 од
кристаллограф. плоскостями
понимается 3 целых взаимно простых числа
обратно пропорц. числу осевых единиц,
отсекаемых данной плоскостью по коорд.
осям x,
y,
z.
од
кристаллограф. плоскостями
понимается 3 целых взаимно простых числа
обратно пропорц. числу осевых единиц,
отсекаемых данной плоскостью по коорд.
осям x,
y,
z.
ABCD (100), AFKB (001), BKLD (010)
Под индексами кристаллографических плоскостей и направлений было вызвано потребностью объяснить зависимость свойств металлов от направлений кристаллографических плоскостей. Иными словами, дать объяснение с точки зрения техники понятие влияния анизотропии.
По различным направлениям в кристалле располагаются различные количества атомов: физические, химические, механические при прочих равных условиях и определяются числом атомов, расположенным в данном направлении; чем больше количество атомов расположено в данном направлении, тем выше уровень свойств.
Неодинаковость свойств по различным направлениям в кристалле и называется анизотропией. Кристалл анизотропен.
