
лаба 5 химия
.docx
Вариант 1
Цель работы:
Экспериментально определить содержимое каждой из шести представленных пробирок, не используя ни одного дополнительного реактива.
Реактивы: хлорид натрия (NaCl), хлорид аммония (NH4Cl), хлорид алюминия (AlCl3), карбонат натрия (Na2CO3), хлорид бария (BaCl), гидрооксид натрия (NaOH).
Оборудование: штатив с пробирками (пустые и с определяемыми
растворами веществ).
Экспериментальная часть
1) Проверили колбы на щёлочную или кислотную среду с помощью определяющих полосок.
пробирка 1) PH = 5 NH4Cl
пробирка 2) PH = 3 AlCl3
пробирка 3) PH = 10 Na2CO3
пробирка 4) PH = 7 BaCl2
пробирка 5) PH = 12 NaOH
пробирка 6) PH = 6 NaCl
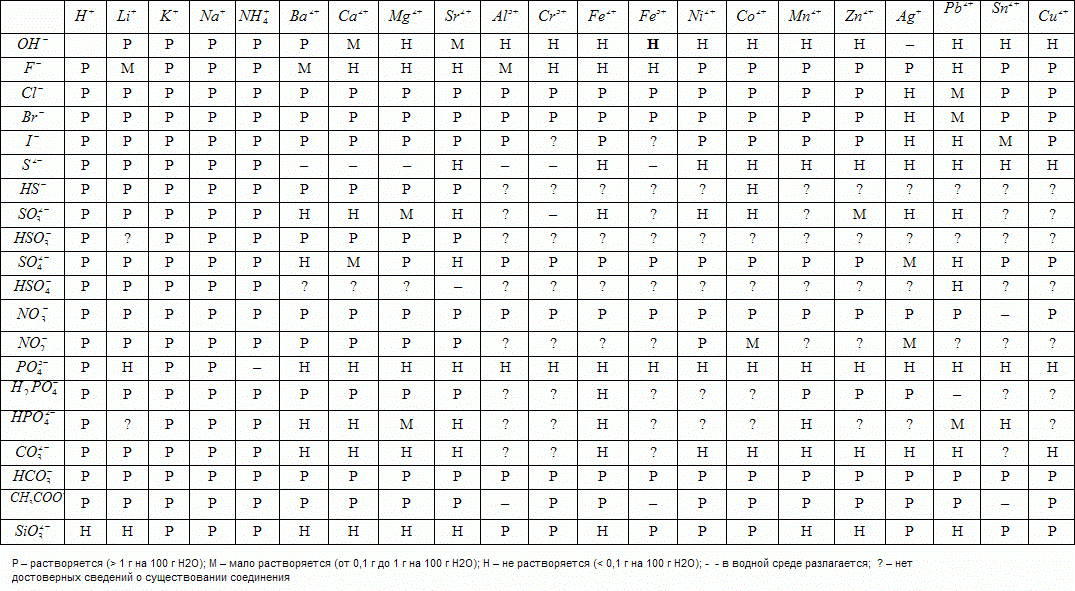
2) Согласно таблице растворимости
Na2CO3 не растворим, значит
Na2CO3 + H2O = NaOH + H2CO3 (CO2 + HCO) значит Na2CO3 может быть в 3 или 5 колбе (с наибольшим значением PH).
3) Смешали 1 и 5 пробирки и получили запах аммиака. Значит:
NH4Cl + NaOH = NH4OH (NH3 + H2O) + NaCl
Из этого получается, что в 1 пробирке находится NH4Cl, 5 – NaOH а в 3 – Na2CO3
4) Смешали 2 и 3 пробирки и получили светло-голубой осадок. Значит:
AlCl3 + Na2CO3 + H2O = Al(OH)3 + NaCl + H2CO3
5) Смешали 2 и 5 пробирки и получили светло-голубой осадок. Значит:
AlCl3 + 3NaOH = Al(OH)3 + 3NaCl – из этого следует, что во 2 пробирке находится AlCl3
6) Смешали 3 и 4 пробирки и получили мутный белый осадок. Значит:
Na2CO3 + BaCl2 = 2NaCl + BaCO3
Значит в 4 пробирке находится BaCl2
7) Внесли полученные результаты в таблицу 1.
Таблица 1. Результат проверки среды колб.
|
|
NaCl |
NH4Cl |
AlCl3 |
Na2CO3 |
BaCl |
NaOH |
|
NaCl |
PH =6 |
|
|
|
|
|
|
NH4Cl |
|
PH =5 |
|
|
|
↑ |
|
AlCl3 |
|
|
PH =3 |
↓ |
|
↓ |
|
Na2CO3 |
|
|
↓ |
PH =10 |
↓ |
|
|
BaCl |
|
|
|
↓ |
PH =7 |
|
|
NaOH |
|
↑ |
↓ |
|
|
PH =12 |
Вывод: в ходе лабораторной работы было установлено, что в:
1 пробирке находится NH4Cl
2 пробирке находится AlCl3
3 пробирке находится Na2CO3
4 пробирке находится BaCl2
5 пробирке находится NaOH
6 пробирке находится NaCl
