Методичка. Молекулярка. термодинамика
.pdf
Для контроля температуры сжатого газа используется лабораторный термометр 3. На рис. 3 показаны примеры подобных изотерм для газа – сернистого гексафторида.
Рис. 3. Изотермы P-V для сернистого гексафторида Изотермы газа, значения которых лежат ниже определенной
температуры имеют вид плато, в этом месте происходит сжижение газа
(паро-жидкостное равновесие). Точка, в которой плато более не существует, называется критической точкой. Для SF6 критическая точка находится при Tкр=46ºС =319 К и Pкр=3,8 МПа.
ЗАДАНИЕ
1.Проведите измерения, заполните таблицу.
2.Постройте графики изотерм исследуемого газа.
171
3.Из графиков изотерм определите значения критической точки исследуемого газа.
4.Найдите погрешность определения значений критической точки.
5.Рассчитайте значения постоянных уравнения Ван-Дер-Ваальса по формулам (9) и (10).
6.Рассчитайте значение радиуса молекулы газа по формуле (4).
7.Рассчитайте значения параметров потенциала взаимодействия молекул по формулам (11), (12).
8.Сделайте выводы по работе.
ПОРЯДОК ВЫПОЛНЕНИЯ РАБОТЫ
1.Включите иммерсионный термостат.
2.Нажмите желтую кнопку 2 раза для установки требуемой температуры. Установите требуемую температуру, используя кнопки
«вверх» и «вниз». Подождите 1 минуту, пока температура газа
установится. Для контроля температуры газа используйте лабораторный
термометр.
3.При помощи вентиля регулировки объема установите необходимое значение объема газа в сосуде. Используйте шкалу на сосуде давления для контроля значений объема. Шкала проградуирована в единицах см3.
4.После того, как стрелка манометра уравновесится, определите значение давления при заданном значении объема.
5.Данные опыта запишите в таблицу 1.
ВНИМАНИЕ: Не поднимайте давление газа в сосуде выше 50*105 Па.
6.Повторите процедуры 3-5 для каждого значения объема.
7.Повторите процедуры 2-5 для каждого значения температуры.
8.Постройте графики изотерм P-V исследуемого газа.
9.Определите значения критической точки газа.
10.Найдите погрешность определения значений критической точки.
172
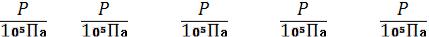
11. Рассчитайте значения постоянных уравнения Ван-Дер-Ваальса по
формулам (9) и (10).
12.Рассчитайте значение радиуса молекулы газа по формуле (4).
13.Рассчитайте значения параметров потенциала взаимодействия молекул по формулам (11), (12).
14.Сделайте выводы по работе.
|
|
|
|
|
Таблица 1 |
|
|
|
|
|
|
|
|
V/см3 |
Изотерма |
Изотерма |
Изотерма |
Изотерма |
Изотерма |
|
|
20ºС |
25ºС |
29ºС |
32,3ºС |
35ºС |
|
|
|
|
|
|
|
|
1,5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
1,25 |
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
0,9 |
|
|
|
|
|
|
|
|
|
|
|
|
|
0,8 |
|
|
|
|
|
|
|
|
|
|
|
|
|
0,7 |
|
|
|
|
|
|
|
|
|
|
|
|
|
0,6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
0,5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
0,4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
0,35 |
|
|
|
|
|
|
|
|
|
|
|
|
|
0,3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
173
ВОПРОСЫ ДЛЯ САМОСТОЯТЕЛЬНОЙ ИНДИВИДУАЛЬНОЙ
РАБОТЫ
1.Что понимают под критическим состоянием вещества?
2.Каков физический смысл констант уравнения Ван-дер-Ваальса и их размерность?
3.Какова связь констант уравнения Ван-дер-Ваальса с критическими параметрами?
4.Что такое температура Бойля? Какой ее физический смысл?
5.Какой процесс называется адиабатическим и как записывается уравнение адиабаты в переменных P – V и V – T?
6.Какой физический смысл первого закона термодинамики?
7.В чем отличие внутренней энергии идеального и реального газа?
8.Вычислите работу, производимую идеальным и реальным газом,
объясните отличие.
9. Каким образом можно вычислить размер молекулы газа?
10.В чем состоит различие изотерм реального и идеального газов?
11.Каков физический смысл потенциала взаимодействия молекул?
12.Опишите методику определения потенциала взаимодействия молекул.
13.Изобразите график функции потенциала, укажите на нем параметры
и 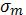 .
.
14.Как связаны постоянные Ван-Дер-Ваальса и параметры взаимодействия молекул с критическими параметрами газа?
15. Кривая взаимодействия (потенциал) молекул газа имеет минимум.
Каков физический смысл данного минимума?
16.В чем состоит качественное отличие реального газа от идеального?
17.Можно ли произвести ожижение идеального газа? Ответ обосновать.
18.Опишите состояние, называемое как «паро-жидкостное».
174
19.В чем состоит количественное отличие реального газа от идеального?
20.Рассмотрите изотермы P-V для сернистого гексафторида. Объясните наличие горизонтальных участков на изученном графике.
21.Каким образом можно изменить параметры 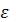 и
и 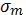 для молекул газа?
для молекул газа?
22.Какой физический смысл имеет заштрихованный участок P–V
диаграммы?
23.Опишите способ фиксации критической точки на экспериментальной изотерме.
24.Опишите методику расчета постоянных в уравнении Ван-дер-
Ваальса.
25. Какие из газов можно перевести в твердое состояние наипростейшим
способом?
175
ПРИЛОЖЕНИЯ |
||||
|
|
|
Таблица 1 |
|
Фундаментальные физические постоянные |
||||
|
|
|
|
|
Гравитационная постоянная |
|
G = 6,6720 10 11 Н м2/кг2 |
|
|
Скорость света в вакууме |
|
с = 2,99792458 108 м/с |
|
|
Магнитная постоянная |
|
0 = 12,5663706144 10 7 Гн/м |
|
|
Электрическая постоянная |
|
0 = 8,85418782 10 12 Ф/м |
|
|
Постоянная Планка |
|
h = 6,626176 10 34 Дж с |
|
|
Масса покоя электрона |
|
mе = 9,109534 10 31 кг |
|
|
Масса покоя протона |
|
mр = 1,6726485 10 27 кг |
|
|
Масса покоя нейтрона |
|
mn = 1,6749543 10 27 кг |
|
|
Элементарный заряд |
|
е = 1,6021892 10 19 Кл |
|
|
Отношение заряда электрона к |
|
е/тe = 1,7588047 1011 Кл/кг |
||
его массе |
|
|
|
|
Атомная единица массы |
|
1 а.е.м. = 1,6605655 10 27 кг |
|
|
Постоянная Авогадро |
|
NA = 6,022045 1023 моль 1 |
|
|
Постоянная Больцмана |
|
k = 1,380662 10 23 Дж/К |
|
|
Молярная газовая постоянная |
|
R = 8,31441 Дж/(моль К) |
|
|
Молярный объем идеального газа при |
|
V0 = 22,41383 10 3 м3/моль |
||
нормальных условиях |
|
|||
|
|
|
|
|
Постоянная Фарадея |
|
F = 96,48456 103 Кл/моль |
|
|
|
|
|
Таблица 2 |
|
Астрономические постоянные |
||||
|
|
|
|
|
Радиус Земли |
|
6,378164 106 м |
|
|
Средняя плотность Земли |
|
5,518 103 кг/м3 |
|
|
Масса Земли |
|
5,976 1024 кг |
|
|
Радиус Солнца |
|
6,9599 108м |
|
|
Средняя плотность Солнца |
|
1,41 103 кг/м3 |
|
|
Масса Солнца |
|
1,989 1030 кг |
|
|
Радиус Луны |
|
1,737 106 м |
|
|
Масса Луны |
|
7,35 1022 кг |
|
|
Среднее расстояние до Луны |
|
3,844 108 м |
|
|
Среднее расстояние до Солнца |
|
1,49598 1011 м |
||
(астрономическая единица) |
|
|
|
|
Период обращения Луны вокруг Земли |
|
27 сут 7 ч 43 мин |
|
|
176
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Таблица 3 |
|||
|
|
|
|
|
|
Диаметры атомов и молекул (в нм) |
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Гелий |
0,20 |
|
|
Кислород |
|
|
|
|
|
0,30 |
|
|
|
|||||||||||
|
Водород |
0,23 |
|
|
Азот |
|
|
|
|
|
0,30 |
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Таблица 4 |
|||
|
|
|
|
|
|
Критические значения Тк и рк |
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
Вещество |
|
Тк, К |
|
рк, МПа |
Вещество |
|
|
|
Тк, К |
|
|
рк, МПа |
||||||||||||
|
Водяной пар |
|
647 |
|
|
|
22,0 |
|
Азот |
|
|
126 |
|
|
3,4 |
|
|
|
|||||||
|
Углекислый газ |
|
304 |
|
|
|
7,38 |
|
Водород |
|
|
33 |
|
|
1,3 |
|
|
|
|||||||
|
Кислород |
|
154 |
|
|
|
5,07 |
|
Гелий |
|
|
5,2 |
|
|
0,23 |
|
|
|
|||||||
|
Аргон |
|
151 |
|
|
|
4,87 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Таблица 5 |
|||
|
|
Давление насыщенного водяного пара при разных температурах |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
t, С |
|
рн, Па |
|
|
t, С |
|
рн, Па |
|
|
t, С |
|
|
рн, Па |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
5 |
|
400 |
|
|
|
8 |
|
|
1070 |
|
40 |
|
|
7335 |
|
|
|
||||||
|
0 |
|
|
|
609 |
|
|
|
9 |
|
|
1145 |
|
50 |
|
|
12302 |
|
|
|
|||||
|
1 |
|
|
|
656 |
|
|
|
10 |
|
|
1225 |
|
60 |
|
|
19817 |
|
|
|
|||||
|
2 |
|
|
|
704 |
|
|
|
12 |
|
|
1396 |
|
70 |
|
|
31122 |
|
|
|
|||||
|
3 |
|
|
|
757 |
|
|
|
14 |
|
|
1596 |
|
80 |
|
|
47215 |
|
|
|
|||||
|
4 |
|
|
|
811 |
|
|
|
16 |
|
|
1809 |
|
90 |
|
|
69958 |
|
|
|
|||||
|
5 |
|
|
|
870 |
|
|
|
20 |
|
|
2328 |
|
100 |
|
101080 |
|
|
|
||||||
|
6 |
|
|
|
932 |
|
|
|
25 |
|
|
3165 |
|
150 |
|
486240 |
|
|
|
||||||
|
7 |
|
|
|
1025 |
|
|
|
30 |
|
|
4229 |
|
200 |
|
1549890 |
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Таблица 6 |
|||
|
|
Удельная теплота парообразования воды при разных температурах |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
t, С |
|
0 |
|
|
|
50 |
|
|
|
100 |
|
|
|
200 |
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
r, МДж/кг |
|
|
|
2,49 |
|
|
|
2,38 |
|
|
2,26 |
|
|
|
1,94 |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
177
|
|
|
|
|
|
|
|
|
|
|
|
Таблица 7 |
|
|
|
Свойства некоторых жидкостей (при 20 °С) |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Плотность, |
|
Удельная |
|
|
Поверхностное |
|||||
Вещество |
|
|
теплоемкость, |
|
|||||||||
|
|
103 кг/м3 |
|
|
натяжение, Н/м |
||||||||
|
|
|
Дж/(кг К) |
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Бензол |
|
|
|
0,88 |
1720 |
|
|
|
0,03 |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Вода |
|
|
|
1,00 |
4190 |
|
|
|
0,073 |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Глицерин |
|
|
|
1,20 |
2430 |
|
|
|
0,064 |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Касторовое масло |
|
0,90 |
1800 |
|
|
|
0,035 |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Керосин |
|
|
|
0,80 |
2140 |
|
|
|
0,03 |
|
|||
Ртуть |
|
|
|
13,60 |
138 |
|
|
|
0,5 |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Спирт |
|
|
|
0,79 |
2510 |
|
|
|
0,02 |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Таблица 8 |
|
|
|
|
Свойства некоторых твердых тел |
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
||
Вещество |
|
Плотность |
|
Температура плавления |
|
Удельная теплоемкость |
|
Удельнаятеплота плавления |
|
Температурный коэффициентлинейрасширенияного |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
, 103 кг/м3 |
T, °С |
|
с, Дж/(кг К) |
, кДж/кг |
|
, 10 5 К 1 |
|
|||||
Алюминий |
|
2,6 |
|
659 |
|
896 |
|
322 |
|
2,3 |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
||
Железо |
|
7,9 |
|
1530 |
|
500 |
|
272 |
|
1,2 |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Латунь |
|
8,4 |
|
900 |
|
386 |
|
|
|
|
1,9 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Лед |
|
0,9 |
|
0 |
|
2100 |
|
335 |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
||
Медь |
|
8,6 |
|
1100 |
|
395 |
|
176 |
|
1,6 |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
||
Олово |
|
7,2 |
|
232 |
|
230 |
|
58,6 |
|
2,7 |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
||
Платина |
|
21,4 |
|
1770 |
|
117 |
|
113 |
|
0,89 |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Пробка |
|
0,2 |
|
|
|
2050 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Свинец |
|
11,3 |
|
327 |
|
126 |
|
22,6 |
|
2,9 |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
||
Серебро |
|
10,5 |
|
960 |
|
234 |
|
88 |
|
1,9 |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Сталь |
|
7,7 |
|
1300 |
|
460 |
|
|
|
|
1,06 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Цинк |
|
7,0 |
|
420 |
|
391 |
|
117 |
|
2,9 |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
178 |
|
|
|
|
|
|
|
Таблица 9
Названия, символы и атомные массы химических элементов
1. |
Водород |
Н |
1,0079 |
32. Германий |
Ge |
72,59 |
||
|
|
|
|
|
|
|
|
|
2. |
Гелий |
Не |
4,00260 |
33. |
Мышьяк |
As |
74,9216 |
|
|
|
|
|
|
|
|
|
|
3. |
Литий |
Li |
6,941 |
34. |
Селен |
Se |
78,96 |
|
|
|
|
|
|
|
|
|
|
4. |
Бериллий |
Be |
9,01218 |
35. |
Бром |
Br |
79,904 |
|
|
|
|
|
|
|
|
|
|
5. |
Бор |
В |
10,81 |
36. |
Криптон |
Кг |
83,80 |
|
|
|
|
|
|
|
|
|
|
6. |
Углерод |
С |
12,011 |
37. |
Рубиний |
Rb |
85,467 |
|
|
|
|
|
|
|
|
|
|
7. |
Азот |
N |
14,0067 |
38. |
Стронций |
Sr |
87,62 |
|
|
|
|
|
|
|
|
|
|
8. |
Кислород |
О |
15,9994 |
39. |
Иттрий |
Y |
88,9059 |
|
|
|
|
|
|
|
|
|
|
9. |
Фтор |
F |
18,998403 |
40. |
Цирконий |
Zr |
91,22 |
|
|
|
|
|
|
|
|
|
|
10. |
Неон |
Ne |
20,179 |
41. |
Ниобий |
Nb |
92,9064 |
|
|
|
|
|
|
|
|
|
|
11. |
Натрий |
Na |
22,98977 |
42. |
Молибден |
Vo |
95,94 |
|
|
|
|
|
|
|
|
|
|
12. |
Магний |
Mg |
24,305 |
43. |
Технеций |
Tc |
98,9062 |
|
|
|
|
|
|
|
|
|
|
13. |
Алюминий |
А1 |
26,98154 |
44. |
Рутений |
Ru |
101,07 |
|
|
|
|
|
|
|
|
|
|
14. |
Кремний |
Si |
28,0855 |
45. |
Родний |
Rh |
102,9055 |
|
15. |
Фосфор |
Р |
30,97376 |
46. |
Палладий |
Pd |
106,4 |
|
|
|
|
|
|
|
|
|
|
16. |
Сера |
S |
32,06 |
47. |
Серебро |
Ag |
107,868 |
|
|
|
|
|
|
|
|
|
|
17. |
Хлор |
Cl |
35,453 |
48. |
Кадмий |
Cd |
112,41 |
|
|
|
|
|
|
|
|
|
|
18. |
Аргон |
Ar |
39,948 |
49. |
Индий |
In |
114,82 |
|
19. |
Калий |
K |
39,0983 |
50. |
Олово |
Sn |
118,69 |
|
20. |
Кальций |
Ca |
40,08 |
51. |
Сурьма |
Sb |
121,75 |
|
|
|
|
|
|
|
|
|
|
21. |
Скандий |
Se |
44,9559 |
52. |
Теллур |
Те |
127,60 |
|
|
|
|
|
|
|
|
|
|
22. |
Титан |
Ti |
47,90 |
53. |
Иод |
I |
126,9045 |
|
|
|
|
|
|
|
|
|
|
23. |
Ванадий |
V |
50,9415 |
54. |
Ксенон |
Xe |
131,30 |
|
24. |
Хром |
Cr |
51,996 |
55. |
Цезий |
Cs |
132,9054 |
|
25. |
Марганец |
Mn |
54,9380 |
56. |
Барий |
Ba |
137,33 |
|
|
|
|
|
|
|
|
|
|
26. |
Железо |
Fe |
55,847 |
57. |
Лантан |
La |
138,9055 |
|
|
|
|
|
|
|
|
|
|
27. |
Кобальт |
Co |
58,9332 |
58. |
Церий |
Ce |
140,12 |
|
|
|
|
|
|
|
|
|
|
28. |
Никель |
Ni |
58,71 |
59. |
Празеодим |
Pr |
140,9077 |
|
29. |
Медь |
Cu |
63,546 |
60. |
Неодим |
Nd |
144,24 |
|
30. |
Цинк |
Zn |
65,38 |
61. |
Прометий |
Pm |
[145] |
|
|
|
|
|
|
|
|
||
31. Галий |
Ga |
69,735 |
62. |
Самарий |
Sm |
150,4 |
||
|
|
|
|
|
|
|
|
|
179