9
.docxБилет № 9
-
Поясните 2-ой закон Фарадея и следствия из этого закона.
2-ой закон Фарадея:
Электрохимические эквиваленты веществ прямопропорциональны их химическим эквивалентам.
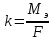 ,
где k
– электрохимический эквивалент, Мэ
– молярная масса эквивалента, F
– число Фарадея.
,
где k
– электрохимический эквивалент, Мэ
– молярная масса эквивалента, F
– число Фарадея.
Следствия из законов Фарадея:
-
Для выделения 1 химического эквивалента вещества при электролизе нужно одно и тоже количество электричества. F = 96496 Кл
m=Mэ
Мэ=I*Ʈ* F=I*Ʈ
Q=I*Ʈ
F=I*Ʈ
Q=I*Ʈ
-
При I*Ʈ=const массы веществ, выделившихся на электродах относятся между собой, как их Мэ.
-
Дайте определение гальванического элемента и поясните его работу.
Если ОВР осуществлять так, чтобы процессы окисления и восстановления были пространственно разделены, и создать возможность перехода электронов от восстановителя к окислителю по проводнику (внешняя цепь), то возникает направленное движение электронов – электрический ток.
Устройства, в которых на электродах самопроизвольно протекают ОВР, в результате которых возникает электрическая энергия, называют гальваническими элементами.
По внутренней цепи происходит обмен ионами.
Электрод, на котором осуществляется процесс окисления, называется анод (его потенциал “-”). Другой электрод – катод (его потенциал “+”).
Гальванический элемент – замкнутый контур.
Электрическая энергия, получаемая с помощью гальванического элемента, будет максимальна, когда элемент работает в условиях наиболее близких к обратимым.
Максимальная разность потенциалов данного гальванического элемента называется его электродвижущей силой (ЭДС). ЭДС=(станд.усл.)ɥ0К - ɥ0А
Уравнение Нернста
Δ
ɥх.р.=
Δ
ɥ0х.р.
+
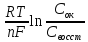 ,
где n
– число электронов в ОВР, F
– число Фарадея
,
где n
– число электронов в ОВР, F
– число Фарадея
Для металлов уравнение приобретает вид:
Δ
ɥ Men+/Me0
=
Δ
ɥ0Men+/Me0
+
 ,
где Т стандартная,
,
где Т стандартная,
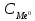 =1моль/л
=1моль/л
Для осуществления процессов ОВР обычно используют катализатор – электрод, который является одновременно проводником электронов , например Pt.
-
Поясните постулаты Дальтона (АМУ).
Основные положения атомно-молекулярного учения:
-
Каждый элемент является совокупностью более мелких частиц – атомов.
-
Все атомы химического элемента одинаковы по химическим свойствам.
-
Атомы различных элементов обладают различными свойствами, в том числе имеют разные массы.
-
Атомы одного элемента не превращаются в атомы другого элемента в условиях химических реакциях.
-
Химические соединения образуются в результате объединения атомов 2-х или более элементов.
-
В данном соединении относительные количества атомов различных элементов всегда постоянно.
Для постулатов Дальтона существуют исключения. Постулат №2 несправедлив для изотопов (например, изотопы водорода: Протий — 1H,
Дейтерий (D) — 2H, Тритий (T) — 3H), постулат № 3 – для изобаров (нуклиды разных элементов, имеющие одинаковое массовое число; например, изобарами являются 40Ar, 40K, 40Ca). Исключением для постулата № 4 является трансмутация, а постулат № 6 справедлив только для веществ-дальтонидов (исключения – бертоллиды).
-
Рассчитайте изменение изобарно-изотермического потенциала энергии Гиббса в реакции: MnO2(ТВ) + 4HCl(г) ® MnCl2(p) + Cl2(г) +2H2O(ж)
MnO2(ТВ) + 4HCl(г) ® MnCl2(p) + Cl2(г) +2H2O(ж)
ΔG0(MnCl2 p)=-440,0 кДж/моль
ΔG0(2H2O ж)=2*(-237,2) кДж/моль
ΔG0(Cl2)=0, т.к. это простое вещество
ΔG0(MnO2 тв)=-466,7 кДж/моль
ΔG0(4HCl2 г)=4*(-94,8) кДж/моль
ΔG0х.р.=(-440,0+(-474,4)+0)-(-466,7+(-379,2))=-68,5 кДж/моль
ΔG0 <0 → разрешена прямая реакция
-
Подсчитайте массу газа Н2 в объеме 100 л при давлении 5 ат. И температуре 80оС.
Из закона
Менделеева-Клапейрона
 следует, что
следует, что
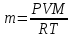
P=0,5 мПа
V=0,1 м3 T=353 К