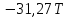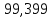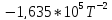4. Расчет изменения энтальпии
Изменение энтальпии реакции (1). В расчете учитываем, что в температурном интервале 300 – 750 К протекают две реакции (2) и (3). Это позволяет общее уравнение (4) представить двумя частями:
 (6)
(6)
для интервала 300 – 570 К. Уравнение (6) описывает широкий интервал температур, начиная со стандартной температуры.
 (7)
(7)
для
интервала 570
– 750 К. В равенстве (7) эффект фазового
превращения тетрахлорида тантала
вычитается, так как это вещество
является исходным. Видно, что необходимо
определить
 :
:




Представляем расчет таблицей 3 и графиком (рисунок 2)
Таблица
3 – Расчетные значения
 реакции(1)
реакции(1)
|
T, K |
|
|
|
|
|
|
300 |
130153,17 |
3864,000 |
1526,400 |
-1090,000 |
134453,570 |
|
325 |
130153,17 |
4186,000 |
1791,400 |
-1006,154 |
135124,416 |
|
350 |
130153,17 |
4508,000 |
2077,600 |
-934,286 |
135804,484 |
|
364 |
130153,17 |
4688,320 |
2247,132 |
-898,352 |
136190,271 |
Продолжение таблицы 3
|
T, K |
|
|
|
|
|
|
364 |
118431,61 |
-11382,280 |
1681,109 |
-3140,110 |
105590,329 |
|
375 |
118431,61 |
-11726,250 |
1784,250 |
-3048,000 |
105441,610 |
|
400 |
118431,61 |
-12508,000 |
2030,080 |
-2857,500 |
105096,190 |
|
425 |
118431,61 |
-13289,750 |
2291,770 |
-2689,412 |
104744,218 |
|
450 |
118431,61 |
-14071,500 |
2569,320 |
-2540,000 |
104389,430 |

Рисунок 2 – Зависимость изменения энтальпии реакции (1) от температуры
Т.к.
 до температуры фазового перехода, то
до температуры фазового перехода, то
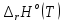 будет возрастать на этом промежутке.
после фазового перехода
будет возрастать на этом промежутке.
после фазового перехода
 и
и
 будет убывать.
будет убывать.
5. Расчет изменения энтропии
Изменение энтальпии реакции (1). И опять учитываем, что в температурном интервале 300 – 450 К протекают две реакции (2) и(3), поэтому изменение энтропии будем считать по двум уравнениям:
 (8)
(8)
для интервала 300 – 364 К.
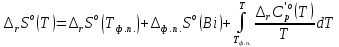 (9)
(9)
для
интервала 364
–
450 К. Определяем
 :
:




Расчет по уравнениям (8) и (9) представим таблицей 4 и графиком (рисунок 3).
Таблица
4 – Расчетные значения
 реакции
(III)
реакции
(III)
|
T, K |
|
|
|
|
|
|
300 |
99,399 |
73,465 |
10,175 |
-1,817 |
181,222 |
|
325 |
99,399 |
74,496 |
11,022 |
-1,548 |
183,369 |
|
350 |
99,399 |
75,450 |
11,870 |
-1,335 |
185,385 |
|
364 |
99,399 |
75,955 |
12,345 |
-1,234 |
186,465 |
Продолжение таблицы 3
|
T, K |
|
|
|
|
|
|
364 |
281,872 |
-184,404 |
9,237 |
-4,313 |
102,391 |
|
375 |
281,872 |
-185,335 |
9,516 |
-4,064 |
101,989 |
|
400 |
281,872 |
-187,353 |
10,150 |
-3,572 |
101,097 |
|
425 |
281,872 |
-189,249 |
10,784 |
-3,164 |
100,244 |
|
450 |
281,872 |
-191,036 |
11,419 |
-2,822 |
99,432 |

Рисунок 3 - Зависимость изменения энтропии реакции (1) от температуры
Сравним графики рисунков 2 и 3. Видим, что поведение обеих функций при изменении температуры подобно. Так и должно быть, так как обе функции описываются изменением теплоемкости реакции.