
- •Свойства высокомолекулярных соединений и их растворов. Практическая значимость темы
- •Классификация полимеров
- •Биополимеры
- •Особые свойства вмс
- •Свойства растворов вмс.
- •Природа растворов вмс.
- •Свойства растворов вмс общие с истинными растворами нмс
- •Свойства растворов вмс общие с коллоидными растворами
- •Особые свойства растворов вмс
- •Вязкость растворов вмс
- •Осмотическое давление растворов вмс.
- •Защитное действие вмс в коллоидных растворах.
- •Коацервация
- •Свойства растворов полиэлектролитов.
- •Изоэлектрическое состояние
- •Свойства растворов белков в изоэлектрическом состоянии.
- •Электрофорез.
- •Факторы, влияющие на электрофоретическую подвижность
- •Методы электрофореза
- •Зональный электрофорез
- •Применение электрофореза
Методы электрофореза
Существует множество разновидностей и модификаций метода электрофореза, которые используются в различных областях.
Выделяют три основных типа электрофоретических систем: электрофорез с подвижной границей, зональный электрофорез и стационарный (вытесняющий) электрофорез.
Электрофорез белков подразделяется также на одномерный и двумерный, препаративный и аналитический, а также электрофорез нативных белков. В случае использования иммунологических методов для выявления разделенных белков используется иммуноэлектрофорез.
Зональный электрофорез
В случае зонального электрофореза смешивание разделенных зон может быть предотвращено. При этом методе разделение производят в закрепленной среде. Наиболее распространены методы разделения на пористых носителях.
Электрофорез на бумаге. Электрофорез проводят с использованием боратных, фосфатных или веронал-мединаловых буферных растворов. Носителем служит специальная хроматографическая бумага, которую разрезают на полоски требуемого размера. Наносят сыворотку крови на катодный конец смоченной буферным раствором полоски. В зависимости от типа прибора и условий опыта электрофорез на бумаге длится от 4 до 16 часов. Скорость движения белков пропорциональна величине их электрического заряда. За определенное время белковые фракции пройдут различный путь и разделятся.

Схема прибора для электрофореза на бумаге.
З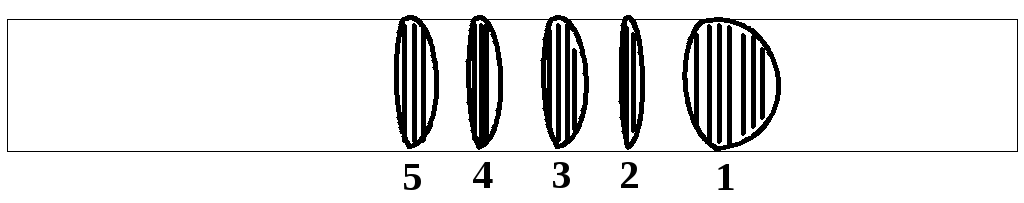 атем
белки фиксируют высушиванием и красят
красителями. Окрашенные зоны белковых
фракций вырезают и элюируют специальным
растворителем (растворNaOH)
для фотометрического определения каждой
фракции. При электрофорезе на бумаге
белков сыворотки крови получается до
5 фракций: альбумины, 1-,
2-,
-,
-глобулины.
атем
белки фиксируют высушиванием и красят
красителями. Окрашенные зоны белковых
фракций вырезают и элюируют специальным
растворителем (растворNaOH)
для фотометрического определения каждой
фракции. При электрофорезе на бумаге
белков сыворотки крови получается до
5 фракций: альбумины, 1-,
2-,
-,
-глобулины.
Электрофореграмма сыворотки крови на хроматографической бумаге:
1 – альбумин, 2 – 1-глобулин, 3 – 2-глобулин, 4 – -глобулин, 5 – -глобулин.
Электрофорез на ацетатцеллюлозной мембране. Мембрана ацетатцеллюлозы как носитель для электрофореза имеет ряд преимуществ по сравнению с бумагой: однородность, строго определенный размер пор, пониженная адсорбционная способность, что исключает образование размытых полос позади зон. Для окрашивания зон применяют методы аналогичные методам окрашивания зон на бумаге.
Э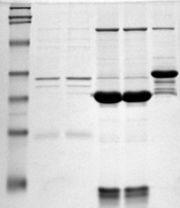 лектрофорез
в гелях.
В этом методе в качестве опорной среды
используют крахмальный, агар-агаровый,
полиакриламидный гели. Характерной
особенностью этой разновидности
зонального электрофореза является его
высокая разрешающая способность,
поскольку гели функционируют как
молекулярные сита: крупные молекулы
проходят сквозь него тем медленнее, чем
меньше размер пор в геле. Методом
электрофореза в агаровом геле в сыворотке
крови выявляется до 7-8 фракций, а при
электрофорезе в крахмальном или
полиакриламидном геле – до 20 фракций.
Агаровый гель ввиду большого количества
воды в нем и вследствие этого большой
скорости движения ионов используется
в иммуноэлектрофорезе для обнаружения
антигенов. Самым перспективным является
полиакриламидный гель, так как он
прозрачен, обладает значительной
механической прочностью, однороден по
составу, химически инертен, размер пор
у этого геля можно варьировать в широких
пределах и его можно использовать с
самыми различными буферными растворами.
Скорость движения белков пропорциональна
их заряду и молекулярной массе.
лектрофорез
в гелях.
В этом методе в качестве опорной среды
используют крахмальный, агар-агаровый,
полиакриламидный гели. Характерной
особенностью этой разновидности
зонального электрофореза является его
высокая разрешающая способность,
поскольку гели функционируют как
молекулярные сита: крупные молекулы
проходят сквозь него тем медленнее, чем
меньше размер пор в геле. Методом
электрофореза в агаровом геле в сыворотке
крови выявляется до 7-8 фракций, а при
электрофорезе в крахмальном или
полиакриламидном геле – до 20 фракций.
Агаровый гель ввиду большого количества
воды в нем и вследствие этого большой
скорости движения ионов используется
в иммуноэлектрофорезе для обнаружения
антигенов. Самым перспективным является
полиакриламидный гель, так как он
прозрачен, обладает значительной
механической прочностью, однороден по
составу, химически инертен, размер пор
у этого геля можно варьировать в широких
пределах и его можно использовать с
самыми различными буферными растворами.
Скорость движения белков пропорциональна
их заряду и молекулярной массе.
Фотография электрофореграмм смеси белков, разделенных в полиакриламидном геле, иллюстрирующая разделение белков по заряду и молекулярной массе.
В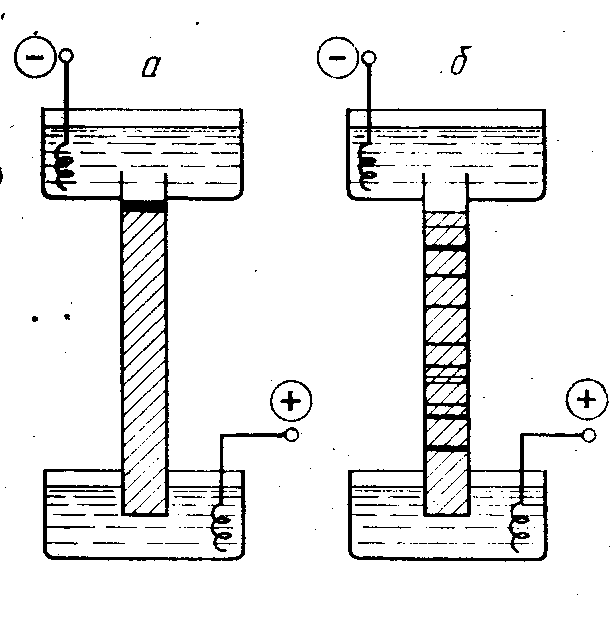 ариантов
проведения электрофореза в полиакриламидном
геле много (вертикальный в трубках и
горизонтальный на пластинах).
ариантов
проведения электрофореза в полиакриламидном
геле много (вертикальный в трубках и
горизонтальный на пластинах).
|
Схема простейшего прибора для электрофореза в геле а - до фракционирования, б - после его окончания |
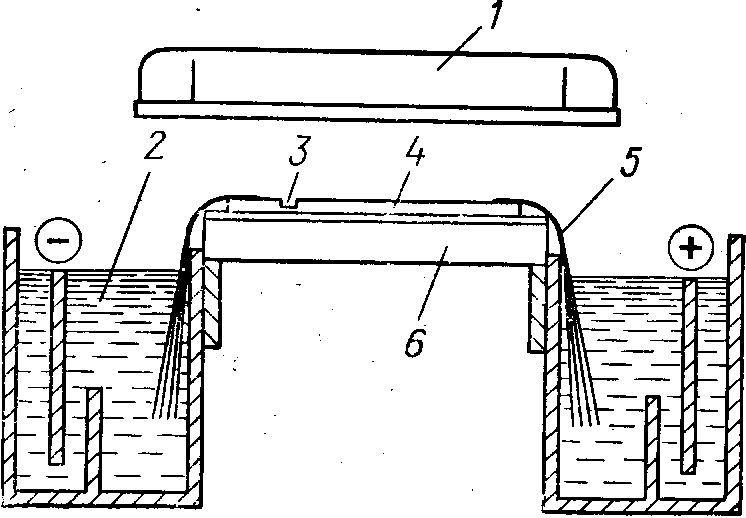
Схема прибора для электрофореза в горизонтальных пластинах 1-антиконденсационная крышка; 2 – электродный резервуар; 3 - колодец для внесения препарата; 4 - гель; 5 - фитиль; 6-охлаждающий столик |
Вытеснительный электрофорез.
Этот метод характеризуется тем, что через некоторое время после разделения зон устанавливается состояние равновесия, при котором ширина зон в дальнейшем не изменяется. К электрофорезу такого типа относятся изоэлектрическое фокусирование.
Изоэлектрическое фокусирование. Это метод разделения белков, основанный на перемещении их молекул под действием постоянного электрического тока в область с величиной рН, соответствующей изоэлектрической точке данного белка. Между анодом и катодом создается градиент рН с помощью амфолитов. Каждый белок мигрирует к соответствующему электроду и прекращает движение, попадая в зону с pH = pJ (фокусируется). Таким образом, молекулы, имеющие одинаковую изоэлектрическую точку, сконцентрируются в узкой зоне.
