
2344 - Пустов Ю.А., Ракоч А.Г. - Коррозионностойкие и жаростойкие материалы - 2013
.pdfТаблица 4.2
Методы испытаний коррозионностойких сталей на склонность к МКК по межгосударственному стандарту ГОСТ 6032–2003 (взамен ГОСТ 6032–89),
международным стандартам ИСО 3651-1:1998 и ИСО 3651/2–98 и стандарту ASTM A262–81 (США)
Метод |
|
|
|
|
|
|
|
по |
Состав электролита |
Международные |
Состав электролита |
||||
ГОСТ |
|||||||
и режим испытаний |
аналоги |
и режим испытаний |
|||||
6032– |
|||||||
|
|
|
|
|
|
||
2003 |
|
|
|
|
|
|
|
|
|
|
Кипячение в растворе 70 |
||||
|
Кипячение в растворе 50 г/дм3 CuSO4+ |
А |
г/дм3 CuSO4·5H2O + |
||||
|
+ 250 см3/дм3 H2SO4 |
+ 100 см3/дм3 H2SO4 |
|||||
АМУ |
(d = 1,84 г/см3). |
ИСО 3651-1:1998 |
(плотность d = 1,84 г/см3). |
||||
В раствор добавляют |
Метод |
В раствор добавляют |
|||||
|
Монипени- |
||||||
|
медную стружку. |
медную стружку. |
|||||
|
Штрауса |
||||||
|
Время испытаний – 8 ч |
Время испытаний |
|||||
|
|
||||||
|
|
|
(20 ± 5) ч |
|
|
||
|
|
|
Выдержка при |
||||
|
|
|
20…30 ºС в растворе |
||||
|
Выдержка при 20…30 ºС |
|
50 г/дм3 |
3 |
|
||
|
|
CuSO4 + 128 |
г/дм |
NaF |
|||
|
3 |
|
|
||||
|
в растворе 50 г/дм |
|
|
3 |
|
|
|
|
3 |
|
(или 177 г/дм KF) + |
||||
|
CuSO4 + 128 г/дм NaF |
|
3 |
3 |
|
|
|
АМУФ |
(или 177 г/дм3 KF) + 250 см3/дм3 H2SO4. |
ИСО 3651-1:1998, |
+ 250 см /дм H2SO4. |
||||
В раствор добавляют медную стружку. |
ИСО 3651-2:1998 |
В раствор добавляют |
|||||
|
Продолжительность испытаний |
|
медную стружку. |
||||
|
|
Продолжительность |
|||||
|
для сталей без молибдена 2 ч, |
|
|||||
|
|
испытаний для сталей |
|||||
|
для сталей с молибденом 3 ч |
|
|||||
|
|
без молибдена 2 ч, |
|||||
|
|
|
|||||
|
|
|
для сталей |
|
|
||
|
|
|
с молибденом 3 ч |
||||
|
|
|
Кипячение в растворе |
||||
|
|
|
110 г/дм3 CuSO4 + |
||||
|
|
В |
+ 35%-ной H2SO4 |
||||
– |
– |
|
|
|
3 |
||
ИСО 3651-2:1998 |
(плотность d=1,84 г/см ). |
||||||
|
|
|
В раствор добавляют |
||||
|
|
|
медные опилки. |
||||
|
|
|
Время испытаний (20±5) ч |
||||
|
Кипячение в растворе 110 г/дм3 |
|
|
|
|
|
|
|
CuSO4 + 55 см3/дм3 H2SO4. |
− |
– |
|
|
|
|
В |
В раствор добавляют цинковую |
|
|
|
|||
|
пыль (5 г/дм3 раствора). |
|
|
|
|
|
|
|
Время испытаний 144 ч |
|
|
|
|
|
|
|
|
|
Кипячение в растворе |
||||
|
Кипячение в растворе 50%-ной H2SO4 |
С |
49 % H2SO4 + 25 г/дм3 |
||||
ВУ |
+ 40 г/дм3 Fe2(SO4)3. |
Fe2(SO4)3. |
|
|
|||
|
Время испытаний 48 ч |
ИСО 3651-2:1998 |
Время испытаний |
||||
|
|
||||||
|
|
|
(20 ± 5) ч |
|
|
||
|
|
|
|
|
|
|
|
111
|
|
|
Окончание табл. 4.2 |
|
|
|
|
|
|
Метод |
|
|
|
|
по |
Состав электролита |
Международные |
Состав электролита |
|
ГОСТ |
||||
и режим испытаний |
аналоги |
и режим испытаний |
||
6032– |
||||
|
|
|
||
2003 |
|
|
|
|
|
|
|
Кипячение в растворе |
|
ДУ |
Кипячение в растворе 65%-ной |
ИСО 3651-1:1998 |
65%-ной (масс.) HNO3; |
|
|
(масс.) HNO3; 5 циклов по 48 ч |
|
5 циклов по 48 ч |
|
|
|
|
(испытания по Хью) |
|
|
Анодное растворение в растворе |
|
Электролитическое |
|
|
65%-ной H2SO4 + 0,5%-ного |
|
травление в 10%-ной |
|
|
уротропина (СН2)6N 4 |
А |
H2C2O4. |
|
Б |
или другого ингибитора серной |
(ASTM A262–81, |
Плотность тока |
|
|
кислоты. |
стандарт США) |
i = 0,65 А/см2. |
|
|
Плотность тока i = 0,65 А/см2. |
|
Время травления |
|
|
Время испытаний 5 мин |
|
1,5 мин |
|
|
|
|
Кипячение при 70 °С |
|
− |
− |
D |
в растворе 10 % HNO3 + |
|
|
|
|
+ 3 % HF |
Примечание. Буквенные обозначения А, Б, В, Д, С, D – буквенные обозначения методов; М – присутствие в растворе для испытаний металлической меди; Ф – присутствие в растворе для испытаний иона фтора; У – ускоренные испытания.
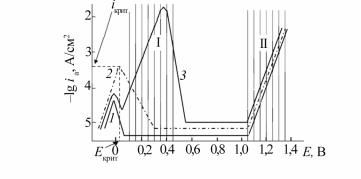
Используемые для испытаний растворы с определенными окисли- тельно-восстановительными потенциалами позволяют проводить испы- тания на МКК сталей, находящихся в различных состояниях: активного растворения, переходной области потенциалов, пассивности и перепасси- вации (рис. 4.6).
Рис. 4.6. Анодные поляризационные кривые стали Х18Н10Т в закаленном, не склонном к МКК (1) и сенсибилизированном, склонном к МКК (2, 3)
состояниях (температура 22 оС):
1, 3 – раствор HClO4 (1 моль/л) + NaCl (0,4 моль/л); 2 – раствор Н2SO4 (1 моль/л)
112
Методы АМУ, АМУФ и методы, рекомендуемые международ-
ными стандартами ИСО 3651-1:1998 и ИСО 3651-2:1998, распро-
страняются на широкий ассортимент ферритных, аустенитных и ау- стенитно-ферритных коррозионностойких сталей, включая такие, как
08Х17Т, 15Х25Т, 0817Н7М3, 08Х18Н10, 08Х18Н10Т, 03ХН12, 08Х18Н12Т, 08Х18Н12Б, 20Х13Н4Г9, 09Х17Н7Ю, 08Х18Г8Н2Т, 12Х18Н9, 12Х18Н12Т.
Окислительно-восстановительный потенциал растворов, приме- няемых в этих методах, близок к 0,35 В (по н.в.э.), что отвечает ус- тойчивой пассивности центральных участков зерен и преимущест- венному растворению периферийных зон. Ионы Cu2+, участвующие в катодном процессе, сопутствующем растворению, восстанавлива- ются до Cu+. Последние накапливаются в растворе. Окисление Cu+ кислородом практически исключено, так как длительное кипячение приводит к практически полному удалению растворенного воздуха. Скорость МКК зависит от соотношения концентрации этих ионов [Сu+/Cu2+], влияющего на окислительно-восстановительный потен- циал среды. Наиболее жесткие условия для развития МКК создаются при низких значениях этого потенциала (0,1 В), который достигается
введением медной стружки. На поверхности стружки протекает про-
цесс Cu2+ + e = Cu+.
В методе В, используемом для испытаний высоколегирован- ных сталей 03Х21Н21М4ГБ, 06Х28МДТ, 03Х28МДТ, применяют тот же принцип стимуляции МКК, но вместо меди в раствор вво-
дят цинковую пыль. Это приводит к глубокому восстановлению ионов Сu2+: Zn + CuSO4 = Cu + ZnSO4; Cu (катод)/Сu2+ (из раство-
ра) + e = Cu+. Кроме того, стальные образцы, находящиеся в кон- такте с растворяющимся в кислоте цинком, испытывают катод- ную поляризацию.
При обработке по методам ВУ и С окислительно- восстановительный потенциал раствора, определяющийся равно- весием Fe3+/Fe2+, составляет 0,7…1,0 В (по н.в.э.) и соответствует пассивной области и переходу к перепассивации. Большие поте- ри массы образцов, наблюдаемые при испытании сталей этим методом, связаны с выпадением зерен в местах проявления МКК. Для некоторых сталей возможно селективное растворение σ-фазы. В связи с тем что во время испытаний имеет место ка- тодное восстановление ионов Fe3+ до Fe2+ и накопление послед- них в растворе, окислительно-восстановительный потенциал рас- твора смещается в отрицательную сторону и растворение стали
113
происходит в активной области. Следует отметить, что испыта- ния обеспечивают качественный контроль и могут быть исполь- зованы для определения чувствительности материалов к МКК после проведения термообработки.
Интенсивность МКК в методах ДУ и испытаний по Хью ха-
рактеризуется потерей массы образцов. Образцы взвешивают по- сле каждой стадии испытаний и рассчитывают скорость коррозии (как скорость проникновения, мм/год) для каждой стадии и уско- ренную для всех пяти циклов. Проведение процесса в несколько циклов объясняется реакцией образования ионов Cr6+. При окис- лении Cr2+ и Cr3+ азотной кислотой и последующем накоплении ионов Cr6+ заметно увеличивается агрессивность раствора, так что интенсивная МКК с выпадением растравленных зерен может развиваться даже в сталях, свободных от выделения карбидов. Поэтому возникает необходимость периодической замены рас- твора и поддержания минимального отношения объема раствора
кплощади поверхности образца: 9 см3/1 см2 (ДУ) и 20 см3/1 см2 (С). Считают, что если скорость коррозии на последующей ста- дии увеличивается по сравнению с предыдущей, то сплав являет- ся чувствительным к МКК. При этом после любого цикла испы- таний скорость коррозии должна превышать 0,5 мм/год. Потен- циал металла при этих испытаниях находится в пределах 0,8…1,6 В (разброс значений обусловлен влиянием примесей, например, хромат-ионов), что соответствует потенциалу перепассивации. Предполагают, что высокие скорости коррозии, получаемые при этих испытаниях, обусловлены частично межкристаллитной кор- розией, частично постоянным вытравливанием и выпадением зе- рен и богатых хромом и особенно молибденом соединений – кар-
бидов и σ-фазы Fe–Cr–(Mo).
Методы Б (ГОСТ 6032–2003) и А (ASTM A262–81) могут быть условно рассмотрены в этом разделе, так как они являются электро- химическими и могут быть использованы для оценки склонности
кМКК готовых изделий.
Вметоде Б выбранный участок поверхности (рис. 4.7) подверга- ют анодному травлению, после чего поверхность промывают водой, протирают фильтровальной бумагой и просматривают под микро- скопом при увеличении не менее чем в 30 раз.
Критерием склонности к МКК является наличие сетки непрерыв- ных нарушений в областях анодного травления.
114
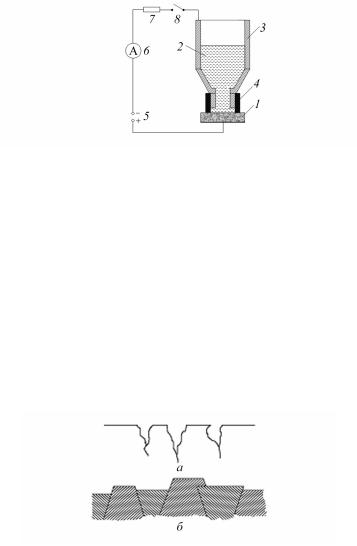
Рис. 4.7. Установка для определения склонности коррозионностойких сталей
кМКК электрохимическим методом Б:
1– образец; 2 – электролит; 3 – свинцовый сосуд; 4 – резиновая манжета; 5 – источник постоянного тока; 6 – амперметр; 7 – сопротивление;
8 – ключ замыкания цепи
Метод А (ASTM A262–81) применяется как предварительное сор- тировочное испытание в комплексе с более длительными испыта- ниями в кипящей азотной кислоте. Образующуюся после анодного травления структуру рассматривают под микроскопом при × 500
иклассифицируют как «ступенчатую», «ямочную» (с растравленны- ми границами зерен) или «двойную» (состоящую из «ступенчатой»
и«ямочной»). Если на поверхности обнаруживается «ступенчатая» структура (рис.4.8), то сплав нечувствителен к МКК и нет необходи- мости проводить дальнейшие испытания.
Рис. 4.8. «Ямочная» (а) и «ступенчатая» (б) структуры поверхности испытуемых образцов
В случае образования «ямочной» структуры (рис. 4.8, а) для вы- явления МКК следует использовать химические методы. Необходи- мость применения химических методов возникает и при образовании «двойной» структуры.
115
«Ямочная» структура, характерная для сплавов, чувствительных к МКК, образуется вследствие более высокой скорости растворения границ зерен по сравнению со скоростью растворения тела зерна. «Ступенчатая» структура объясняется различием в скоростях раство- рения различным образом ориентированных кристаллографических плоскостей. «Двойная» структура возникает в том случае, когда кар- биды хрома располагаются по границам зерен в виде отдельных включений, не образуя непрерывных сеток.
Испытания по методу D состоят из двух двухчасовых периодов выдержки, причем для каждого периода используют свежеприготов- ленный раствор. Эти испытания являются более быстрыми по срав- нению с другими и специфическими по отношению только к обед- ненным хромом границам зерен, так как не оказывают влияния на субмикроскопическую σ-фазу, присутствующую в сталях, содержа- щих молибден.
Раствор для испытаний имеет низкий окислительно- восстановительный потенциал и в зависимости от состава сталей (ау- стенитного класса) потенциал коррозии будет находиться в пределах 0,14…0,54 В. Поэтому стали с высоким содержанием хрома могут на- ходиться в области активного растворения, что приводит к значитель- ному растворению границ зерен по сравнению с центральными участ- ками зерен, которые могут оставаться запассивированными. Так как скорости коррозии сталей в этой смеси кислот очень высоки и сильно меняются от испытания к испытанию, то возникает необходимость в проведении двух испытаний для сопоставления скоростей коррозии образца, который изучается, и образца того же сплава, но после обра- ботки, предотвращающей выделение карбидов.
Испытания по методу D очень надежны, но применяются на прак- тике довольно редко из-за необходимости использования двух образ- цов в различном состоянии и высокой токсичности раствора. По этим причинам аналогичный метод, когда-то входивший в ГОСТ испыта- ний сталей на МКК, в настоящее время в России не применяют.
Для визуального обнаружения и оценки склонности к МКК после выдержки в растворах (для всех методов, кроме ДУ и В) образцы из- гибают на 90° в соответствии с ГОСТ 14019–80.
Радиус закругления r оправки для аустенитных сталей не должен превышать толщины образца h. При h < 1 мм допускается r = 1 мм. Значение r для ферритных, аустенитно-мартенситных и аустенитно- ферритных сталей, а также отливок из аустенитных сталей должны быть равны соответственно: r = 3 мм при h ≤ 1 мм; r ≤ 3 h при
116
h = 1…3 мм; r = 10 мм при h > 3 мм. Для ферритных сталей r = 3 h при h > 3 мм.
Если толщина образцов не превышает 5 мм, проверяют обе по- верхности, придавая образцу Z-образную форму. Показателем стой- кости к МКК является отсутствие трещин. Если изгиб невозможен или трещины присутствуют и на контрольных образцах, стойкость к МКК оценивают металлографически. Наличие и глубину МКК ус- танавливают на поперечных шлифах, которые подвергают электро- химическому травлению в соответствующих электролитах по ГОСТ 6032–2003 и рассматривают при увеличении не менее чем в 200 раз. Признак МКК – разрушение границ не менее чем на 30 мкм. Для от- дельных марок сталей разработан ряд усовершенствованных химиче- ских методов контроля на склонность к МКК, предусматривающих проведение испытаний с меньшей продолжительностью (табл. 4.3).
Таблица 4.3
Ускоренные химические методы испытаний некоторых коррозионностойких сталей на склонность к МКК
Метод |
Состав электролита |
Марка стали |
|
и режим испытаний |
или сплава |
||
|
|||
Модифицированный |
50%-ный раствор H2SO4 + |
|
|
метод ДУ (добавка |
+ 40 г/л Fe2(SO4)3 + 9 г/л HF; |
06Х28МДТ, |
|
в испытательный |
перемешивание в течение 12 ч |
03Н28МДТ |
|
раствор HF) |
при 75…80 оС |
|
|
Модифицированный |
35%-ный раствор H2SO4 + |
|
|
+ 50 г/л CuSO4·5H2O; |
|
||
метод АМУ (повышение |
10Х18Н10Т, |
||
кипячение в растворе |
|||
концентрации H2SO4 |
06Х18Н10Т |
||
(с добавлением медной стружки) |
|||
в испытательном растворе) |
|
||
в течение 4 ч |
|
||
|
|
||
|
5%-ный раствор HNO3 + |
Стали типа |
|
Испытание в смеси кислот |
+ 260 см3/дм3 HCl (d = 1,19 г/см3) + |
||
|
+ 20 г/дм3 FeCl3·6H2O |
Х18Н10Т |
Примечание. Критерий склонности к МКК – наличие трещин на поверхности об- разца, изогнутого на 90о (ГОСТ 6032–2003).
Ускоренные испытания на склонность алюминиевых сплавов к МКК проводят по ГОСТ 9.021–74 в растворе 3 % NaCl + 1 % HCl (d = 1,2 г/см3) при 18…25 °С в течение 24 ч. Кроме того, могут быть использованы следующие режимы:
1)6%-ный раствор NaCl +1%-ный раствор H2O2, погружение при 30 °С, 6 ч;
2)3%-ный раствор NaCl, переменное погружение: 10 мин – выдержка
вэлектролите; 50 мин – на воздухе; время испытаний – 20 сут.
117
4.4.2. Электрохимические методы испытаний на устойчивость к межкристаллитной коррозии
Традиционные стандартные химические методы, основанные на длительном кипячении образцов в растворах, предусмотренных ГОСТ 6032–2003, дают надежную информацию о склонности сталей и сплавов к МКК. Эти методы просты и удобны для массовых испы- таний. Вместе с тем стандартные химические методы обладают ря- дом существенных недостатков: значительной продолжительностью испытания (8…240 ч); недостаточной объективностью при использо- вании в качестве критерия склонности к МКК наличия трещин при изгибе образца; качественным характером оценки результатов испытаний (за исключением металлографического определения глу- бины МКК, которое в заводских условиях применяется крайне ред- ко); возможность оценки качества образцов, а не готовых изделий; использование кипящих растворов, в том числе высококонцентриро- ванных кислот.
Фундаментальные электрохимические исследования позволили разработать ускоренные методы определения склонности сталей и сплавов к МКК и сформулировать основные принципы разработки растворов для проведения испытаний. Было показано, что скорость МКК существенно зависит от потенциала. Наиболее интенсивно процесс разрушения нержавеющих сталей развивается в двух облас- тях (см. рис. 4.6): I – при потенциалах, соответствующих переходу из активного в пассивное состояние; II – при потенциалах, соответст- вующих концу пассивной области и области перепассивации. При эксплуатации в слабоокислительных растворах стали имеют по- тенциалы, отвечающие области I, что соответствует испытаниям по методам АМ, АМУ и В (ГОСТ 6032–2003). В области II потенциалы коррозии сталей устанавливаются при испытании их методом ДУ,
атакже при эксплуатации в сильноокислительных растворах.
Впереходной области (I) реализуются условия, при которых тело зерна пассивно и растворяется с незначительной скоростью, а пери- ферийные (приграничные) зоны в связи с более низкой концентраци- ей хрома (в твердом растворе) находятся в активном или частично запассивированном состоянии и растворяются с высокой скоростью. Поэтому в указанной области потенциалов электрохимическое пове- дение стали, склонной к МКК, значительно отличается от поведения стали, устойчивой к такому виду разрушения. Это проявляется в воз- растании плотности анодного тока растворения (в том числе плотно- сти критического тока пассивации), смещении в более положитель-
118
ную сторону критического потенциала пассивации и потенциала на- чала пассивации (см. рис. 4.6). Для переходной области потенциалов обычно характерна высокая скорость проникновения МКК.
При использовании растворов, смещающих потенциал в область перепассивации (II) наблюдается значительное ускорение МКК. В этой области стали разрушаются и в закаленном состоянии, но
сменьшей скоростью, чем в отпущенном.
Внастоящее время разработано большое число методов оценки устойчивости коррозионностойких сталей к МКК, использующих один или несколько электрохимических критериев: плотность анод- ного тока при постоянном потенциале переходной области; количе- ство электричества, затрачиваемое при переходе из пассивного со- стояния в активное (площадь реактивационнйо петли) и наоборот, а также отношение этих количеств электричества; форма потенцио- динамической кривой, особенно кривой обратного хода; форма кри- вой изменения плотности анодного тока во времени при постоянном потенциале пассивной области; потенциал реактивации; время, необ- ходимое для реактивации; потенциал коррозии; появление активаци- онного участка на анодной потенциодинамической кривой при по- тенциалах, соответствующих переходной области из активного в пас- сивное состояние и др.
Вприл. 2 представлены электрохимические методы оценки ус- тойчивости некоторых сталей и сплавов к МКК, используемые для замены стандартных химических методов испытаний, рекомендуе- мых ГОСТ 6032–2003. Некоторые из электрохимических методов рекомендованы к использованию ГОСТ 9914–91.
Наиболее перспективными являются методы потенциостатическо- го травления (прил.2, пп. 1–4), максимально приближенные к требо- ваниям ГОСТ 6032–2003, и позволяющие проводить экспрессную качественную и количественную оценку склонности к МКК. Исполь-
зование высокоэффективного электролита на основе смеси HClO4 + NaCl (вариант 1 метода ПТ) обеспечивает удачное сочетание
пассивирующего действия ClO 4− на зерно и депассивирующего дей-
ствия иона Cl– на обедненные пограничные зоны. При потенциалах, отвечающих переходной области, на склонных к МКК образцах про- исходит интенсивное развитие питтинга, благодаря чему МК- разрушение проникает вглубь образца с высокой скоростью уже при комнатной температуре.
Активирующее действие ионов Cl–, вызывающее появление пит- тингов по границам зерен и МК-разрушение, проявляется в серно-
119
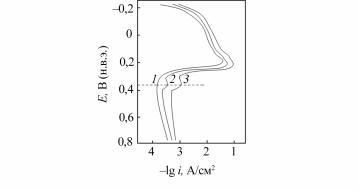
кислом электролите (вариант 4 метода ПТ). При снятии анодной по- тенциодинамической кривой в интервале потенциалов 0,3…0,4 В (по нормальному хлорсеребряному электроду) обнаруживается акти- вационный участок (рис. 4.9), при этом максимальное значение анод- ного тока отвечает потенциалу 0,36 В. Увеличение склонности к МКК характеризуется возрастанием тока.
Рис. 4.9. Андные потенциодинамические кривые (1,4 В/ч) сплава
06Х28МДТ в растворе 50%-ного H2SO4 + 1 н. NaCl:
1 – закаленное состояние; 2, 3 – отпуск при 700 ºС в течение 20 мин и 10 ч соответственно
Потенциостатический реактивационный метод основан на сня- тии анодной потенциодинамической кривой обратного хода. Для склонных к МКК сталей наблюдается ярко выраженная акти- вация в виде анодной петли (рис. 4.10, а, б). У закаленных, не склонных к МКК сталей, она отсутствует. У отпущенных ста- лей типа ЭИ943 (0Х23Н28М3Д3Т) в области потенциалов анодной петли имеет место глубокое растравливание зерен и выкрашива- ние отдельных кристаллов (глубина МКК – 70 мкм). В некоторых вариантах метода (например, 10 и 11 прил. 2) рассчитывают коли- чество электричества, израсходованного на реактивацию (Qa) и пассивацию (Qп). Отсутствие или наличие склонности к МКК оп- ределяют по отношению Qa/Qп или ia/iп (ia и iп – плотность тока ре- активации и пассивации соответственно). При этом, чем больше эти отношения, чем выше склонность к МКК, а сама величина от- ношений, устанавливающая отсутствие или наличие склонности к МКК, определяется выбранным вариантом метода.
120
