
2344 - Пустов Ю.А., Ракоч А.Г. - Коррозионностойкие и жаростойкие материалы - 2013
.pdfщей E2 = i r1. Отключение поляризующего тока после полного заряжения двойного электрического слоя до Е0 приводит к исчезновению этого вклада со скоростью спада заднего фронта импульса, а потенциал самого электрода меняется по кривой 3 в соответствии с формулой
Eэ |
= E0 exp |
− |
τ |
. |
(2.41) |
|
|||||
|
|
|
RC |
|
|
Таким образом, для измерения потенциала электрохимической систе- мы без омической составляющей необходимо применение импульсов с длительностью, превышающей время зарядки, и крутым передним
изадним фронтами.
Спомощью рассмотренного способа возможно изучение процес- сов электрохимической коррозии металлов в почве, стальной аппара- туры в бетоне, металлов в диэлектрических средах, под лакокрасоч- ными покрытиями и слоями продуктов коррозии, характеризующих- ся высоким омическим сопротивлением.
Значительно расширяет возможности релаксационных методов изучения коррозионных процессов применение поляризации им- пульсами переменной полярности. Причем изменение соотношения длительностей и амплитуд импульсов позволяет исследовать кинети- ку парциальных электродных реакций, идущих одновременно на по- верхности корродирующего металла, изучить процессы селективного растворения сплавов. Импульсная поляризация является эффектив- ным методом исследования механизма пассивации и природы пасси- вирующих слоев, а в сочетании с вращающимся дисковым электро- дом обеспечивает измерение диффузионных характеристик и расчет концентрации ионов металла в приэлектродном слое, что важно при изучении коррозии в движущихся средах.
2.7.5. Измерение импеданса
Измерение полного сопротивления переменному току границы элек- трод–электролит, называемого импедансом, в коррозионных исследова- ниях наиболее часто применяют для решения следующих задач:
•изучение кинетики электродных процессов на поверхности корродирующего металла;
•определение области потенциалов, в которой происходит ад- сорбция ингибиторов;
•определение сплошности и толщины изолирующих материалов.
При исследовании импеданса используются методы синтеза и анализа наиболее простых линейных электрических цепей, эквива-
71
лентных электрохимической системе. Линейные элементы такой эк- вивалентной цепи (емкости, сопротивления), их величины, характе- ризуют соответствующие электрохимические свойства и параметры системы (емкость двойного электрического слоя, скорость электро- химической реакции, импеданс адсорбции, диффузии и т.д.). При этом для обеспечения эквивалентности необходимо, чтобы зависи- мость тока от потенциала для этих параметров была такой же, как и для элементов электрической цепи, т.е. линейной. Это требование накладывает ограничения на амплитуду прилагаемого к системе си- нусоидального тока, которая для большинства случаев не должна превышать 1…5 мВ.
При измерениях импеданса и анализа их результатов можно вы- делить несколько этапов:
1)экспериментальное определение частотной зависимости изме- ряемого импеданса Z = f(ω), где ω – частота переменного тока;
2)построение эквивалентной электрической схемы;
3)определение параметров элементов этой схемы;
4)определение по этим параметрам электрохимических характе- ристик исследуемой системы.
Для стационарных систем первый этап выполняется с помощью измерения импеданса мостами переменного тока. Задачи, возникаю- щие на этапах 2 и 3, решаются с помощью анализа частотной зави- симости импеданса для исследуемой системы. Анализ проводят пу-
тем сравнения экспериментально установленной зависимости Z = f(ω) с частотной зависимостью ряда вероятных электрических схем, принимаемых в качестве эквивалентных, исходя из физико- химических представлений о свойствах исследуемой границы элек- трод–электролит, т.е. о свойствах двойного электрического слоя, возможности адсорбции веществ на этой границе и протекания опре- деленных электрохимических реакций с учетом транспорта реаги- рующих частиц и продуктов к электроду и от него.
Для простых эквивалентных схем анализ довольно прост и может быть проведен графическим или аналитическим способом. При на- личии же большого числа элементов в эквивалентной схеме анализ существенно усложняется, особенно при изучении свойств границы твердый электрод–электролит, когда из-за неоднородности и шеро- ховатости поверхности возникают трудно определяемые вклады в частотную зависимость импеданса. Необходимость упрощения эк- вивалентной схемы в подобных ситуациях заставляет проводить ис- следования двойного слоя и электродных реакций раздельно.
72
Примером применения измерений импеданса для определения механизма и кинетики электродных процессов являются результаты изучения анодного растворения серебра в щелочи KOH. Независи- мыми поляризационными потенциостатическими измерениями было обнаружено снижение анодного окисления серебра и величины ем- кости границы (в емкостных измерениях) электрод–электролит при наложении положительного потенциала. Первый эффект мог быть связан с замедлением акта разряда, либо с появлением концентраци- онной поляризации, а второй – с наличием полупроводниковых свойств у формирующегося слоя.
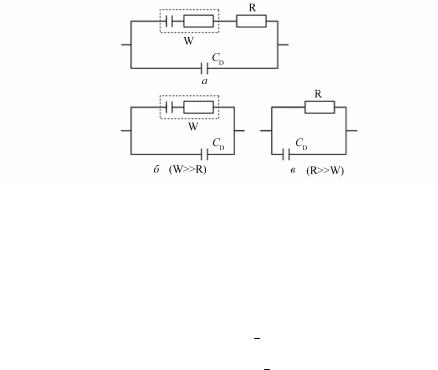
В отсутствие на электроде адсорбции продуктов реакции и при нали- чии стадии диффузии частиц, участвующих в разряде, эквивалентная схема исследуемой границы имеет вид, представленный на рис. 2.33, а, где СD – емкость двойного электрического слоя, R – сопротивление, ха- рактеризующее величину, обратную скорости разряда, W – импеданс диффузии разряжающихся частиц (импеданс Варбурга).
Рис. 2.33. Эквивалентные электрические схемы электродного процесса при наличии диффузии разряжающихся частиц в отсутствие их адсорбции на электроде
Некоторые частные случаи могут быть получены для различных ско- ростей диффузии и разряда (рис. 2.33, б, в). Причем в случае, показанном на рис. 2.33, в, экспериментально измеряемые емкостная СП и омическая RП составляющие импеданса не должны зависеть от частоты переменного тока ω. В то же время для варианта, показанного на рис. 2.33, б, зависи-
− 1
мость емкостной составляющей СП = f( ω 2 ) должна быть линейной, а ее
− 1
экстраполяция к бесконечной частоте ( ω 2 = 0) давать величину СD.
73
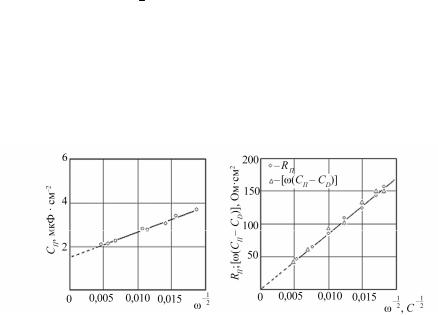
Кроме того, частотные зависимости омической составляющей RП и функ-
− 1
ции [ω(СП − СD)] от ω 2 также должны быть линейны, выходить из нача- ла координат и иметь одинаковый наклон, т.е. совпадать, что и было под- тверждено экспериментально (рис. 2.34). Поскольку наклон прямой на рис. 2.33, б не зависит от содержания щелочи в широком интервале концентраций и, следовательно, от концентрации растворенного оксида Ag2O, полученные результаты указывают на внутридиффузионную при- роду концентрационной поляризации и ее лимитирующий характер в общем процессе анодного окисления серебра.
Рис. 2.34. Экспериментальные зависимости емкостной и омической составляющих импеданса от частоты переменного тока
В подобных экспериментах измерения дают общий импеданс элек- трохимической ячейки, включающий в себя наряду с импедансом ис- следуемого электрода сопротивление электролита и импеданс вспомо- гательного электрода. Для устранения последнего вклада площадь вспомогательного электрода должна быть не менее чем на два-три по- рядка больше площади поверхности исследуемого электрода.
Следует отметить, что при длительных экспериментах и в случае быстро идущих процессов возможно изменение состояния поверхности исследуемого электрода и, соответственно, составляющих импеданса. Во избежание этого применяют потенциостатирование электрода (при корректном включении потенциостата в измерительную схему), сокра- щение времени съемки частотной зависимости и одновременные изме- рения на нескольких частотах с автоматической записью результатов.
Современные потенциостаты снабжаются анализаторами частот-
ного отклика (FRA – Frequency Response Analyzer), предназначен-
ными для проведения исследований импеданса электрохимических систем в реальном масштабе времени (рис. 2.35).
74

Рис. 2.35. Модуль FRA с потенциостатом IPC Pro
2.7.6. Некоторые методы подготовки поверхности образцов к электрохимическим измерениям
При завершении рассмотрения электрохимических методов измере- ний следует остановиться на некоторых методах подготовки образцов, позволяющих улучшить воспроизводимость результатов за счет стан- дартизации состояния поверхности электрода. В частности, в экспери- ментах самого различного типа необходимо перед их началом удалить оксиды, образовавшиеся на рабочем электроде при его контакте с воз- духом. Одним из наиболее распространенных способов проведения та- кой операции для меди, железа, серебра, никеля и других металлов (за исключением элементов, обладающих исключительно высокой тер- модинамической устойчивостью оксидов – Al, Zr, Nb, Ta и т.п.) являет- ся их катодная обработка непосредственно в рабочей ячейке. Причем для свежезачищенной поверхности нержавеющей стали или хрома ка- тодное восстановление ведется в 1 н. растворе H2SO4 при плотности ка- тодного тока iк = 10–2 А/см2 в течение 2…3 мин, а для железа, находив- шегося в течение 10 мин после зачистки на воздухе, iк = 10–5 А/см2 в боратном растворе с рН 7,6. Иногда задается потенциал катодной об- работки, смещение которого в отрицательную сторону от стационарно- го значения (для активного состояния металла) обычно составляет 100…200 мВ. Время обработки в целях устранения возможного наводо- роживания, а иногда и аномального растворения, должно быть мини- мальным, но достаточным для растворения оксидов.
С той же целью применяют отжиг образцов в газообразном водо- роде, способствующий восстановлению исходной структуры поверх- ности и исключающий адсорбцию компонентов раствора на образце и его селективное растворение, присущие методу катодной обработ-
75
ки. Следует отметить, что отжиг в водороде может вызвать обезугле- роживание сталей, требует усложнения аппаратуры и увеличения времени на подготовку образцов к исследованию.
Для повышения воспроизводимости результатов электрохимиче- ских измерений образцы иногда предварительно подвергаются элек- трохимической тренировке, заключающейся в циклической анодно- катодной поляризации электрода по специальной программе, опре- деляемой задачей исследования. Однако при достаточно длительной тренировке состояние поверхности образца может существенно из- мениться и исказить результаты измерений.
В целях создания одинакового исходного состояния образца до- вольно часто применяется потенциостатическая стандартизация по- верхности электрода, состоящая в его выдержке в течение опреде- ленного времени при заданном потенциале. Обычно этот вид обра- ботки используют при изучении пассивного состояния, проводя ее при потенциалах, на 50…100 мВ превышающих потенциал полной пассивации. Длительность выдержки определяется временем стаби- лизации поляризующего тока.
76
3.КОРРОЗИОННЫЕ ИСПЫТАНИЯ
3.1.Лабораторные коррозионные испытания
3.1.1. Испытания при полном погружении
Ускоренные испытания при полном погружении в электролиты следует проводить только в том случае, если металлы предназначены для эксплуатации в подобных условиях.
При проведении испытаний металлических материалов на сопро- тивляемость коррозии при полном погружении, как правило, контроли- руют три наиболее важные факторы: аэрацию, температуру и скорость движения коррозионной среды. Эти факторы различным образом влия- ют на разные металлы, поэтому установление стандарта на условия ис- пытаний в отношении аэрации, температуры и скорости движения элек- тролита практически невозможно. В зависимости от среды эти стандар- тизованные условия испытаний будут благоприятствовать максималь- ной коррозии одних сплавов и минимальной коррозии других, т.е. при- водить к большой ошибке при выборе сплавов для работы в условиях, отличающихся от условий стандартных испытаний.
Полное воспроизведение условий эксплуатации практически не- возможно, в связи с этим рекомендуется последовательное варьиро- вание каждого из перечисленных факторов в выбранной коррозион- ной среде. Полученная информация может быть практически исполь- зована для уменьшения скорости коррозии в условиях эксплуатации.
Температура – это наиболее легко контролируемый фактор. Под- держивается с высокой точностью (±1 оС) с помощью термостата или в условиях кипения раствора в сосуде с обратным холодильником, обеспечивающим постоянную концентрацию раствора.
Аэрация – это подача в раствор кислорода в количестве, равном или превышающем его содержание в воздухе. Проходящий через раствор электролита воздух (кислород) заметно увеличивает ско- рость коррозии даже небольших образцов. Для облегчения перехода кислорода из пузырьков воздуха в раствор применяют специальные фильтры, позволяющие получить пузырьки газа небольших разме- ров. Необходимо исключить непосредственное попадание пузырьков газа на поверхность образца, для чего аэратор помещают в стороне от него. Изменение степени аэрации раствора необходимо проводить не изменением скорости подачи газа, а изменением количества рас-
77
творенного кислорода. Для этого кислород в различных количествах добавляют в поток нейтрального газа (гелий, аргон, азот), пропус- каемого через раствор. Это распространяется и на условия полного отсутствия аэрации, которые могут быть достигнуты путем насыще- ния раствора азотом или другим инертным газом.
Скорость. Определение влияния скорости движения электролита на сопротивляемость металла коррозии является крайне трудным, особенно при высоких скоростях. Наиболее сложно контролировать состояние жидкости при испытании образцов, вращающихся с высо- кой скоростью.
Влияние скорости изучают, используя два типа испытаний:
1)движение образца через жидкость, находящуюся в состоянии покоя;
2)движение жидкости вдоль образца, находящегося в фиксиро- ванном состоянии.
При необходимости применяют оба вида экспозиции. Следует учитывать, что достигать нулевую относительную скорость в реаль- ных условиях не представляется возможным, что связано с постоян- ным перемещением жидкости, вызываемым конвекцией и стеканием продуктов коррозии с поверхности образцов под действием гравита- ционных сил.
На рис. 3.1 представлены самые простые способы испытаний в откры- том сосуде. Испытания можно проводить как при комнатной температуре (рис. 3.1, а), так и при термостатировании. В последнем случае сосуд
собразцами помещают в термостат. Чаще всего применяют водяные тер- мостаты, в которых температура поддерживается с помощью электриче- ских нагревателей и реле (рис. 3.1, б). При проведении испытаний в усло- виях перемешивания коррозионной среды в сосуд помещают стеклянную мешалку (рис. 3.1, в). При использовании электромагнитной мешалки на нее ставят сосуд с образцом, а перемешивание происходит благодаря вращению внутри сосуда железного стержня, запаянного в стекло (рис. 3.1, г). Перемешивание электролита можно проводить, вращая сами
образцы (рис. 3.1, д) или пропуская через электролит поток воздуха под давлением приблизительно 105 Па (рис. 3.1, е).
При проведении испытаний при полном погружении рекоменду- ется использовать на 1 см2 площади образца 20…200 см3 раствора.
Во время испытаний особое внимание следует уделять монтажу образцов. Недопустимо наличие прямых контактов образцов с эле- ментами крепления. В некоторых случаях на контактирующие по- верхности наносят защитное покрытие.
78
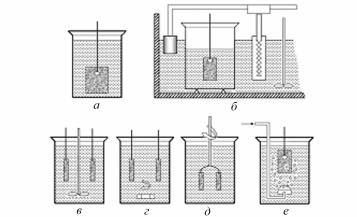
Рис. 3.1. Способы испытаний металлических образцов в открытом сосуде при полном погружении:
а– при комнатной температуре в спокойном электролите;
б– при повышенных температурах в термостате;
в– при перемешивании раствора стеклянной мешалкой;
г– при перемешивании электромагнитной мешалкой (ЭММ);
д– при вращении образцов;
е– при перемешивании и аэрации потоком воздуха под давлением 105 Па
Если при изучении влияния малых скоростей (~10 см/с) могут быть использованы несложные устройства, обеспечивающие вертикально- вращательное движение образца (рис. 3.1, в–е), то для исследования эффектов, возникающих при более высоких скоростях, требуется при- менение разнообразной аппаратуры, с помощью которой достигается высокая скорость движения образца в растворе. Образцы жестко за- крепляются на горизонтальных валах, которые приводятся в движение электродвигателем, обеспечивающим заданную скорость вращения. Испытания, проведенные этим способом, показали, что для каждого материала существует определенная критическая скорость, по дости- жении которой наступает разрушение защитных пленок.
При всей очевидной простоте описанный способ имеет существен- ный недостаток. В данном случае критическая скорость отражает толь- ко качественную характеристику относительной способности материала сопротивляться коррозионному воздействию высоких скоростей, по- скольку величина критической скорости зависит от диаметра диска.
Разновидностью описанного метода является испытание образцов, закрепленных на периферии вращающихся в коррозионной среде дисков (рис. 3.2). В этом случае возникает сильное перемешивание
79
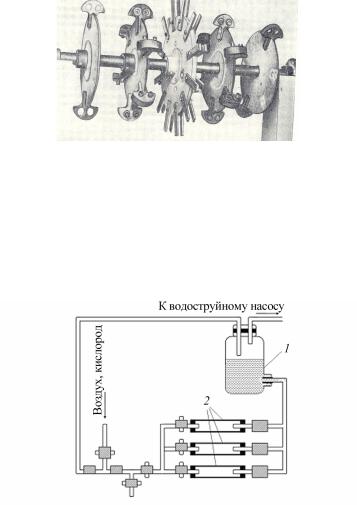
раствора и, в зависимости от уровня раствора над образцом, может происходить более или менее значительный захват раствором пу- зырьков воздуха.
Рис. 3.2. Крепление образцов в условиях испытаний образцов, закрепленных на периферии вращающихся дисков
Прямым методом изучения влияния скорости перемещения агрес- сивной среды на устойчивость к коррозионному разрушению являет- ся пропускание ее через образец в виде трубы (рис. 3.3). Скорость потока задается контрольным клапаном или регистрируется специ- альным измерительным счетчиком.
Рис. 3.3. Установка для коррозионных испытаний в условиях циркуляции электролита с аэрацией:
1 – сосуд с электролитом; 2 – образцы в виде труб
Испытания при повышенных температурах в агрессивных элек- тролитах (кислотах) проводят с помощью устройства, снабженного
80
