
Vlianie_grandaxina_na_pokazateli_kachestva_zhiz
.docxСтруктурные изменения региональной геометрии левого желудочка могут способствовать позднему прогрессирующему нарушению функции левого желудочка, которое продолжается длительное время в отсутствие дополнительных эпизодов ишемии и некрозов миокарда [20].
В табл. 2 представлено распределение пациентов с различными типами ремоделирования миокарда левого желудочка в зависимости от ФК ХСН в точках исследования.
Таблица 2. Распределение пациентов с концентрической гипертрофией и концентрическим ремоделированием миокарда левого желудочка в зависимости от ФК ХСН
|
ФКХСН |
Опытная группа (n=42) |
Контрольная группа (n=46) |
||
|
0 нед |
24 нед |
0 нед |
24 нед |
|
|
ФКI - концентрическая гипертрофия |
2% |
0 |
2% |
0 |
|
ФКI - концентрическое ремоделирование |
2% |
4% |
2% |
4% |
|
ФК II - концентрическая гипертрофия |
10% |
10% |
10% |
8% |
|
ФК II - концентрическое ремоделирование |
26% |
26% |
26% |
28% |
|
ФК III - концентрическая гипертрофия |
20% |
18% |
18% |
16% |
|
ФК III - концентрическое ремоделирование |
30% |
32% |
32% |
34% |
|
ФК IV - концентрическая гипертрофия |
0 |
2% |
0 |
2% |
|
ФК IV- концентрическое ремоделирование |
8% |
6% |
8% |
6% |
Анализ
динамики изменения характера
ремоделирования сердца в процессе
терапии больных 1 и 2 групп свидетельствует
об отсутствии достоверных различий
между пациентами опытной и контрольной
групп. Так, в конце 6-месячного наблюдения
концентрическая гипертрофия (увеличение
массы миокарда и относительной толщины
стенки левого желудочка) наблюдалась
у 30% пациентов опытной и у 32% - контрольной
групп. В остальных случаях пациенты
имели концентрическое ремоделирование
миокарда (нормальная масса миокарда и
увеличенная относительная толщина
стенки левого желудочка). 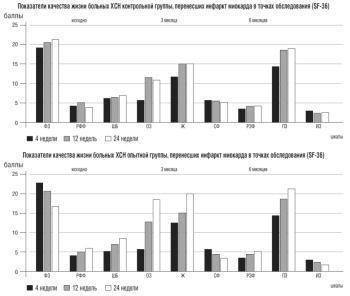
Более выраженные изменения дистанции ТШХ, показателей ХМЭКГ, ФВ и ИС в конце 6-месячной терапии у больных опытной группы по сравнению с пациентами контрольной нашли отражение и в существенном различии показателей КЖ больных 1 и 2 групп (рис. 5).
Рисунок 5. Показатели качества жизни больных хронической сердечной недостаточностью контрольной и опытной групп в точках обследования
Шкалы: ФЗ - физическое здоровье, РФФ - ролевое физическое функционирование, ШБ - шкала боли, 03 -общего здоровья, Ж - жизнелюбия, СФ - социального функционирования, РЭФ - ролевого эмоционального функционирования, ПЗ - психического здоровья, ИЗ - изменения состояния здоровья, КЖ - коэффициент качества жизни (%)
Согласно Миннесотскому опроснику и опроснику SF - 36, включающему в себя все аспекты деятельности человека (физический, социальный и эмоциональный), показатели КЖ в опытной группе достоверно увеличились на 22,8% и 39,1%, соответственно (рис. 8). Динамика этих показателей в контрольной группе составила 8,1 % и 13,2%, соответственно; различие между 1 и 2 группами достоверно (р<0,05). Это не может не сказаться на продолжительности и результатах реабилитации, цель которой - снижение инвалидизации населения после перенесенного инфаркта миокарда и возвращение больного к полноценной жизни.
Важной также является установленная в ходе исследования зависимость между увеличением толерантности к нагрузкам (по данным ТШХ), уменьшением частоты эпизодов ишемии миокарда и показателями психологических тестов: шкала боли SF-36 и Сиетлский опросник. Показатели этих шкал выросли по сравнению с исходными на 35,8% (р<0,05) и на 62,9% (р<0,05), соответственно. То есть у пациентов основной группы на фоне роста коронарного резерва, редукции тревожно-депрессивной симптоматики уменьшились количество и интенсивность ангинозных приступов (рис.6).
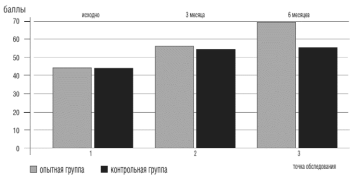
Рисунок 6. Показатели качества жизни больных со стенокардией в точках обследования (Сиетлский опросник)
Анализ взаимосвязи качества жизни пациентов и типов ремоделирования миокарда свидетельствует об отсутствии линейной зависимости между соматическим состоянием больных, клиническим течением болезни и степенью удовлетворенности жизнью. При более детальном анализе показателей качества жизни в группе пациентов с концентрической гипертрофией миокарда установлены достоверно более высокие показатели по шкале социального функционирования и более низкие - по шкале ролевого эмоционального функционирования (SF-36).
Это свидетельствуете выраженной психо-социальной дезадаптации этих больных по сравнению с группой пациентов с концентрическим ремоделированием миокарда. Основными причинами снижения качества жизни у больных в раннем постинфарктном периоде являются разного рода ограничения, прежде всего - в социальном статусе и повседневной активности.
Так
как у пациентов с тревожно - депрессивной
симптоматикой имеется нарушение баланса
между симпатическим и парасимпатическим
отделами вегетативной нервной системы,
это опосредованно может приводить к
нарушениям ритма сердца. В связи с этим
проводилась оценка вегетативного
статуса пациентов с помощью шкалы
балльной оценки проявлений вегетативной
дистонии [11]. На момент включения в
исследование у пациентов обеих групп
был одинаковый уровень проявлений
вегетативной дисфункции. На фоне
применения Грандаксина в составе
базисной терапии ХСН уровень вегетативной
дисфункции снизился на 38,9% (нормализовался),
а в контрольной группе (прием только
базисных препаратов) - на 15,9% (межгрупповые
различия достоверны, р<0,05) (рис. 7). 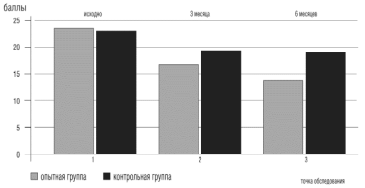
Рисунок 7. Показатели синдрома вегетативной дисфункции у больных ХСН в точках обследования
Таким образом, в ходе лечения психический и соматический компоненты заболевания подвергались обратному развитию параллельно, что подтверждает сочетание противотревожного и вегетостабилизирующего эффектов в спектре клинической эффективности Грандаксина. Снижение исходного уровня тревоги на фоне улучшения объективных характеристик (ТШХ, ФВ, ИС и т.д.) проявлялось редукцией эмоциональных нарушений, опасений за неблагоприятный исход восстановительного периода инфаркта миокарда. Уже через 1-2 недели лечения Грандаксином пациенты отмечали уменьшение частоты и выраженности ощущения учащенного сердцебиения, напряжения в теле, плаксивости; нормализовался сон. На этом фоне повышался уровень социальной адаптации больных опытной группы. Эти пациенты, оказавшись вне поля зрения врача, смогли вернуться к прежнему уровню активности (физической и социальной).
В ходе проведенного исследования установлено, что переносимость препарата в целом хорошая. Случаев преждевременной отмены Грандаксина из-за побочных эффектов не было. Гематологические, клинико-биохимические показатели при дополнении препаратом базисной терапии ХСН не изменялись. После отмены Грандаксина не обнаружено признаков лекарственной зависимости.
Анализ основных параметров ЭКГ пациентов основной группы в начале и в конце исследования показал, что применение Грандаксина в сочетании с препаратами лечения ХСН не влияет на продолжительность основных ЭКГ-интервалов (PQ, QT и т.д.) (табл. 3).
Таблица 3. Показатели электрокардиограммы у больных ХСН, перенесших инфаркт миокарда, на фоне дополнения базисной терапии Грандаксином
|
Показатели ЭКГ |
Опытная группа (n=42) |
Контрольная группа (n=46) |
|||
|
На момент включения в исследование |
В конце исследования |
На момент включения в исследование |
В конце исследования |
||
|
R-R,сек |
3,683+0,032 |
4,12+0,014 |
3,742+0,034 |
4,123+0,023 |
|
|
P-Q,сек |
0,154+0,043 |
0,194+0,015 |
0,134+0,032 |
0,187+0,014 |
|
|
Q-T, сек |
0,318+0,043 |
0,381+0,0123 |
0,321 ±0,022 |
0,379+0,012 |
|
Многие психотропные препараты, в том числе и транквилизаторы, противопоказаны при наличии у пациента синдрома апноэ во сне, так как могут усугубить его проявления. Поэтому входе настоящего исследования оценивались показатели шкалы для выявления апноэ во сне до и после окончания приема препарата. Анализ полученных данных показал, что применение Грандаксина не влияет на выраженность апноэ во сне (пограничное значение по шкале "Апноэ во сне" - 3 балла) (рис.8).
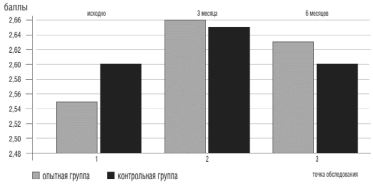
Рисунок 8. Показатели опросника "апноэ во сне" у больных ХСН в точках обследования на фоне приема Грандаксина
С учетом данных ряда публикаций о неблагоприятном влиянии транквилизаторов на уровень внимания и оперативной памяти [12] изучались показатели когнитивных функций, исходно изменённые у многих больных с тяжелыми формами ИБС. Ни у одного из пациентов опытной группы клинически значимых нарушений когнитивного статуса не наблюдалось. К концу исследования в обеих группах сократилось общее время выполнения тестов, свидетельствующих об уровне внимания, кратковременной и долговременной памяти, логического мышления (на 15,4% - в опытной и на 8,5% - в контрольной группах, р<0,05). Это можно объяснить улучшением сократительной способности миокарда, увеличением ФВ, а следовательно - кровообращения головного мозга.
За время наблюдения (6 мес) признаков неблагоприятного лекарственного взаимодействия Грандаксина с соматотропными препаратами (нитраты, р-блокаторы, антиаритмики, ингибиторы АПФ, сердечные гликозиды, мочегонные) не отмечалось.
Заключение Полученные данные свидетельствуют об эффективности Грандаксина в терапии тревожно-депрессивных расстройств у больных ХСН в раннем постинфарктном периоде. На фоне нормализации психологического статуса пациентов, получавших Грандаксин, прослеживается положительная динамика их объективного статуса: рост фракции сердечного выброса, увеличение дистанции ТШХ, снижение индекса сократительной способности миокарда. Психическое состояние и качество жизни больных хронической сердечной недостаточностью, перенесших инфаркт миокарда, весьма динамично.
Основными причинами снижения качества жизни у больных в раннем постинфарктном периоде являются разного рода ограничения, прежде всего - в социальном статусе и повседневной активности. Взаимосвязь между соматическим состоянием, психологическим статусом и качеством жизни больных хронической сердечной недостаточностью в раннем постинфарктном периоде не носит характера прямой линейной зависимости.
У пациентов опытной группы в ходе 6-месячного наблюдения установлена значимая редукция тревожно-депрессивной симптоматики, что сопровождается уменьшением выраженности симптомов ХСН и коронарной недостаточности, снижением индекса локальной сократимости миокарда и ростом фракции сердечного выброса. Это позитивно сказывается на когнитивно-мнестических функциях данных пациентов. Кроме того, обнаружено, что Грандаксин опосредованно влияет на электрическую стабильность миокарда за счет нормализации баланса между парасимпатическим и симпатическим отделами вегетативной нервной системы. Резюмируя вышеизложенное, можно констатировать, что применение Грандаксина улучшает качество жизни постинфарктных больных, сокращает сроки реабилитационного периода, позволяет лучше адаптироваться к окружающей действительности и вновь стать полноценным членом общества.
Грандаксин характеризуется высокими показателями переносимости и безопасности.
Результаты исследования позволяют рекомендовать использование Грандаксина с целью коррекции психологического статуса у больных ХСН в раннем постинфарктном периоде, имеющих тревожные расстройства, умеренные проявления вегетативной дисфункции, умеренные инсомнические нарушения.
Отсутствие значимого положительного эффекта этого препарата у пациентов с субклинической депрессией, по-видимому, требует дополнительного назначения антидепрессантов.
Таким образом, применение Грандаксина в составе базисной терапии ХСН улучшает не только физическое функционирование больных, перенесших инфаркт миокарда и имеющих аффективные расстройства, но и улучшает качество жизни пациентов (их психологический и социальный статус), обеспечивая лучший эффект от реабилитационных мероприятий по сравнению с базисной терапией.
Литература
1. Беленков Ю.Н, Мареев В.Ю. Принципы рационального лечения хронической сердечной недостаточности. М; 2000:254. 2. Вейн A.M. Вегетативные расстройства. М. 2000:749. 3. Вейн A.M., Рябус М.В. Нарушения сна в общемедицинской практике. М. Медпресс. 1998:43. 4. Дробижев М.Ю. Лечение депрессивных расстройств в кардиологии. Consilium Medicum. Экстравыпуск. 2002:15-18. 5. Левин Я.И, Садыкова Э.Т. Золпидем в лечении нарушений сна у больных ишемическим инсультом. Российский медицинский журнал. 1996;3:16-19. 6. Новик А.А., Ионова Т.И. Концепция исследования качества жизни в медицине/Изд. "Элби"; Санкт -Петербург. 1999;139. 7. Оганов Р.Г, Масленникова Г.Я. Стратегия преодоления стресса в современных условиях. Кардиология. 2002;44:7: 72-76. 8. Погосова Г.В. Депрессия: новый фактор риска ИБС и предиктор коронарной смерти. Кардиология. 2002; 42:4:86-90. 9. Смулевич А.Б. Депрессивные расстройства в кардиологии. Consilium Medicum. Экстравыпуск. 2002:3-5. 10. Сыркин А.Л. Ишемическая болезнь сердца и соматизированные депрессии: особенности клиники, дифференциальной диагностики и терапевтических подходов. Consilium Medicum. Экстравыпуск. 2002:7-9. 11. Сыркин А.Л. Инфаркт миокарда. М. 1998; 548. 12. Шейдер Р. Психиатрия. М. Практика, 1998; 765.
