
- •0Лекция № 1.
- •1.Статическая биохимия (изучает структуру веществ ) - биоорганическая химия.
- •2.Значение биохимии для диагностики заболеваний.
- •1 .Альфа спираль ( л.Поллинг) - виток составляет от 3 до 6 ак. Терминатором спирали является ак-пролин.
- •2.Бетта складчатый слой.
- •3.Петли полипептидной цепи (соединительные петли).
- •1.Физико-химические свойства белков. Их использование для разделения белков.
- •2.Принципы классификации белков.
- •3.Характеристика простых белков.
- •1.Молекулярная масса белков определяет многие свойства белков: седиментация, диффузия, плотность белковых растворов, коллоидные свойства белков и др. Характеристики.
- •2.Способность белков связываться с лигандами,
- •3.Электрохимические свойства белков.
- •1. Концевыми соон и nh2 группами.
- •2.Боковыми группами:
- •1.Ионообменная хроматография.
- •2.Разделение белков на основании величины заряда - электрофорез белков. С помощью электрофореза в сыворотке крови выделяют как минимум 5 фракций: альбумины, альфа, альфа-2, гамма, бета - глобулины.
- •4.Коллоидные свойства белков.
- •5. Гидратация белков - способность белков связывать воду. Она осуществляется за счёт:
- •1. Повышают скорость реакции.
- •1.Витаминные.
- •4.Специфичность действия ферментов. В основе специфичности действия ферментов лежит конформационное соответствие его активного центра молекуле субстрата. Различают следующие виды специфичности:
- •1.Ингибиторы ферментативной активности.
- •1. Класификация ферментов.
- •1.Энзимопатология (патологическое состояние, связанное с полным отсутствием фермента в организме).
- •1.Поступление веществ из внешней среды посредством питания и дыхания.
- •1 .Катаболическая - распад ацетила.
- •1.Теория «активации» кислорода академика баха. Ведущей ролью в процессе биологического окисления он представлял образование пероксидов.
- •1 .Механизм окислительного фосфорилирования.
- •1. Целостность мембраны - непроницаемость её для протонов.
- •1.Связывание кислорода с активным центром фермента.
- •2.Восстановление кислорода и перенос его на субстрат.
- •1.Диоксигеназы - ферменты, включающие в субстрат молекулу кислорода.
- •2. Вторичные радикалы (он, липидные радикалы – l,, lo,, loo,) Их образование происходит с участием железа (11). Это патологические продукты.
- •3. Третичные радикалы (антиоксиданты) - образуются под влиянием вторичных радикалов.
- •1 .Фермент - супероксиддисмутаза (сод).
- •2.Она раздражает слизистую оболочку жкт, усиливая секрецию желёз.
- •3.Усиливает сокращение кишечника,
- •4.В толстом кишечнике под действием ферментов условно-патогенной микрофлоры клетчатка подвергается брожению с образованием глюкозы, лактозы и газообразных веществ.
- •1. Основной фосфоролитический путь
- •2.Неосновной амилолитический.
- •1.Болезнь ферса - фосфорилаза печени.
- •3 Реакции гликолиза являются необратимыми:
- •1.Гексокиназная.
- •2.Фосфофруктокиназная.
- •3.Пируваткиназная.
- •1. Глицеральдегид-3-фосфат
- •1. Транскетолазные реакции:
- •1.Липиды, их классификация и биологическая роль.
- •2.Превращение липидов в органах пищеварения.
- •1.Структурными липидами.
- •2.Резервными липидами.
- •3.Свободными липидами. — хиломикроны,
- •1 .Структурная. Липиды являются обязательным структурным компонентом биологических мембран клеток.
- •1. Эмульгируют пищевые жиры.
- •2. Активируют липолитические ферменты.
- •3. Выполняют роль переносчиков трудно растворимых в воде продуктов гидролиза жира и жирорастворимых витаминов a, d, е, к.
- •1.Транспортные липопротеины крови. Состав и биологическая роль. 2.Простагландины, простациклины, тромбоксаны, лейкотриены. Механизм их образования и биологическая роль.
- •3.Окисление глицерина и вжк в тканях.
- •1. Хиломикроны. Образуются в стенке кишечника и имеют самый крупный размер частиц.
- •2. Лпонп. Синтезируются в стенке кишечника и печени.
- •3. Лпнп. Образуются в эндотелии капилляров из лпонп.
- •4. Лпвп. Образуются в стенке кишечника и печени.
- •1.Простагландины:
- •1 . Альфа -глицерофосфата
- •1.Биосинтез вжк в тканях, химизм реакций, биологическая роль. 2.Холестерин, биологическая роль, биосинтез, окисление. 3.Патология липидного обмена.
- •1.Наличие атф, со2, н2о, надф*н2, поступающий из гексозомонофосфатного пути превращения глюкозы.
- •2.Наличие специальных белков-переносчиков (hs -апб). 3.Наличие специальных ферментов синтеза.
- •1.Структурная. Свободный холестерин является, обязательным структурным компонентом мембран клеток.
- •2.На этапе пищеварения.
- •1. Белковое питание.
- •2. Превращение белков в органах пищеварения.
- •3. Гниение белков. Образование токсических продуктов и механизм их обезвреживания.
- •1 .На этапе поступления жиров с пищей:
- •2.На этапе пищеварения.
- •1. Белковое питание.
- •1.Реакция декарбоксилированая.
- •1. Источники аминокислот в клетке и пути их использования.
- •3.Реакции дезаминирования - разрушение nн2-группы с выделением аммиака. В организме возможны следующие виды дезаминирования.
- •1. Образование амидов
- •2. Восстановительное аминирование.
- •3. Образование солей аммония.
- •4. Синтез мочевины - основной путь обезвреживания аммиака - орнитиновый цикл.
- •1.Особенности метаболизма нуклеопротеинов.
- •2.Бета -аминоизобутират.
- •1.Азот промежуточных продуктов (пептиды, ао, ак, креатин, индол, скатол и т.Д.)
- •2.Азот конечных продуктов (мочевина, мочевая к-та, индикан, креатинин)—
- •1.Продукционная - повышение образования компонентов остаточного азота, главным образом
- •2.Ретенционная - задержка азотистых шлаков из-за нарушения выделительной функции почек.
- •1. Нарушение на этапе поступления белков. В норме в организм должно поступать 80 - юОгр белков. Обязательно поступление всех незаменимых ак.
- •2. Нарушение на этапе пищеварения:
- •3. Нарушение межуточного обмена - нарушение обмена аминокислот в тканях.
- •1. Матрица - нити днк. Расщепление нити называется репликативная вилка. Она
- •2. Репарация днк.
- •3. Транскрипция гена.
- •1. Матрица - 1 нить днк. Образуется транскрипционный глазок.
- •1.Рекогниция (распознавание) - узнавание между аминокислотами и их транспортной
- •3. Инициация - начало процесса трансляции.
- •4. Элонгация (продолжение) протекает циклически в виде последовательной смены трёх фаз:
- •5. Терминация (прекращение).
- •6. Броцессинг белка (созревание) совокупность химических модификаций
- •1. Регуляция происходит только на уровне транскрипции. Первичные транскрипты генов у них транслируются до завершения транскрипции.
- •3. Регуляция биосинтеза белков у прокариот протекает альтернативно путём репрессии и индукции.
- •1. Выделение днк из биологического материала.
- •2. Амплификация - репликация на органическом участке молекулы днк. Производится за счёт работы ферментов и смены температурных режимов.
- •3. Детекция продуктов pcr (копий заданного участка) Схема pcr:
- •1. Изучаемая днк,
- •1. Структурные гены
- •2. Регуляторные элементы
- •1. Фенотипическое различие между клетками,
- •2. Индивидуальные различия между организмами одного вида. Каждый человек отличается от другого человека на 0,1% генома.
- •3. Широкое разнообразие белков. На основе 35000 генов синтезируются около 5000000 белков. В настоящее время нельзя сказать точно, что изучать важнее - геном или белковый состав организма.
- •1. Лежит в основе развития предрасположенности к заболеваниям (атеросклероз)
- •1.Внутриклеточное и межклеточное согласование клеточных процессов,
- •1.Малый период жизни (динамичность, оперативность регуляции).
- •1. Фактор расширения сосудов;
- •1. Передняя
- •1. Стимуляция синтеза белка: (через ифр I.)_
- •2. Влияние на углеводный обмен:
- •3. Влияние на минеральный обмен (через ифр1) - задержка кальция, фосфора, магния в организме,
- •4. Влияние на липидный обмен (не через ифр 1):
- •1. Альфа -меланоцитстимулирующий гормон (мсг) (промежуточная доля).
- •1. Гормоны щитовидной и паращитовидной желез.
- •1. Повышение поглощения тканями кислорода за исключением мозга, ретикуло-эпителиальной системы и гонад.
- •1. Углеводный обмен:
- •2. Липидный обмен:
- •1. Выделяют группу энзимовитаминов - это предшественники коэнзимов или простетических групп ферментов:
- •4. Участвуют в синтезе медиаторов (вит.С - серотонин), стероидных гормонов. Авитаминоз - это патологическое состояние, которое развивается в результате отсутствия
- •1. Он принимает участие в дифференцировке эпителиальных тканей, а также участвует в регуляции роста и дифференцировке эмбриональных тканей. В эмбриональных тканях
- •1. Нарушение дифференцировки эпителия - кератинизация.
- •2. Нарушение восприятия света и сумеречного зрения - гемеролапия («куриная слепота»). При хроническом гиповитаминозе вит.А развивается дистрофия и необратимая дегенерация палочек.
- •1 Витамин к и витамин е.
- •2 Водорастворимые витамины.
- •1. Является кофактором карбоксилирования глу в протромбине, т.Е. Необходим для его поевпашения в тромбин.
- •2. Участвует в превращении проконвертина в конвертин
- •1. Участие в окислительно-восстановительных реакциях:
- •2. Синтез кортикостероидов
- •1. Входит в состав тдф: тиамин(атф) ® тдф
- •2.Участвует в передаче нервного импульса.
- •1. Участвует в окислительно-восстановительных реакциях, т.К. Входит в состав фермента фмн
- •I. Метилирование в12
- •1. Является ко-ферментом карбоксилаз пвк, ацетил -коа, пропионил-коа.
- •2. Участвует в реакциях синтеза жирных кислот и стерина.
- •1. Входит в состав ко-фермента а, следовательно, участвует в синтезе ацетил-коа, различных ацил-коа, образующихся в результате следующих реакций:
- •2. Участвует в синтезе более 80 различных ферментов.
- •1. Участвует в образовании фосфотидилхолина.
- •1. Прямо воздействующие:
- •2. Структуры аналогичные витаминам:
- •1. Снижение затрат энергии в современных условиях, следовательно, необходимость снижение
- •1. Для крови: нб - 75%, кб - 25%. Суммарно этот показатель обозначается, как общий билирубин крови, который в норме для взрослого человека составляет 8 -20ммоль/л.
- •2. Печеночная желтуха (токсические и вирусные и другие гепатиты).
- •3. Подпеченочная желтуха (механическая).
- •4. Физиологическая желтуха новорождёных.
- •1. Транспортирует ионы меди, связывает и удерживает их в кровеносном русле
- •3. Обладает противовоспалительным действием
- •4. Является антиоксидантом, обезвреживает активные формы кислорода и пол.
- •IgD. Функция неизвестна.
- •1. Метаболиты: аминокислоты (25%), креатин (5%), полипептиды и нуклеотиды (3,5%)
- •2. Конечные азотистые продукты: мочевина(50%), мочевая кислота (4%), креатинин (2,5%), индикан и аммиак.
- •1.Экскреторная функция - это выделение мочевины, мочевой кислоты, креатина, лекарств, токсинов, избытка воды, микроэлементов, электролитов. Состоит из трёх фаз:
- •2.Регуляторная и гомеостатическая.
- •3.Секреторная функция:
- •1.Мочевина (20 - 35г/сутки). Повышается при повышенном распаде белков при нормальной функции печени, высокобелковое питание. Понижается при нарушении синтеза в печени, нарушении функции почек.
- •3. Креатинин (0,8 - 2,3г/сутки). Повышается при усиленном распаде компонентов мышечной ткани (травмы мышц), увеличение употребления мясной пищи. Понижается при угнетении фильтрации почками.
- •4. Белок (не более зОмг/л). Качественными реакциями не обнаруживается. Протеинурия наблюдается при гематурии, нарушении функции почек.
- •1. Химический состав нервной ткани.
- •1. Глу связывает аммиак
0Лекция № 1.
Биохимия, её задачи. Структурная организация белков.
1 .Предмет биохимии.
2.Задачи биохимии.
3.Значение биохимии для медицины.
4.Белки,их биологическая роль.
5.Структурная организация белков.
Биохимия относится к фундаментальным дисциплинам медицины и биологии. В результате научного познания мира выделился ряд фундаментальных дисциплин: философия, физика, химия, биология и д.р. Биохимия выделилась с одной стороны в результате разделения наук. Ей не доставало точности, т.к. длительно она была описательной наукой. Середина 20 в. ознаменовалась глобальными открытиями в физике. В это же время интеграция биологии с точными науками способствовала её бурному развитию. Биохимия возникла как наука, благодаря привлечению в биологию точных знаний, в частности химии.
Биохимия—наука о структуре веществ, входящих в состав живого организма, их превращениях и физико-химических процессах, лежащих в основе жизнедеятельности.
Выделяют три составных компонента общей биохимии:
1.Статическая биохимия (изучает структуру веществ ) - биоорганическая химия.
2.Динамическая биохимия (изучает превращение веществ в организме).
3.Функциональная биохимия ( изучает процессы, лежащие в основе функций органов и тканей). Кроме общей (базисной) биохимии выделяют ещё ряд разделов биохимии, в зависимости от направления проводящихся исследований:
1.Биохимия растений.
2.Биохимия микроорганизмов.
3.Биохимия животных.
4.Медицинская биохимия.
5.Ветеринарская биохимия.
6.Техническая биохимия.
7.Биохимия генетики.
8.Молекулярная биохимия.
Задачи биохимии.
1.Изучение процессов БИОКАТАЛИЗА.
2.Изучение механизмов наследственности на молекулярном уровне.
3.Изучение строения и обмена нуклеиновых кислот.
4.Изучение строения и обмена белков.
5.Изучение превращения углеводов.
6.Изучение обмена жиров.
7.Изучение биологической роли сигнальных молекул (ГОРМОНЫ, НЕЙРОМЕДИАТОРЫ).
8.Изучение роли витаминов в обмене веществ.
9.Изучение роли минеральных веществ.
Значение биохимии для медицины.
Основные вопросы медицины: патогенез, диагностика, лечение и профилактика заболеваний.
1.Значение биохимии для понимания механизма заболевания.
ПРИМЕР. В норме, ГЕМОГЛОБИН-А располагается в эритроцитах равномерно, занимая весь объём клетки. При смене 1 АК ГЛУТАМИНА на ВАЛИН образуется ГЕМОГЛОБИН-S, плохо растворимый и выпадающий в эритроцитах в осадок. Сущность этого заболевания раскрыл Л. ПОЛЛИНГ. Только биохимические исследования позволяют диагностировать это заболевание и раскрыть механизм развития вследствие недостатка гормона инсулина. Сердечно-сосудистые заболевания (атеросклероз). Раньше считали, что важную роль в патогенезе принадлежит накоплению ЛИПОПРОТЕИНОВ низкой плотности и нарушение соотношения между ЛИПОПРОТЕИНАМИ низкой плотности и ЛИПОПРОТЕИНАМИ высокой плотности. В настоящее время предполагают, что важным является чувствительность рецепторов клеток к ЛИПОПРОТЕИНАМ низкой плотности.
2.Значение биохимии для диагностики заболеваний.
Широкое использование биохимических исследований биологических жидкостей.
A. Количество субстратов.
Б. Исследование активности ферментов.
B. Исследование уровня гормонов. Методы РИА, ИФА, ИХЛА, ДНК-зонды.
Важным моментом в настоящее время является выявление ПРЕДЗАБОЛЕВАНИЙ.
3. Значение биохимии для лечения. Выявление нарушенных звеньев метаболизма и создание соответствующих лекарственных препаратов, широкое использование природных препаратов.
4.Значение биохимии для профилактики заболеваний.
ПРИМЕР. Недостаток витамина С —цинга—для профилактики использование витамина С (профилактика простудных заболеваний).
Недостаток витамина D— рахит— использование витамина D.
БЕЛКИ, ИХ БИОЛОГИЧЕСКАЯ РОЛЬ.
Белки - это высокомолекулярные азотсодержащие органические вещества, состоящие из АК. соединённых ПЕПТИДНЫМИ связями в ПОЛИПЕПТИДНУЮ цепь, и имеющие сложную структурную организацию.
Характерные признаки белков, отличающие их от других соединений:
1 .Белки - АЗОТСОДЕРЖАЩИЕ вещества (до 16 %).
2.Структурной единицей белков являются альфа АК L-РЯДА.
![]()
3-.АК связываются ПЕПТИДНЫМИ связями в ПОЛИПЕПТИДНУЮ цепь.
4.Большая молекулярная масса белков (от 20000 до нескольких миллионов дальтон).
5.Сложная структурная организация.
ФУНКЦИИ БЕЛКОВ.
1.Каталитическая. Многие белки являются ферментами
2.Регуляторная. Некоторые гормоны являются белками
3.Структурная. Во все структуры живой клетки входят белки.
4.Рецепторная. Белки являются обязательным компонентом рецепторов, способны узнавать другие молекулы.
5.Транпортная. Транспорт жиров, лекарственных веществ и д.р.
6.Опорная. Коллаген, белки костной ткани.
7.Энергетическая. Окисление 1 грамма белка сопровождается выделением 17 КДЖ энергии. В сутки 15% энергии образуется за счёт распада Б.
8.Сократительная. Актин, миозин мышц.
9.Генно-регуляторная (ГИСТОНЫ).
10.Иммунологическая. Антитела являются белками.
11 .Гемостатическая. Фибриноген.
СТРУКТУРНАЯ ОРГАНИЗАЦИЯ БЕЛКОВ. Свойства белков обусловлены их структурой.
ПЕРВИЧНАЯ СТРУКТУРА - последовательное соединение АК в ПОЛИПЕПТИДНОЙ цепи с помощью ПЕПТИДНЫХ связей.
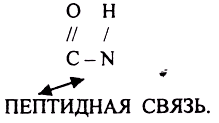
Свойства ПОЛИПЕПТИДНОЙ цепи зависят от составляющих её АК.
Порядок АК в цепи устанавливается с помощью СЕКВЕНИРОВАНИЯ - процедура выявления последовательности АК. Впервые было проведено в 1958 г. Ф. СЕНДЖЕРОМ на инсулине.
ВТОРИЧНАЯ СТРУКТУРА - способ укладки в пространстве ПОЛИПЕПТИДНОЙ цепи. Образуется за счет водородных связей между 1 и 4 АК.
![]()
Выделяют 3 вида вторичной структуры:
