
- •Оглавление.
- •Раздел I введение в технологию
- •Глава 1
- •Основные понятия и определения
- •§ 1.1. Предмет и содержание курса технологии отраслей промышленности
- •§ 1.2. Связь технологии с экономикой
- •§ 1.3. Понятие о технологических процессах: принципы их классификации
- •§ 1.4. Материальные и энергетические (тепловые) балансы
- •§ 1.5. Понятие о себестоимости и качестве промышленной продукции
- •§ 1.6. Общие положения по технике безопасности и охране труда на промышленных предприятиях
- •Глава 2 сырье, вода и энергия в промышленности § 2.1. Сырье в промышленности
- •Минеральное сырье
- •Растительное и животное сырье
- •Обогащение сырья
- •Комплексное использование минерально-сырьевых ресурсов
- •§ 2.2. Вода в промышленности
- •Промышленная водоподготовка
- •Промышленные сточные воды и их очистка
- •§ 2.3. Роль энергии в технологических процессах
- •Рациональное использование энергии
- •Глава 3 научно-техническая революция и научно-технический прогресс в промышленности § 3.1. Сущность, значение и основные направления научно-технического прогресса
- •§ 3.2. Нтр и технология
- •§ 3.3. Химизация народного хозяйства - важное направление нтп
- •§ 3.4. Нтп в области промышленных материалов
- •§ 3.5. Нтп в области орудий труда. Механизация, автоматизация и роботизация производства
- •§ 3.6. Применение вычислительной техники и асу в технологии
- •§ 3.7. Экологические проблемы нтп
- •Раздел II
- •§ 4.2. Основные закономерности, определения и классификация химических процессов
- •§ 4.3. Понятие о скорости и равновесии химических процессов
- •§ 4.4. Выход продукции в химико-технологических процессах
- •§ 4.5. Общие принципы интенсификации химико-технологических процессов
- •Перспективы развития и совершенствования химико-технологических процессов
- •Глава 5. Высокотемпературные процессы § 5.1. Сущность и значение высокотемпературных процессов
- •Влияние температуры на процессы, идущие в кинетической области
- •Влияние температуры на скорость процессов в диффузионной области
- •Условия, ограничивающие применение высоких температур
- •Типовое оборудование
- •§ 5.2. Тенденции совершенствования высокотемпературных процессов
- •§ 5.3. Высокотемпературные процессы в металлургии
- •Высокотемпературные процессы черных металлов в производстве
- •§ 5.4. Высокотемпературные процессы в производстве строительных материалов
- •§ 5.5. Высокотемпературная переработка топлива
- •Термические процессы переработки нефти и нефтяных фракций
- •§ 5.6. Высокотемпературные процессы в химической промышленности
- •Глава 6 электрохимические процессы § 6.1. Значение и сущность электрохимических процессов
- •Основные закономерности электрохимических процессов
- •§ 6.2. Электролиз водных растворов Электрохимическое производство хлора и едкого натра (каустической соды)
- •Электролиз воды
- •Электрохимическое производство продуктов окисления
- •§ 6.3. Гидроэлектрометаллургия
- •§ 6.4. Электролиз расплавленных сред
- •Свойства расплавленных электролитов
- •Глава 7 каталитические процессы § 7.1. Роль каталитических процессов, основные закономерности и определения
- •§ 7.2. Применение каталитических процессов в промышленности
- •§ 7.3. Производство аммиака
- •§ 7.4. Каталитические процессы нефтепереработки
- •Глава 8 процессы, идущие под повышенным или пониженным давлением § 8.1. Роль давления в технологии
- •§ 8.2. Давление как фактор интенсификации газообразных процессов
- •§ 8.3. Роль давления в жидкофазных и твердофазных процессах
- •Глава 9 биохимические процессы § 9.1. Основные понятия и определения
- •§ 9.2. Применение биотехнологических процессов в промышленности
- •Глава 10 фотохимические процессы
- •Глава 11 радиационно-химические процессы
- •Глава 12 плазмохимические процессы § 12.1. Общие понятия и определения
- •§ 12.2. Виды плазмохимических процессов
- •Глава 13 общие сведения о физических процессах химической технологии § 13.1. Значение физических процессов и их классификация
- •§ 13.2. Виды физических процессов Физико-механические процессы
- •Массообменные процессы
- •Раздел III
- •§ 14.2. Кислоты, щелочи Неорганические кислоты
- •§ 14.3. Минеральные удобрения
- •§ 14.4. Полимеры Общие сведения о полимерах, их строении, свойствах и способах получения
- •Пластмассы, их свойства, значение и применение в народном хозяйстве
- •Химические волокна и их применение в народном хозяйстве
- •Каучуки и резина
- •§ 14.5. Нефтепродукты
- •Глава 15 строительные материалы § 15.1. Общие сведения
- •§ 15.2. Основные виды строительных материалов Природные (естественные) материалы, применяемые в строительстве
- •Керамические материалы
- •Огнеупорные материалы
- •Минеральные вяжущие
- •Бетон, железобетон и строительные растворы
- •Силикатные (автоклавные) материалы
- •Асбестоцементные материалы
- •Стекло и изделия на его основе
- •Теплоизоляционные материалы
- •Глава 16 металлы и сплавы § 16.1. Общие сведения
- •§ 16.2. Методы определения качества металла (сплава)
- •§ 16.3. Термическая и химико-термическая обработка
- •§ 16.4. Черные металлы и сплавы
- •Материалы со специальными свойствами (стали, сплавы)
- •Магнитные материалы
- •Инструментальные материалы
- •§ 16.5. Цветные металлы и их сплавы
- •§ 16.6. Коррозия металлов
- •Классификация коррозионных процессов
- •Электрохимическая коррозия металлов
- •§ 16.7. Защита металлов от коррозии Защита металлов от химической коррозии
- •Экономия на 1 т листа
- •Защита металлов от электрохимической коррозии
- •Технико-экономические показатели и выбор методов защиты
- •Раздел IV
- •Типы производств
- •Типизация технологических процессов
- •Технологичность конструкций изделий
- •Качество изделий
- •Понятие о точности обработки
- •Основные методы и средства контроля качества изделий
- •Шероховатость поверхности
- •Выбор заготовок
- •§ 17.2. Экономическая оценка технологического процесса
- •Глава 18
- •Литье в песчано-глинистые формы
- •Специальные способы литья
- •§ 18.2. Основы технологии производства заготовок методами пластической деформации
- •Формообразование заготовок, изделий из пластмасс и резины методами пластической деформации
- •Формообразование деталей методами порошковой металлургии
- •§ 18.3. Изготовление неразъемных соединений Понятие о неразъемных соединениях. Виды неразъемных соединений
- •Сущность процессов сварки материалов и их классификация
- •Сварка плавлением
- •Огневая резка материалов
- •Сварка давлением
- •Контроль качества сварных соединений
- •Клеевая технология
- •§ 18.4. Обработка конструкционных материалов резанием
- •Обработка на станках-автоматах и полуавтоматах
- •Чистовая обработка наружных поверхностей тел вращения
- •Обработка внутренних поверхностей тел вращения.
- •Обработка плоских поверхностей
- •Обработка фасонных поверхностей
- •Методы изготовления деталей зубчатых зацеплений
- •Обработка резанием неметаллических материалов
- •Обработка заготовок на агрегатных станках
- •§ 18.5. Электрофизические методы обработки
- •Применение ультразвука в промышленности
- •Плазменная обработка материалов
- •Лазерная обработка
- •Глава 19 основные технологические процессы электроники и микроэлектроники § 19.1. Технология изготовления интегральных микросхем
- •Фотолитография в микроэлектронике
- •Нанесение тонких пленок в вакууме
- •Осаждение из газовой фазы
- •§ 19.2. Технология изготовления печатных плат
- •Технологические процессы изготовления пп
- •Субстрактивные методы изготовления печатных плат
- •Технология изготовления многослойных печатных плат
- •Аддитивные методы изготовления печатных плат
- •Печатные платы с многопроводным монтажом
- •Глава 20 технология сборочных процессов § 20.1. Понятие о технологическом процессе сборки и его организационных формах
- •§ 20.2. Контроль и испытание готовых изделий
- •Глава 21 основы технологии строительного производства § 21.1. Роль капитального строительства в развитии народного хозяйства ссср
- •§ 21.2. Строительные работы
- •§ 21.3. Основные направления совершенствования строительства
- •Глава 22 оптимизация технологических процессов § 22.1. Общая постановка задач оптимизации технологических процессов
- •§ 22.2. Методы оптимизации технологических процессов
- •Регрессионный и корреляционный методы анализа при оптимизации технологических процессов
- •Методы планирования эксперимента для оптимизации технологических процессов
§ 7.3. Производство аммиака
Для нормальной жизнедеятельности растений и животных азот необходим только в усвояемой форме. Однако из-за высокой химической инертности азота его неисчерпаемые ресурсы * живой природе практически недоступны. Для решения продовольственной проблемы человечество переводит азот в усвояемую форму, «связывая» его до простейшего соединения — аммиака, из которого затем получают азотную кислоту и минеральные удобрения.
Темпы роста производства аммиака постоянно увеличиваются. При этом количественный рост производства сопровождается качественными изменениями структуры производственной базы. Укрупняются мощности единичных агрегатов синтеза аммиака **6 внедряются новые эффективные катализаторы и сорбенты, разрабатываются прогрессивное оборудование и технологические схемы, обеспечивающие более полное использование сырья и топлива. В последние годы за счет лучшей утилизации теплоты производство аммиака удается организовать по энерготехнологическому принципу, в котором процесс полностью самообеспечивает себя паром и механической энергией.
Производство аммиака состоит из трех стадий: получение азотоводородной смеси, ее очистка и собственно синтез аммиака.
Первая стадия — получение азотоводородной смеси. Сырьем для производства аммиака являются азот и водород. Азот выделяют из воздуха — газовой смеси, содержащей по объему 78,05% азота, 20,95% кислорода, 0,94% аргона и в незначительных количествах углекислый газ, неон, гелий, криптон и ксенон. Для этого воздух глубоким охлаждением переводят в жидкое состояние, а затем ректификацией, основанной на различии температур кипения отдельных газов, разделяют на составные части.
Водород получают одним из способов: электролизом воды или водных растворов поваренной соли; из коксового газа последовательным сжижением всех его компонентов, кроме водорода; конверсией оксида углерода генераторного газа; конверсией метана или его гомологов.
Получение водорода — наиболее дорогая стадия производства. В настоящее время большую часть водорода для синтеза аммиака получают из наиболее дешевых видов сырья — газов, содержащих метан и его гомологи. К ним относятся попутные газы нефтедобычи, природный газ, газы нефтепереработки. В присутствии водяного пара и кислорода метан превращается в водород:
С Н4
+ Н2О
СО + Н2
- Q
Н4
+ Н2О
СО + Н2
- Q
С Н4+
0.5O2
СО + 2Н2
+ Q
Н4+
0.5O2
СО + 2Н2
+ Q
а образовавшийся оксид углерода конвертируется до СО2 и Н2:
С О
+ Н20
С02
+ Н2
+ Q
О
+ Н20
С02
+ Н2
+ Q
Конверсию природного газа проводят при атмосферном или повышенном давлении с применением катализаторов (каталитическая конверсия) или без них (высокотемпературная конверсия). Часто процесс на никелевом катализаторе ведут так, чтобы остаточная концентрация метана составляла 8 — 10%. При такой концентрации метана его дальнейшее конвертирование воздухом (т. е. смесью азота и кислорода в соотношении 4:1) позволяет получить сразу азотоводородную смесь с соотношением N2: Н2 = = 1:3. Это исключает необходимость строительства дорогостоящих и энергоемких установок разделения воздуха и значительно улучшает технико-экономические показатели процесса.
Однако полученные азот, водород и азотоводородная смесь загрязнены попавшими из природного газа соединениями серы, а также оксидами и диоксидами углерода, образовавшимися при конверсии. Из-за высокой чувствительности катализатора синтеза аммиака к этим примесям, сильно снижающим его активность и вызывающим необратимые отравления (особенно соединения, содержащие серу), газ подвергают тщательной очистке.
Вторая стадия — очистка газа. Для удаления примесей сернистых соединенийтипа сероуглерода CS2, сероокиси углерода COS и меркаптанов R —SH их гидрируют на кобальтмолибденовом катализаторе при температуре 350-450 °С до легкоулавливаемого сероводорода
9 Н2
+ примеси
(CS2
+ COS + R - SH) 4H2S
+ 2CH4
4+ H2O
Н2
+ примеси
(CS2
+ COS + R - SH) 4H2S
+ 2CH4
4+ H2O
Образовавшийся сероводород удаляют из газа с помощью различных поглотителей, например оксида цинка: ZnO + H2S ZnS + Н2О
После такой очистки газ содержит сероводорода не более 1 мг/м3.
Очистка газа от СО2 производится с помощью жидких поглотителей. На смену водной очистке, потреблявшей большое количество воды и энергии на ее перекачку, пришла более эффективная очистка с помощью водных растворов этаноламинов либо горячих растворов поташа, активированных мышьяком. При промывке газа указанными водными растворами примеси СО2 образуют карбонаты и бикарбонаты. Регенерация поглотителей с удалением СО2 в десорбере производится: для этаноламинов — нагреванием до 120 °С, для растворов поташа — снижением давления.
Примеси СО удаляются из газа поглощением мед-ноаммиачным раствором слабой уксусной или муравьиной кислоты. Эффективность очистки увеличивается с повышением давления до 30 МПа и понижением температуры до 25 — 0 °С. После очистки в газе остается не более 0,003% СО. При очистке азотоводородной смеси, получаемой из коксового газа, остатки СО удаляют промывкой жидким азотом. При этом часть азота испаряется и переходит в азотоводородную смесь, обеспечивая соотношение N2 : Н2, близкое 1:3. Разбавляя смесь дополнительным количеством азота, ее доводят до необходимого для синтеза аммиака точного соотношения N2: Н2 = 1:3. В тех случаях, когда остаточные количества СО и СО2 в газе небольшие (до 1 %), удаление примесей осуществляется их гидрированием (метанирова-нием) по реакциям
С
 О
+ ЗН2
СН4
+ Н2О;
СО2
+ 4Н2
СН4
+ 2Н2О
О
+ ЗН2
СН4
+ Н2О;
СО2
+ 4Н2
СН4
+ 2Н2О
Температура процесса 200 — 400 °С, катализатор — никель, нанесенный на оксид алюминия.
Третья стадия — синтез аммиака. Образование аммиака по реакции
N 2+3H2
2NH3
+ Q
протекает
достаточно быстро только в присутствии
катализаторов, содержащих в качестве
активаторов оксиды алюминия, калия и
кальция. Тепловой эффект реакции растет
с увеличением температуры, а равновесный
выход зависит не только от температуры,
но и от давления.
2+3H2
2NH3
+ Q
протекает
достаточно быстро только в присутствии
катализаторов, содержащих в качестве
активаторов оксиды алюминия, калия и
кальция. Тепловой эффект реакции растет
с увеличением температуры, а равновесный
выход зависит не только от температуры,
но и от давления.
Синтез аммиака является обратимым экзотермическим процессом. В соответствии с принципом Ле-Шателье отвод теплоты должен смещать реакцию вправо. С этой целью промежуточное охлаждение газовой смеси менее нагретым встречным потоком производится после каждого ее контакта с катализатором. Это обеспечивает автотермичность процесса. Однако несмотря на отвод теплоты, температура по ходу процесса все же несколько увеличивается. Поэтому в колонне синтеза аммиака используются катализаторы, эффективно работающие в различных диапазонах температур.
Современные колонны синтеза аммиака большой единичной мощности имеют четыре полки с катализаторами. На первой (по ходу газа) находится низкотемпературный катализатор (350— 500 °С), на второй — средне-температурный (400 —550 °С); на третьей и четвертой — высокотемпературные (550 — 700 °С).
На фактический выход аммиака кроме перечисленных факторов оказывают влияние активность катализатора, состав газовой смеси, конструктивные особенности аппарата (чем меньше в них гидравлическое сопротивление, тем выше пропускная способность и ниже энергетические затраты) и продолжительность соприкосновения газа с катализатором (или обратная величина, называемая объемной скоростью газа). С увеличением объемной скорости съем аммиака с 1 м3 контактной массы резко возрастает. Но одновременно с этим увеличивается объем непрореагировавшей азотоводородной смеси. Во избежание потерь эту смесь необходимо многократно прокачивать через катализатор по замкнутому циклу. Это повышает расход энергии на перекачку. С экономической точки зрения подобные затраты могут быть сведены к минимуму при некоторых оптимальных значениях объемной скорости газа (от 15000 до 30000 м3 газовой смеси через 1 м3 катализатора в час).
Технико-экономические показатели этого производства могут быть улучшены переходом к энерго-, ресурсо-и трудосберегающей технологии. Это достигается применением агрегатов большой единичной мощности, маловодных схем и АСУТП. Особое внимание уделяется утилизации теплоты топочных газов, выходящих из печи нагрева метана, а также газовых потоков, покидающих реактор гидрирования органической серы, конвертеры метана и оксида углерода, колонны синтеза аммиака, метанатора и т. д.
Утилизированная высокопотенциальная теплота используется для получения пара высокого давления. Энергия этого пара в турбинах преобразуется в механическую для сжатия и перемещения газов с помощью компрессоров. Низкопотенциальная теплота утилизируется для получения технологического пара низкого давления, подогрева воды, получения холода и т. п. Подобный принцип энергосбережения самообеспечивает процесс паром и механической энергией. Для районов, испытывающих недостаток в топливе, это позволяет организовать производство с минимальными энергозатратами. Замена же водяного охлаждения воздушным значительно сокращает и водопотребление. Указанные принципы используются в современных схемах производства аммиака на агрегатах большой (1500 т/сут) единичной мощности. Один такой агрегат обеспечивает годовую экономию эксплуатационных затрат в сумме 15 млн. руб. и капиталовложений до 25 млн. руб. Указанная схема включает блоки получения азотоводородной смеси, очистки газа и синтеза аммиака.
Рис. 7,6
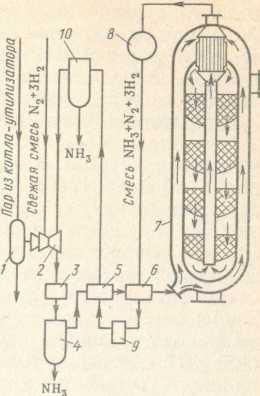
и направляется в полочную колонну синтеза 7. По сравнению с традиционным контактным аппаратом с двойной теплообменной трубкой в полочных радиальных колоннах гидравлическое сопротивление, а следовательно, и энергопотери значительно снижены. В такой колонне с внутренним диаметром до 2,1 м, высотой до 25 м и толщиной стенок из хромомолибденовой стали 10 — 30 см имеется четыре полки. Полки загружаются катализатором в возрастающем количестве и с возрастающим диапазоном рабочих температур от первой к последней.
Для поддержания заданного температурного режима по высоте колонны после каждой полки производят отвод теплоты экзотермической реакции в котел-утилизатор. Тонкое регулирование температуры достигается введением в горячую газовую смесь определенного количества холодной смеси.
Примерно 15-20% азотоводородной смеси на катализаторе превращается в аммиак. Выйдя из колонны синтеза с температурой 320 — 380 °С, смесь последовательно отдает теплоту питательной воде котла-утилизатора в водоподогревателе 8, а затем нагревает встречный холодный газовый поток в «горячем» теплообменнике 6. Далее она охлаждается в аппарате воздушного охлаждения 9 и «холодном» теплообменнике 5. При давлении около 30 МПа в такой газовой смеси аммиак конденсируется уже при температуре 25 — 40 °С и после отделения в сепараторе 10 направляется в хранилище.
Газовая смесь, содержащая до 2 - 3 % несконденсировавшегося аммиака, и непрореагировавшие азот и водород турбокомпрессором 2 возвращаются в производственный цикл.
Степень превращения азотоводородной смеси в аммиак в колонне синтеза колеблется от 15 до 20%. Но благодаря многократной ее циркуляции по замкнутой схеме фактический выход аммиака в системах среднего давления составляет 91 — 95%. По сравнению с системами, работающими при низком (10 МПа) и высоком (100 МПа) давлении, в системах среднего давления, получивших в мировой практике наибольшее распространение, удачно решаются вопросы выделения аммиака при достаточной скорости процесса в контактном аппарате. Помимо жидкого аммиака получают и газообразный, который обычно тут же перерабатывается в мочевину, аммиачную селитру, азотную кислоту.
