
teplotech
.pdfГОСУДАРСТВЕННЫЙ КОМИТЕТ РОССИЙСКОЙ ФЕДЕРАЦИИ ПО ВЫСШЕМУ ОБРАЗОВАНИЮ
ВОЛГОГРАДСКИЙ ГОСУДАРСТВЕННЫЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ
КАФЕДРА "ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ТЕПЛОТЕХНИКИ"
ПОСТРОЕНИЕ КРИВОЙ НАСЫЩЕНИЯ И ОПРЕДЕЛЕНИЕ ТЕПЛОТЫ ПАРООБРАЗОВАНИЯ
Методические указания к лабораторной работе
Волгоград
2003
2
Построение кривой насыщения и определение теплоты парообразования. Методические указания к лабораторной работе / Сост. А.А. Буров, Г.Н. Злотин, Е.А. Федянов. - 3-е изд., доп. и перераб. – Волгоград. гос. техн. ун-т. – Волгоград, 2003. – 11 c.
Даются цели и содержание лабораторной работы по экспериментальному определению параметров насыщения для воды и водяного пара. Рассматриваются основные методы определения этих параметров. Описывается лабораторная установка. Излагается рекомендуемая методика выполнения работы, обработки и анализа результатов. Приводятся вопросы для самоконтроля.
Ил. 3. Табл. 1. Библиогр.: 4 назв.
Рецензент Е.А. Захаров
Печатается по решению редакционно-издательского совета Волгоградского государственного технического университета
Волгоградский государственный технический университет, 2003
3
1. ЦЕЛЬ РАБОТЫ
1.1.Изучение методов экспериментального определения зависимости между температурой и давлением насыщения.
1.2.Определение теплоты парообразования и ее зависимости от температуры насыщения.
1.3.Углубление знаний о свойствах реальных газов, в частности водяного пара.
2. СОДЕРЖАНИЕ РАБОТЫ
2.1.Экспериментальное определение значений температуры насыщения для воды и водяного пара при различных давлениях. Сравнение полученных данных с табличными.
2.2.Построение кривой насыщения в исследованной области изменения параметров.
2.3.Определение с помощью кривой насыщения теплоты парообразования для воды и анализ зависимости ее величины от температуры насыщения.
3.МЕТОДЫ ОПРЕДЕЛЕНИЯ ПАРАМЕТРОВ НАСЫЩЕНИЯ И ТЕПЛОТЫ ПАРООБРАЗОВАНИЯ
Для получения зависимости давления насыщенного пара от его температуры используются различные методы. Наибольшее распространение получили статические методы и метод точек кипения.
3.1. Статические методы
Суть статических методов заключается в следующем. Исследуемое вещество помещается в термостатированный сосуд, из которого предварительно удален воздух. После того, как в сосуде устанавливается равновесие между конденсированной фазой и паром, измеряется либо давление в сосуде (прямой метод), либо количество вещества, перешедшее в паровую фазу (косвенный метод).
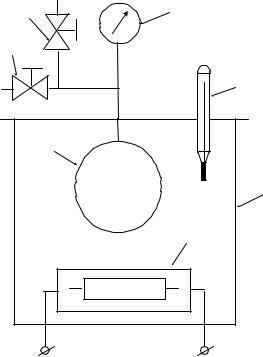
На рис.3.1. показана схема установки, в которой реализуется прямой статический метод. Исследуемое вещество находится в сосуде 1, который помещен в термостат 2. Заданная температура в термостате поддерживается нагревателем 3. Давление в сосуде измеряется мановакуумметром 4, а температура - термометром 5. Вентили 6 и 7 используется для вакуумирования сосуда и заполнения его исследуемым веществом.
|
4 |
6 |
4 |
7 |
|
|
5 |
|
1 |
|
2 |
|
3 |
Рис. 3.1. Схема установки для определения параметров насыщения статическим методом
Давление насыщенного пара однозначно определяется температурой на границе между паром и жидкостью. Поэтому при использовании статических методов важно обеспечить хорошее термостатирование с тем, чтобы температура, измеренная термометром 5, соответствовала бы температуре исследуемого вещества на границе раздела фаз.
3.2. Метод точек кипения
Определение давления и температуры насыщенного пара методом точек кипения основано на том, что при равенстве внешнего давления давлению насыщенного пара жидкость закипает. При реализации этого метода исследуемая жидкость помещается в сосуд (рис. 4.1), который, в отличие от статического метода, предварительно не вакуумируется. Свободное пространство над жидкостью в нем заполнено воздухом или другим инертным газом. Устанавливая с помощью вакуумного насоса или компрессора различные давления газа в сосуде и нагревая жидкость, фиксируют тем или иным способом, например визуально, момент закипания. Значения давления и температуры в сосуде в этот момент соответствуют давлению и температуре насыщения для исследуемой жидкости. Так как кипящая жидкость может быть перегрета, температуру в сосуде измеряют над ее поверхностью, т.е. в области пара.

5
Вданной лабораторной работе используется метод точек кипения.
3.3.Метод определения теплоты парообразования
Парообразование является разновидностью ходов. Для этих процессов справедливо Клаузиуса:
dp |
= |
qфп |
|
, |
|
T |
|
||
dT |
v |
|||
процессов фазовых переуравнение Клайперона-
(3.1)
где |
p – давление; T – температура; qфп – теплота фазового перехода; |
||||||
v – разность удельных объемов фаз. |
|
||||||
|
Если использовать обозначения, |
принятые для водяного пара, то |
|||||
уравнения (3.1) приобретает вид |
|
||||||
|
|
dp |
|
r |
|
||
|
|
|
= |
|
|
, |
(3.2) |
|
|
dT |
T |
(v′′ − v′) |
|||
|
|
|
|
н |
|
|
|
где |
r – теплота парообразования; Tн |
– температура насыщения; v′′ – уде- |
|||||
льный объем сухого насыщенного пара; v′ – удельный объем кипящей жидкости.
Формулу (3.2) используют при исследованиях термодинамических свойств воды и водяного пара для определения удельных объемов или теплоты парообразования. Так, например, если при некоторой заданной температуре Tн каким-либо образом найдены значения производной dp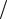 dT и
dT и
удельных объемов, то по формуле (3.2) можно рассчитать величину теплоты парообразования r . В области малых давлений насыщения, в которой v′′ >> v′ , величиной v′ можно пренебречь. Тогда
dp |
= |
r |
, |
(3.3) |
|
T v′′ |
|||
dT |
|
|
||
|
|
н |
|
|
+a ( − ) =
p v b R T . (3.4)
v2
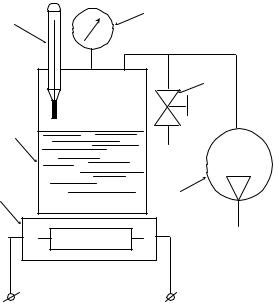
Вуравнении (3.4) характеристическая газовая постоянная R есть отношение универсальной газовой постоянной к молярной массе водяного пара, а значения коэффициентов a и b берутся из справочной литературы или вычисляются через параметры вещества в критической точке:
|
|
|
|
|
|
|
6 |
|
|
|
27 |
|
R2 T 2 |
1 |
|
R T |
|
||
a = |
|
|
к |
; b = |
|
|
к |
. |
(3.5) |
64 |
|
8 |
|
||||||
|
|
pк |
|
pк |
|
||||
Для воды и водяного пара pк |
= 22,13 МПа, Tк |
= 647,3 К. |
|||||||
4. ОПИСАНИЕ ЛАБОРАТОРНОЙ УСТАНОВКИ Установка (рис.4.1) представляет собой частично заполненную водой
стеклянную колбу (1), установленную на нагревательном устройстве (2). Пространство над колбой соединено с вакуумным струйным насосом (3).
Величина вакуума может регулироваться с помощью игольчатого вентиля (4), соединяющего пространство колбы с атмосферой. С помощью вакуумметра (5) и термометра (6) измеряются давление в колбе и температура паровой фазы. При выполнении лабораторной работы необходимо выполнять следующие правила техники безопасности:
1)включение нагревательного устройства и вакуумного насоса производить только с разрешения преподавателя;
2)запрещается включать лабораторную установку при отсутствии на ней защитного экрана;
3)перед включением установки убедиться в отсутствии трещин на колбе
икорпусе вакуумного насоса, а также в отсутствии влаги на нагревательном устройстве;
5
6
4
1
3
2
Рис. 4.1. Схема лабораторной установки: 1 – колба; 2 – нагреватель; 3 – водоструйный вакуумный насос; 4 – регулировочный вентиль; 5 – вакууметр; 6 – термометр
7
4)запрещается оставлять включенную установку без присмотра;
5)при обнаружении каких-либо неисправностей в установке необходимо ее немедленно отключить и поставить об этом в известность преподавателя или лаборанта.
5.МЕТОДИКА ПРОВЕДЕНИЯ ЭКСПЕРИМЕНТА И ОБРАБОТКИ РЕЗУЛЬТАТОВ
5.1. Методика проведения эксперимента.
5.1.1.Измерить атмосферное давление и температуру воздуха в лабо-
ратории.
5.1.2.Включить нагреватель и после того, как температура, которую показывает установленный в колбе термометр, начнет повышаться, создать над поверхностью воды в колбе максимально возможное разрежение. Для этого пустить воду в струйный насос при полностью закрытом регулировочном вентиле.
5.1.3.Наблюдать за поведением воды и в момент ее закипания измерить температуру пара и величину разрежения в колбе. Результаты измерений поместить в таблицу 5.1.
5.1.4.С помощью регулировочного вентиля последовательно уменьшать примерно на 10 кПа разрежение в колбе, измеряя при каждом новом значении давления температуру пара в момент закипания жидкости. Всего получить таким образом 6..8 пар соответствующих друг другу значений
разрежения pн вак и температуры насыщения |
tн . Полученные значения |
|||||||||||||
занести в таблицу 5.1. |
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
Таблица 5.1 |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Номер |
|
|
pн вак |
|
tн |
pн |
|
Tн |
v′′ |
|
r |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
точки |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кгс |
|
Па |
°С |
Па |
|
К |
м |
3 |
|
кДж |
||
|
|
|
|
|
|
|
|
|
|
|||||
|
|
см2 |
|
|
кг |
|
кг |
|||||||
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

8
6. ОБРАБОТКА РЕЗУЛЬТАТОВ ЭКСПЕРИМЕНТА
6.1. Вычисляются значения абсолютных давлений и температур:
pн |
= pатм − pн вак , |
(6.1) |
Tн |
= tн + 273,15 . |
(6.2) |
6.2. По уравнению Ван-дер-Ваальса находятся значения v′′ . Для решения уравнения Ван-дер-Ваальса рекомендуется использовать один из численных методов. В частности, можно воспользоваться специальной программой, которая имеется в ЭВМ, установленной в лаборатории. Перед запуском программы необходимо найти по справочнику или вычислить значения характеристической газовой постоянной и коэффициентов a и b для водяного пара. При вычислениях необходимо согласовывать размерность давлений и газовой постоянной в формулах (3.4) и (3.5). Если в эти формулы давления подставляются в Па, то размерность характеристической газовой постоянной R должна быть Дж/(кг К).
6.3.Строится кривая насыщения pн = f(Tн ) и исходя из ее вида делается вывод о характере взаимосвязи pн и Tн .
6.4.Используя полученную зависимость pн = f(Tн ) , найти для всех измеренных значений Tн , кроме минимального и максимального, величину производной dp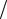 dT . Для нахождения производной можно воспользоваться
dT . Для нахождения производной можно воспользоваться
одним из известных методов численного дифференцирования. Некоторые из этих методов представлены в математических пакетах программ для ЭВМ. Кроме того, можно применить графический способ, то есть определять производные по величине углов наклона касательных к кривой насыщения в точках с заданной температурой Tн . При этом следует помнить,
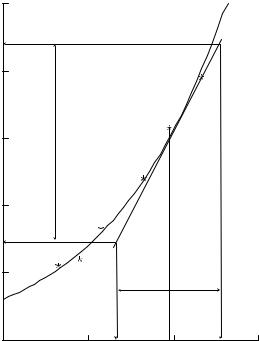
что тангенс угла наклона касательной должен быть вычислен с учетом масштабов, принятых на графике для температур и давлений. Графический способ нахождения dp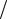 dT иллюстрируется рис. 6.1. На этом рисунке
dT иллюстрируется рис. 6.1. На этом рисунке
в качестве примера показано определение значения dp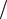 dT при температуре
dT при температуре
насыщения в экспериментальной точке 1. Касательная AB проводится к кривой насыщения в той ее точке 1', которая соответствует значению температуры насыщения в экспериментальной точке. На касательной выбираются произвольно точки A и B. По значениям давлений и температур в
этих точках находятся разности p и |
T . В данном примере p = 60 кПа, |
T = 26 К и, следовательно, dp dT ≈ |
p T = 2,3 кПа/К. |
6.4. По уравнению Клайперона-Клаузиуса (3.3) рассчитываются теплоты парообразования для заданных значений температуры насыщения. Проводится сравнение полученных значений со справочными табличными данными [1, 4].
|
|
|
9 |
|
|
100 |
|
|
|
|
|
|
|
B |
|
80 |
|
|
|
кПа |
|
|
|
|
насыщения, |
|
|
1 |
|
60 |
p |
1' |
|
|
|
|
|||
|
|
|
|
|
Давление |
40 |
|
|
|
|
|
A |
|
|
|
|
|
|
|
|
20 |
|
T |
|
|
|
|
|
|
|
0 |
|
|
|
|
320 |
340 |
360 |
380 |
|
|
Температура насыщения, К |
|
|
Рис. 6.1. Пример определения производной dp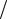 dT графическим способом
dT графическим способом
6.5.Результаты всех расчетов заносятся в таблицу 5.1.
6.6.Строится график зависимости теплоты парообразования от температуры насыщения. Делается вывод о характере полученной зависимости.
7. СОДЕРЖАНИЕ ОТЧЕТА
7.1.Отчет оформляется на листах формата А4 в соответствии с образцами, имеющимися в лаборатории.
7.2.Отчет должен содержать:
1)цель работы;
2)схему установки;
3)таблицу 5.1;
4)кривую насыщения и вывод о характере взаимосвязи pн и Tн .
5)необходимые вычисления или графические построения по определению производных dp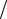 dT ;
dT ;
6)график зависимости теплоты парообразования от температуры на-
сыщения.
10
8.ВОПРОСЫ ДЛЯ САМОКОНТРОЛЯ
1.Какие свойства реальных газов не учитываются в модели идеального га-
за?
2.Как записывается уравнение Ван-дер-Ваальса? Чем это уравнение отличается от уравнения состояния идеального газа?
3.Что такое критическая точка вещества?
4.При каких условиях можно путем изотермического сжатия перевести вещество из газообразного состояния в жидкое?
5.Какой пар называется насыщенным?
6.Как выглядит изображение процесса парообразования при p = const в
pv- и Ts- координатах?
7.Чем отличаются сухой пар от влажного? Что понимается под степенью сухости ?
8.Что такое теплота парообразования?
9.Как записывается уравнение Клайперона-Клаузиуса?
10.Как определяются параметры состояния пара при инженерных расчетах?
11.Как определить удельный объем, энтальпию, энтропию и внутреннюю энергию влажного водяного пара с помощью таблиц?
12.Какие экспериментальные методы применяются для определения параметров насыщения?
СПИСОК РЕКОМЕНДУЕМОЙ ЛИТЕРАТУРЫ
1.Нащокин В.В. Техническая термодинамика и теплопередача.– М.: Высшая школа, 1980.– С. 161–172.
2.Юдаев Б.Н. Техническая термодинамика. Теплопередача.– М.: Высшая школа, 1988.– С. 85–100.
3.Техническая термодинамика./ Под редакцией Крутова В.И. – М.: Высшая школа, 1971. – С. 231–261.
4.Вукалович М.П. Теплофизические свойства воды и водяного пара.– М.: Машиностроение, 1967.– 160 с.
