
б.х. 11-20
.doc11. Молочная кислота (лактат). Лактат является метаболическим продуктом анаэробного гликолиза и в нормальных условиях находится в равновесии с его непосредственным предшественником пируватом. Лактат образуется из пирувата в качестве конечного продукта анаэробного гликолиза. Эта окислительно-восстановительная реакция требует восстановленного никотинамидаденин-динуклеотида (NADH) и иона водорода (Н+) и катализируется лактатдегидрогеназой (ЛДГ). Реакция выражается следующим уравнением: Пируват + NADH+ЛДГ H+ *=t Лактат + NAD. Лактат может элиминироваться только путем превращения в пируват, концентрация лактата тесно связана с судьбой пирувата. Печень и почки являются основными органами, потребляющими лактат. При изъятии лактата главным метаболическим путем, используемым этими органами, становится глюконеогенез. Почки осуществляют клиренс лактата в основном через глюконеогенез. Скелетная мускулатура и миокард способны поглощать некоторое количество лактата из циркуляции; значение этого пути клиренса не представляется достаточно ясным. Утилизация лактата скелетной мускулатурой может зависеть от концентрации лактата в крови и от состояния (активного или пассивного) мышцы.
Молочнокислый ацидоз может рассматриваться как нарушение равновесия между скоростью продукции лактата в тканях с активным гликолизом и скоростью его утилизации тканями с активным глюконеогенезом.
12. Гликолиз - это анаэробный процесс. При расчете энергетического эффекта биохимического процесса в анаэробных условиях следует учитывать:
1) затраты АТФ (как правило, в фосфотрансферазных реакциях);
2) образование АТФ в процессах субстратного фосфорилирования.
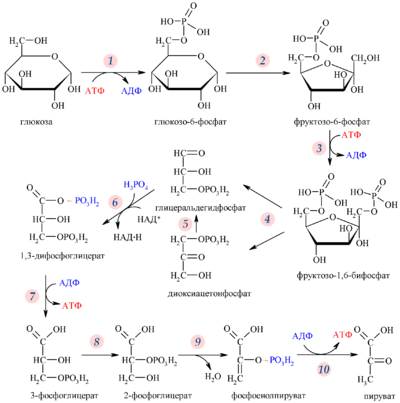
В первом этапе гликолиза происходит затрата 2 моль АТФ: на фосфорилирование глюкозы и на фосфорилирование глюкозо-6-фосфата. Еще раз заострим внимание на том, что из 1 моль глюкозы образуется 2 моль 3-фосфоглицеринового альдегида, который вступает во второй этап гликолиза.
Во втором этапе гликолиза можно найти две реакции субстратного фосфорилирования, в которых образуется 2 моль АТФ при распаде 1 моль 3-фосфоглицеринового альдегида. Следовательно, при распаде 2 моль 3-фосфоглицеринового альдегида образуется 4 моль АТФ. Суммируя полученное и затраченное количество АТФ, получаем суммарный энергетический эффект гликолиза - 2 моль АТФ.
13. Ключевые ферменты гликолиза.
1. Гексокиназа — это регуляторный фермент гликолиза во внепеченочных клетках. Гексокиназа аллостерически ингибируется глюкозо-6-фосфатом. Глюкокиназа — регуляторный фермент гликолиза в гепатоцитах. Синтез глюкокиназы индуцируется инсулином.
2. Фосфофруктокиназа-1. Это главный ключевой фермент, катализирует реакцию, лимитирующую скорость всего процесса (наиболее медленная реакция). Синтез фермента индуцируется инсулином. Аллостерические активаторы — АМФ, АДФ, фруктозо-2,6- дифосфат. Уровень фруктозо-2,6-дифосфата увеличивается под действием инсулина и понижается под действием глюкагона. Аллостерические ингибиторы — АТФ, цитрат.
3. Пируваткиназа. Фермент активен в нефосфорилированной форме. Глюкагон (в гепатоцитах) и адреналин (в миоцитах) стимулируют фосфорилирование фермента, а значит инактивируют фермент. Инсулин, наоборот, стимулирует дефосфорилирование фермента, а значит активирует фермент. Аллостерический активатор — Фр-1,6-ФФ. Аллостерический ингибитор — АТФ, ацетил КоА. Синтез фермента индуцирует инсулин.
Аллостерическая регуляция скорости гликолиза, зависимая от изменения соотношения АТФ/АДФ, направлена на изменение скорости использования глюкозы непосредственно клетками печени. Глюкоза в клетках печени используется не только для синтеза гликогена и жиров, но также и как источник энергии для синтеза АТФ. Основными потребителями АТФ в гепатоцитах являются процессы трансмембранного переноса веществ, синтез белков, гликогена, жиров, глюконеогенез. От скорости утилизации АТФ в этих процессах зависит скорость его синтеза. АТФ, АДФ и АМФ, а также NAD+ и NADH служат аллостерическими эффекторами некоторых гликолитических ферментов и ферментов глюконеогенеза. В частности, АМФ активирует фосфофруктокиназу и ингибирует фруктозо-1,6-бисфосфатазу. АТФ и NADH ингибируют пируваткиназу, а АДФ активирует пируваткарбоксилазу.
14. Глико́лиз (фосфотриозный путь, или шунт Эмбдена — Мейерхофа, или путь Эмбдена-Мейергофа-Парнаса ) — ферментативный процесс последовательного расщепления глюкозы в клетках, сопровождающийся синтезом АТФ. Гликолиз при аэробных условиях ведёт к образованию пировиноградной кислоты (пирувата), Гликолиз является основным путём катаболизма глюкозы в организме животных и человека.
Аэробный распад глюкозы можно выразить суммарным уравнением:
С6Н12О6 + 6 О2 → 6 СО2 + Н2О + 2820 кДж/моль.
Этот процесс включает несколько стадий:
-
Аэробный гликолиз - процесс окисления глюкозы с образованием двух молекул пирувата;
-
Общий путь катаболизма, включающий превращение пирувата в ацетил-КоА и его дальнейшее окисление в цитрантом цикле;
-
ЦПЭ на кислород, сопряжённая с реакциями дегидрирования, происходящими в процессе распада глюкозы.
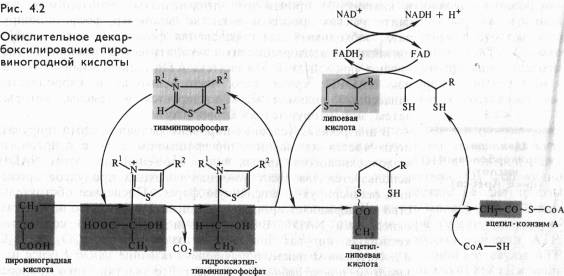
15. Окислительное декарбоксилирование ПВК катализирует пируватдегидрогеназа. В состав пируватдегидрогеназного комплекса входит несколько структурно связанных ферментных белков и коферментов. ТПФ (Тиаминпирофосфат) катализирует начальную реакцию декарбоксилирования ПВК. Эта реакция идентична катализируемой пируватдекарбоксилазой. Однако в отличие от последней, пируватдегидрогеназа не превращает промежуточный продукт гидроксиэтил-ТПФ в ацетальдегид. Вместо этого гидроксиэтильная группа переносится к следующему ферменту в мультиферментной структуре пируватдегидрогеназного комплекса.
Окислительное декарбоксилирование ПВК является одной из ключевых реакций в обмене углеводов. В результате этой реакции ПВК, образовавшаяся при окислении глюкозы, включается в главный метаболический путь клетки — цикл Кребса, где окисляется до углекислоты и воды с выделением энергии. Таким образом, благодаря реакции окислительного декарбоксилирования ПВК создаются условия для полного окисления углеводов и утилизации всей заключенной в них энергии. Кроме того, образующаяся при действии ПДГ-комплекса активная форма уксусной кислоты служит источником для синтеза многих биологических продуктов: жирных кислот, холестерина, стероидных гормонов, ацетоновых тел и других.
Пируватдегидрогеназный комплекс (ПДК) — комплекс трех ферментов, который осуществляет окислительное декарбоксилирование пирувата. Продуктами окисления являются углекислый газ, ацетил-КоА, НАДН.Н+.
Пируватдегидрогеназный комплекс включает в себя 3 фермента, 3 кофактора (простетическая группа, связанная с апоферментом прочно ковалентно), 2 кофермента (простетическая группа, связанная с апоферментом непрочно нековалентно):
-
Е1 — пируватдегидрогеназа декарбоксилирующая.
Кофактором является активная форма витамина В1 — тиаминпирофосфат.
-
Е2 — дигидролипоилацетилтрансфераза.
Кофактором является витаминоподобное вещество — липоевая кислота, которая присоединив 2 атома водорода может превращаться в дигидролипоил.
Коферментом является активная форма пантотеновой кислоты — НS-КоА, она принимает ацетильный остаток от липоевой кислоты.
-
Е3 — дигидролипоилдегидрогеназа .
Кофактором является флавинадениндинуклеотид (ФАД) — активная форма витамина В2.
Коферментом является активная форма витамина PP — никотинамидадениндинуклеотид (НАД+).
СН3-СО-СООН + НS-КоА + НАД+ => СО2 + СН3-СО~SKoA + НАДН.Н+
Суммарное уравнение
Последовательность реакций, катализируемых
ПДК.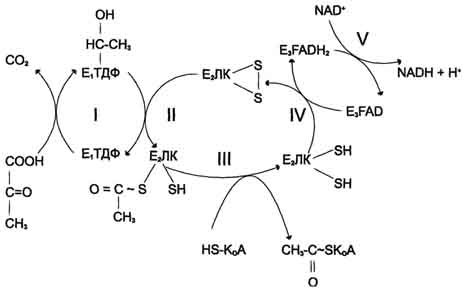
16. Энергетическое значение аэробного распада глюкозы.
При аэробном окислении 1 молекулы глюкозы образуется 2 молекулы ПВК, которые диффундируют в митохондрии и подвергаются окислительному декарбоксилированию с образованием 2 молекул АУК. При этом образуется 2 молекулы НАДН2, которые окисляются в БО, давая 6 АТФ. 2 АУК окисляются в ЦТК, давая 6 НАДН2, 2ФПН2 и 2АТФ, что в сумме даст 24 АТФ. Т.о., в митохондриях получается 24+6=30АТФ.
Значение: Гликолиз — катаболический путь исключительной важности. Он обеспечивает энергией клеточные реакции, в том числе и синтез белка. Промежуточные продукты гликолиза используются при синтезе жиров. Пируват также может быть использован для синтеза аланина, аспартата и других соединений. Благодаря гликолизу производительность митохондрий и доступность кислорода не ограничивают мощность мышц при кратковременных предельных нагрузках.
Жиры синтезируются только при наличии энергии. убстратом для синтеза жиров de novo является глюкоза.
Как известно, попадая в клетку, глюкоза превращается в гликоген, пентозы и окисляется до пировиноградной кислоты. При высоком поступлении глюкоза используется для синтеза гликогена, но этот вариант ограничивается объемом клетки. Поэтому глюкоза "проваливается" в гликолиз и превращается в пируват либо напрямую, либо через пентозофосфатный шунт. Во втором случае образуется НАДФН, который понадобится впоследствии для синтеза жирных кислот.
17. Глюконеогенез – синтез глюкозы из неуглеводных продуктов. Такими продуктами или метаболитами являются в первую очередь молочная и пи-ровиноградная кислоты, так называемые гликогенные аминокислоты, гли-церол и ряд других соединений. Иными словами, предшественниками глюкозы в глюконеогенезе может быть пируват или любое соединение, превращающееся в процессе катаболизма в пируват или один из промежуточных продуктов цикла трикарбоновых кислот.
У позвоночных наиболее интенсивно глюконеогенез протекает в клетках печени и почек (в корковом веществе).
Большинство стадий глюконеогенеза представляет собой обращение реакции гликолиза. Только 3 реакции гликолиза (гексокиназная, фосфо-фруктокиназная и пируваткиназная) необратимы, поэтому в процесс глю-конеогенеза на 3 этапах используются другие ферменты.
Образование фосфоенолпирувата из пирувата. Синтез фосфоенолпирувата осуществляется в несколько этапов. Первоначально пируват под влиянием
пируваткарбоксилазы и при участии СО2 и АТФ карбоксилируется с образованием оксалоацетата:

Затем оксалоацетат в результате декарбоксилирования и фосфорили-рования под влиянием фермента фосфоенолпируваткарбоксилазы превращается в фосфоенолпируват. Донором фосфатного остатка в реакции служит гуанозинтрифосфат (ГТФ):
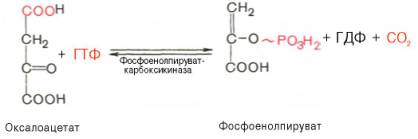
Первый этап синтеза протекает в митохондриях (рис. 10.6). Пируват-карбоксилаза, которая катализирует эту реакцию, является аллостери-ческим митохондриальным ферментом. В качестве аллостерического активатора данного фермента необходим ацетил-КоА. Мембрана митохондрий непроницаема для образовавшегося оксалоацетата. Последний здесь же, в митохондриях, восстанавливается в малат:

Реакция протекает при участии митохондриальной НАД-зависимой малатдегидрогеназы. В митохондриях отношение НАДН/НАД+ относительно велико, в связи с чем внутримитохондриальный оксалоацетат легко восстанавливается в малат, который легко выходит из митохондрии через митохондриальную мембрану. В цитозоле отношение НАДН/НАД+ очень мало, и малат вновь окисляется при участии цитоплазматической НАД-за-висимой малатдегидрогеназы:
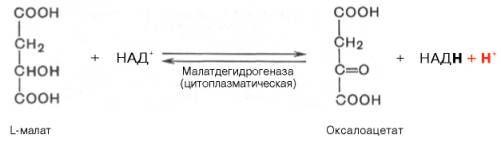
Дальнейшее превращение оксалоацетата в фосфоенолпируват происходит в цитозоле клетки.
Превращение фруктозо-1,6-бисфосфата во фруктозо-6-фосфат. Фосфо-енолпируват, образовавшийся из пирувата, в результате ряда обратимых реакций гликолиза превращается во фруктозо-1,6-бисфосфат. Далее следует фосфофруктокиназная реакция, которая необратима. Глюконеогенез идет в обход этой эндергонической реакции. Превращение фруктозо-1,6-бис-фосфата во фруктозо-6-фосфат катализируется специфической фосфатазой:

Образование глюкозы из глюкозо-6-фосфата. В последующей обратимой стадии биосинтеза глюкозы фруктозо-6-фосфат превращается в глюкозо-6-фосфат. Последний может дефосфорилироваться (т.е. реакция идет в обход гексокиназной реакции) под влиянием фермента глюкозо-6-фос-фатазы:
![]()
18. Цикл Кори — совокупность биохимических ферментативных процессов транспорта лактата из мышц в печень, и дальнейшего синтеза глюкозы из лактата, катализируемое ферментами глюконеогенеза.
При интенсивной мышечной работе, а также в условиях отсутствия или недостаточного числа митохондрий (например, в эритроцитах или мышцах) глюкоза вступает на путь анаэробного гликолиза с образованием лактата. Лактат не может далее окисляться, он накапливается (при его накоплении в мышцах раздражаются чувствительные нервные окончания, что вызывает характерное жжение в мышцах). С током крови лактат поступает в печень. Печень является основным местом скопления ферментов глюконеогенеза (синтез глюкозы из неуглеводных соеднений), и лактат идет на синтез глюкозы.
Реакция превращения лактата в пируват катализируется лактатдегидрогеназой, далее пируват подвергается окислительному декарбоксилированию или может подвергаться брожению.
Цикл Кори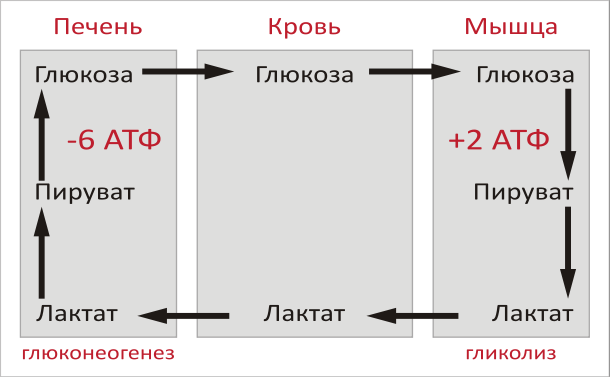
19. В условиях голодания часть белков мышечной ткани распадается до аминокислот, которые далее включаются в процесс катаболизма. Аминокислоты, которые при катаболизме превращаются в пируват или метаболиты цитратного цикла, могут рассматриваться как потенциальные предшественники глюкозы и гликогена и носят название гликогенных. Например, окса-лоацетат, образующийся из аспарагиновой кислоты, является промежуточным продуктом как цитратногр цикла, так и глюконеогенеза.
Из всех аминокислот, поступающих в печень, примерно 30% приходится на долю аланина. Это объясняется тем, что при расщеплении мышечных белков образуются аминокислоты, многие из которых превращаются сразу в пируват или сначала в оксалоацетат, а затем в пируват. Последний превращается в аланин, приобретая аминогруппу от других аминокислот. Аланин из мышц переносится кровью в печень, где снова преобразуется в пируват, который частично окисляется и частично включается в глюкозонеогенез. Следовательно, существует следующая последовательность событий (глюкозо-аланиновый цикл): глюкоза в мышцах → пируват в мышцах → аланин в мышцах → аланин в печени → глюкоза в печени → глюкоза в мышцах. Весь цикл не приводит к увеличению количества глюкозы в мышцах, но он решает проблемы транспорта аминного азота из мышц в печень и предотвращает лактоацидоз.
20. Регуляция гликолиза
Различают местную и общую регуляцию.
-
Местная регуляция осуществляется путём изменения активности ферментов под действием различных метаболитов внутри клетки.
-
Регуляция гликолиза в целом, сразу для всего организма, происходит под действием гормонов, которые, влияя через молекулы вторичных посредников, изменяют внутриклеточный метаболизм.
Важное значение в стимуляции гликолиза принадлежит инсулину. Глюкагон и адреналин являются наиболее значимыми гормональными ингибиторами гликолиза.
Инсулин стимулирует гликолиз через:
-
активацию гексокиназной реакции;
-
стимуляцию фосфофруктокиназы;
-
стимуляцию пируваткиназы.
Также на гликолиз влияют и другие гормоны. Например, соматотропин ингибирует ферменты гликолиза, а тиреоидные гормоны являются стимуляторами.
Регуляция гликолиза осуществляется через несколько ключевых этапов. Реакции, катализируемые гексокиназой (1), фосфофруктокиназой (3) и пируваткиназой (10) отличаются существенным уменьшением свободной энергии и являются практически необратимыми, что позволяет им быть эффективными точками регуляции гликолиза.
Регуляция глюконеогенеза. Уменьшение количества углеводов в клетках или снижение сахара в крови является основным стимулом для увеличения скорости глюконеогенеза. Кроме того, уменьшение количества углеводов может стать причиной изменения направления гликолитических или фосфоглюконатных реакций, что способствует превращению дезаминированных аминокислот в углеводы, наряду с глицеролом. Такой гормон, как кортизол, играет особенно важную роль в регуляции процессов глюконеогенеза.
