
Звягина Учебное пособие
.pdf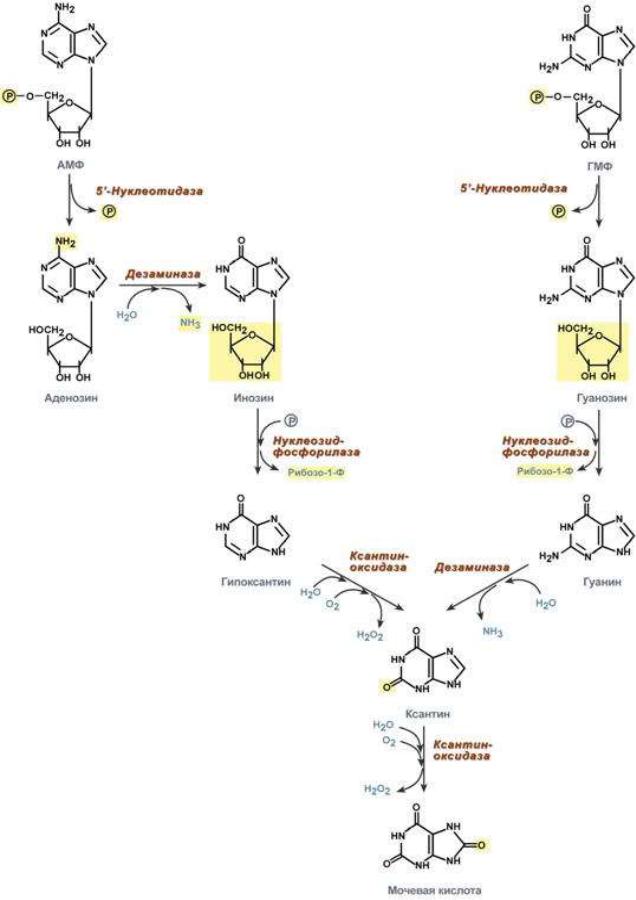
Рисунок 16. Схема распада пуриновых нуклеотидов до мочевой кислоты
131
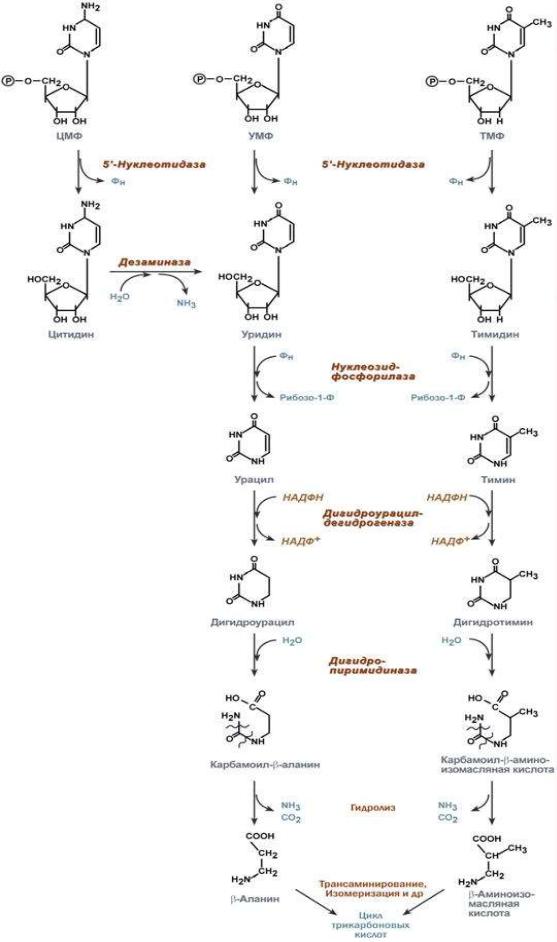
Рисунок 17. Схема распада пиримидиновых нуклеотидов до конечных продуктов
132

Другое заболевание, при котором кристаллы уратов откладываются в почечной лоханке или в мочевом пузыре, известно как мочека-
менная болезнь.
Для лечения подагры и мочекаменной болезни применяются:
ингибиторы фермента ксантиноксидазы. Например, аллопуринол
– вещество пуриновой природы, является конкурентным ингибитором фермента. Действие этого препарата приводит к повышению концентрации гипоксантина. Гипоксантин и его соли лучше растворимы в воде, и легче выводятся из организма.
диетическое питание, исключающее продукты, богатые нуклеиновыми кислотами, пуринами и их аналогами: икра рыб, печень, мясо, кофе и чай.
соли лития, поскольку они лучше растворимы в воде, чем ураты натрия.
Катаболизм пиримидиновых азотистых оснований
Конечными продуктами пиримидинового обмена являются β- аланин и β-аминоизомасляная кислота (аминоизобутират) (рис.17). β- аланин содержится в плазме крови и многих других тканях, он используется в мышцах на образование дипептидов: карнозина и анзерина, часть его может окисляться до СО2 и Н2О.
Синтез пуриновых мононуклеотидов
Для синтеза мононуклеотидов de novo необходимы очень простые вещества: CO2 и рибозо-5-фосфат. Синтез происходит с затратой АТФ. Кроме этого, необходимы заменимые аминокислоты, которые синтезируются в организме, поэтому даже при полном голодании синтез нуклеиновых кислот не страдает.
Особенностью синтеза пуриновых нуклеотидов является то, что циклическая структура пуринового азотистого основания постепенно достраивается на активной форме рибозо-фосфата, как на матрице. При циклизации получается уже готовый пуриновый мононуклеотид.
Пуриновое кольцо строится из СО2, аспарагиновой кислоты, глутамина, глицина и серина. Эти вещества либо полностью включаются
133

в пуриновую структуру, или передают для ее построения отдельные группировки.
5-фосфорибозиламин вовлекается в цепь последовательных реакций, и в результате образуется первый пуриновый нуклеотид – инозинмонофосфорная кислота (ИМФ).
Рисунок 18. Схема синтеза пуриновых нуклеотидов
134

АМФ и ГМФ превращаются далее в нуклеозиддифосфаты с помощью нуклеозидмонофосфаткиназ, функция этих ферментов заключается в том, чтобы поддерживать равновесие фонда нуклеотидов.
ГДФ далее превращается в ГТФ при участии фермента нуклеозиддифосфаткиназы и молекулы АТФ. Превращение АДФ в АТФ происходит, в основном, за счет окислительного фосфорилирования.
В некоторых тканях есть альтернативный способ синтеза – реутилизация (повторное использование) пуриновых азотистых оснований, которые образовались при распаде нуклеотидов.
Ферменты, катализирующие реакции реутилизации, наиболее активны в быстроделящихся клетках (эмбриональные ткани, красный костный мозг, раковые клетки), а также в тканях головного мозга. На схеме видно, что фермент гуанингипоксантинФРПФтрансфераза
обладает более широкой субстратной специфичностью, чем аденинФРПФтрансфераза – помимо гуанина, может переносить и гипоксантин - образуется ИМФ. У человека встречается генетический дефект этого фермента – «болезнь Леша-Нихана». Для таких больных характерны выраженные морфологические изменения в головном и костном мозге, умственная и физическая отсталость, агрессия, аутоагрессия.
135

Синтез пиримидиновых мононуклеотидов.
В отличие от пуринов, при биосинтезе пиримидинов de novo вначале образуется пиримидиновое кольцо, а лишь затем к нему присоединяется рибозо-5-фосфат. Источниками атомов для пиримидинового кольца являются глутамин, аспартат и СО2. Синтез начинается с образования карбамоилфосфата:
Глутамин + СО2 + 2 АТФ Карбамоилфосфат + Глутамат + 2
КарбамоилфосфатсинтетазаI
АДФ + Фн.
Из мононуклеотидов посредством фосфаткиназ синтезируются ди- и трифосфаты
ЦТФ образуется из УТФ в следующей рекции:
136
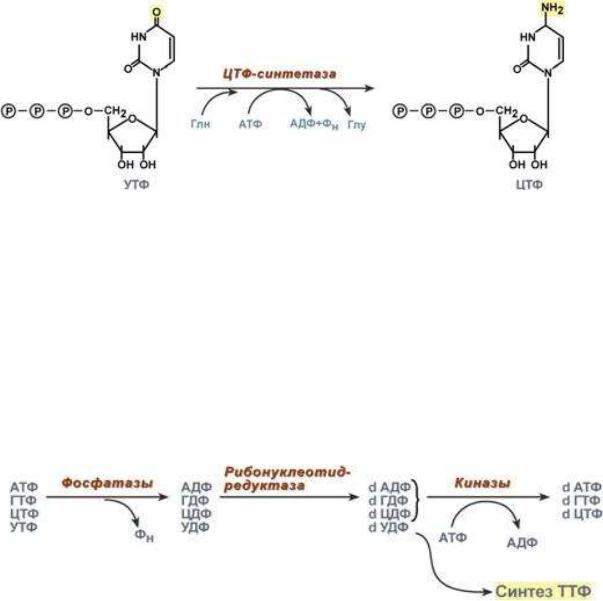
дТМФ синтезируется из дезоксиформы УМФ Ключевой фермент синтеза пиримидиновых нуклеотидов — ас-
партаткарбамоилтрансфераза.
Регуляция: избыток пиримидиновых нуклеотидов ингибирует ключевой фермент, а избыток пуриновых — активирует.
Образование дезоксирибонуклеотидов
Особенностью обмена пуринов и пиримидинов является то, что они могут образовывать не только рибонуклеотиды, но и дезоксирибонуклеотиды, которые необходимы клетке для синтеза ДНК.
В самом начале процесса происходит потеря рибонуклеозидтрифосфатами одной фосфатной группы и образуются АДФ, ГДФ, ЦДФ, УДФ.
Во второй реакции фермент рибонуклеозид-редуктаза восстанавливает АДФ, ГДФ, ЦДФ, УДФ до дезоксирибонуклеозиддифосфатов dАДФ, dГДФ, dЦДФ, dУДФ. Донором водорода для восстановления рибозы является белок тиоредоксин, его SH-группы окисляются кислородом рибозы и образуется вода. Последующее восстановление тиоредоксина в рабочее состояние обеспечивается за счет НАДФН2.
137

После образования dАДФ, dГДФ, dЦДФ фосфорилируются, а dУДФ используется для синтеза тимидилового нуклеотида.
Обмен гемпротеинов. Распад гемоглобина. Образование билирубина и других желчных пигментов. Обезвреживание билирубина. Понятие о свободном («непрямом») и связанном («прямом») билирубине.
Распад гемоглобина происходит в селезенке и печени. Сначала разрывается связь между I-м и II-м кольцами под действием фермента - оксигеназы. После ее действия образуется пигмент зеленого цвета - вердоглобин. В его составе сохраняется и железо и белок. В дальнейшем вердоглобин распадается на составные части: белок, железо и пигмент-биливердин. Железо образует комплекс с белком трансферрином, и этот комплекс поступает в ткани, где оно снова может быть использовано для синтезов или депонироваться в виде комплекса с белком ферритином.
138
Билирубин плохо |
растворим в воде, поэтому он адсорбируется |
на альбумине крови. |
Такой комплекс называется свободным или не- |
прямым билирубином. Он свободный, потому что не связан ни с каким другим веществом ковалентными связями; непрямой, потому что не дает прямой реакции с диазореактивом Эрлиха (для определения этого вида билирубина необходимо предварительно осадить альбумины).
Впечени непрямой билирубин подвергается обезвреживанию путем связывания с глюкуроновой кислотой. В реакции расходуется УТФ. При этом к молекуле билирубина присоединяются 2 молекулы глюкуроновой кислоты (образование билирубиндиглюкуронида) под действием фермента - УДФ - глукуронозилтрансферазы. Это веще-
ство малотоксично и хорошо растворяется в воде, называется прямым связанным билирубином, т.к. определяется в прямой реакции с диазореактивом и, ковалентно связан с глюкуроновой кислотой. В таком виде билирубин поступает в желчь и вместе с ней выводится из организма.
При определении содержания билирубина используют диазореактив, который дает розовую окраску с билирубином и по ее интенсивности судят о концентрации билирубина в крови.
Вкрови человека примерно 75% непрямого билирубина от его общего количества. Общее содержание билирубина в норме (прямой+непрямой) от 8 до 20 мкмоль/л.
Билирубин - это конечный продукт распада гемоглобина у человека. Однако, поступив с желчью в кишечник, он превращается под действием ферментов микрофлоры кишечника. Сначала от него отщепляется глюкуроновая кислота, затем происходит частичное восстановление и образуется вещество, называемое мезобилиноген, а затем стеркобилиноген. Стеркобилиноген в основном выводится с калом и на воздухе (в кале) превращается в стеркобилин, а мезобилиноген частично всасывается из кишечника по системе v.portae, т.е. попадает в печень и там разрушается. Поэтому его нет у здоровых людей в крови. Небольшая часть стеркобилиногена тоже всасывается из кишечника через систему геморроидальных вен, т.е. попадает сразу в большой круг кровообращения, минуя печень, поэтому часть его выводится с мочой.
Значит, стеркобилиноген является компонентом мочи в норме.
ВНОРМЕ:
Кровь:
139
Билирубин (в основном непрямой) - в норме (8-20 мкмоль/л) Гемоглобин - в норме (мужчины - 130-145 г/л; женщины - 110-130 г/л Моча: светло-желтого цвета, стеркобилиноген - в норме, мезобилиногена нет.
Кал: нормальной окраски, стеркобилиноген - в норме
Нарушения обмена билирубина. Диагностическое значение определения билирубина в крови и моче.
При некоторых заболеваниях билирубин начинает накапливаться в слизистых оболочках, коже, склерах. Человек «желтеет». Этот симптом называется желтуха и наблюдается при желчнокаменной болезни, гемолизе, инфекционном или токсическом гепатитах. Определение билирубина в моче, в крови и в кале позволяет выявить причины желтухи.
Гемолитическая желтуха. Наблюдается при усилении распада эритроцитов. Билирубина образуется больше, чем в норме и скорость экскреции тоже увеличивается. Непрямой билирубин повышается в крови. В моче билирубина нет, а содержание стеркобилина в кале и в моче повышено.
Печеночная желтуха (паренхиматозная). Наблюдается при повреждении гепатоцитов (например, при вирусном гепатите). Билирубин не обезвреживается. Желчные пигменты поступают не только в кишечник, но и в кровь. Т.е. в крови повышается содержание непрямого билирубина.
Обтурационная желтуха (механическая). Наблюдается при закупорке желчных протоков (например, при желчнокаменной болезни). Желчь продолжает вырабатываться, но поступает не только в желчные протоки, а также в кровь. В крови повышается уровень билирубина, в основном - прямого билирубина. Наблюдается билирубинурия. Содержание стеркобилина в моче и в кале снижено (кал становится светлым, а моча темнеет за счет прямого билирубина).
I.Вопросы для самоподготовки:
1.Фонд свободных аминокислот.
2.Классификация протеолитических ферментов.
3.Функции и регуляция активности тканевых протеиназ.
4.Дезаминирование аминокислот, его виды.
5.Трансдезаминирование и прямое окислительное дезаминирование аминокислот, биологическая роль этих процессов.
140
