
Физика атомов и молекул
1. Укажите, какой ответ может быть окончанием фразы:
«Физикой атомов и молекул называют раздел курса посвященный
изучению кинематических и динамических характеристик атомов и молекул определяющих сколь угодно точно их импульс и энергию».
изучению корпускулярных и волновых свойств атомов и молекул с помощью линейного дифференциального уравнения Шредингера для определения волновой
 - функции, позволяющей оценивать
вероятности координаты, скорости,
импульса, энергии и изменения их
состояний во времени с неизбежной не
точностью».
- функции, позволяющей оценивать
вероятности координаты, скорости,
импульса, энергии и изменения их
состояний во времени с неизбежной не
точностью».изучению природы химической связи молекул».
изучению моделей атомов и молекул, объясняющих их спектры излучения и поглощения».
изучению сил взаимодействия электронов с положительным ядром».
2. Укажите научные и экспериментальные результаты, которые позволили Бору создать квантовую теорию строения атома:
1 Модель атома по Томсону. 2 Ядерная модель атома по Резерфорду.
3. Закономерности линейчатого спектра излучения атома водорода, выраженного формулой Бальмера – Ридберга.
4 Квантовый характер спектров излучения и поглощения света.
5 Правильного ответа здесь нет.
3. Укажите формулу Бальмера для определения длины волны излучения атомов водорода
![]()
4. Укажите математические зависимости первого и второго постулатов Бора
![]()
5. Укажите опыты, в которых сделан вывод о ядерной модели атома:
1 Франка и Герца. 2 Дэвиссона и Джермера. 3 Томсона и Тартаковского.
4 Резерфорда по
рассеянию
![]() — частиц. 5 Штерна и Герлаха.
— частиц. 5 Штерна и Герлаха.
6. Какие выводы следуют из теории Бора?
Энергия электрона в атоме принимает непрерывный ряд значений.
Энергия электрона в атоме принимает дискретные значения.
Атом непрерывно излучает энергию.
Атом излучает квант энергии при переходе электрона из одного стационарного состояния в другое.
7. Укажите формулу Бальмера выведенную на основе теории Бора водородоподобных атомов
![]()
8. Найти
численное значение полной энергии атома
водорода во втором стационарном
состоянии. Постоянную Ридберга принять
равной R
= 1,1 107
м -1,
![]() = 6,63 10-34
Дж с и скорость света с
= 3 108
м/с.
Полученный
результат выразить в электрон-вольтах
(l
эВ = 1,6 10 -19
Дж).
= 6,63 10-34
Дж с и скорость света с
= 3 108
м/с.
Полученный
результат выразить в электрон-вольтах
(l
эВ = 1,6 10 -19
Дж).
9. Определить радиус второй боровской орбиты атома водорода в этом стационарном состоянии. Постоянную Ридберга принять равной R = 1,1 107 м -1, массу электрона m = 9,1 10 31кг, h = 6,63 10 -34 Дж с.
|
10. Какой из переходов на схеме энергетических уровней атома водорода (рис. 3) соответствует излучению линий серии Лаймана.
|
рис. 3 |
11. Какой из переходов на схеме энергетических уровней атома водорода (рис 6 10) соответствует излучению линий серии Бальмера.
12. Какой из показанных на рисунке 3 переходов между энергетическими уровнями атома водорода соответствует поглощению линии видимой серии?
13. Какой из показанных на рисунке 3 переходов между энергетическими уровнями атома водорода соответствует поглощению наибольшей длины волны ультрафиолетовой области?
14. В каком из перечисленных явлений проявляется волновая природа электрона?
1. Дифракция электронов.
2. Термоэлектронная эмиссия. 3. Фотоэффект.
4. Эффект Комптона. 5 Вторичная эмиссия электронов.
15. Какая из приведенных формул соответствует формуле де Бройля?
![]()
16. Вычислить длину волны де Бройля для электрона, движущегося со скоростью ν = 2,2 Мм/с. (h = 6,63 10 -34 Дж*с и масса электрона m = 9,1 10 -31 кг)
17. Что подтверждает результат опытов Дэвиссона – Джермера?
1 Волновые свойства света. 2 Волновую природу электрона. 3 Корпускулярные свойства электрона
4 Квантовый характер поглощения света. 5 Квантовый характер излучения света
18. Вычислить длину волны де Бройля для электрона, импульс которого равен р = 1,1 10 26 кг *м/с (h = 6,63 10 -34 Дж*с и масса электрона m = 9,1 10 -31 кг)
19. Какие из приведенных формул выражают соотношение неопределенностей Гейзенберга
![]()
20. Определить неопределенность в составляющей скорости для электрона, движущегося в атоме при условии, что положение электрона может быть определено с точностью до размеров атома, т.е. Δх = 10 - 10 м (h = 6,63 10 -34 Дж*с и масса электрона m = 9,1 10 -31 кг).
21. Какие выводы следуют из соотношения неопределенностей?
Частица не может иметь одновременно точные значения координаты х и импульса р.
Микрочастица может иметь одновременно точные значения координаты х и импульса р.
Чем точнее для микрочастицы определена одна из величин - координата х или импульса р, тем больше становится не точность в определении другой.
Микрочастица веет да имеет одновременно вполне точные значения координаты и импульса.
Правильного ответа здесь нет
22. Что характерно для частицы, не проявляющей волновых свойств?
Частица не обладает одновременно определенными значениями координаты и импульса.
Частица обладает одновременно определенными значениями координаты и импульса.
Принцип причинности позволяет определить координату и импульс в момент времени.
Движущаяся частица описывает определенную траекторию.
Возможны состояния частицы, при которых одна из величин - импульс - имеет определенные значения, другая величина - координата - имеет неопределенные значения.
23.
Скорость частицы, которая двигается
вдотъ оси х,
определяется с точностью до
![]() = 1 см/с. Оценить неопределенность
координаты частицыΔх,
если такой частицей являются а) электрон,
б) броуновская частица массой m
=10 -
16
кг , в) дробинка массой m
=10 -
4
кг.
= 1 см/с. Оценить неопределенность
координаты частицыΔх,
если такой частицей являются а) электрон,
б) броуновская частица массой m
=10 -
16
кг , в) дробинка массой m
=10 -
4
кг.
24. Какие понятия применимы для описания состояний микрочастицы?
1) Траектория. 2) ψ — функция. 3) Координата. 4) Функция (ψ) 2 5) Энергия микрочастицы.
25. Какая из перечисленных величин определяет вероятность нахождения микрообъекта в данной точке пространства?
1) Координата. 2 ) |ψ| 2 — функции. 3) Импульс. 4 Координаты и импульс. 5) Правильного ответа здесь нет.
26. Что выражает квадрат модуля амплитуды волновой функции |ψ| 2 ?
1 Энергию частицы. 2 Вероятность попадания фотона в данную точку пространства.
3 Амплитуду волн де Бройля для данной частицы.
4 Вероятность нахождения микрообъекта в данной области пространства.
5 Вероятность нахождения микрообъекта где- либо в пространстве.
27. Укажите условия нормировки волновой функции
![]()
28. Какие из приведенных уравнений соответствует уравнению Шредингера для атома водорода в стационарном состоянии?

29. По какой формуле вычисляется энергия микрочастицы, находящейся в одномерном потенциальном ящике
![]()
30. Электрон помещен в одномерный потенциальный ящик с шириной l = 4 10 - 1Ом . Чему равна энергия электрона на втором энергетическом уровне? Найти длину волны фотона, который излучается при переходе из четвертого энергетического уровня на второй.
31. По, каким формулам вычисляется полная энергия электрона в атоме водорода на n- м энергетическом уровне?
![]() 32.
Частица, движущаяся в одномерной
бесконечно глубокой потенциальной яме,
находится в основном состоянии (т.е. с
наименьшей энергией). Вычислить
вероятность Ρ
того, что координата частицы имеет
значение, заключенное в пределах от
0,25
l
до 0,75
l,
где
l
-ширина ямы.
32.
Частица, движущаяся в одномерной
бесконечно глубокой потенциальной яме,
находится в основном состоянии (т.е. с
наименьшей энергией). Вычислить
вероятность Ρ
того, что координата частицы имеет
значение, заключенное в пределах от
0,25
l
до 0,75
l,
где
l
-ширина ямы.
|
33. Укажите поведение прохождения частицы сквозь потенциальный барьер на основе выводов квантовой механики
4 Частица не проходит сквозь потенциальный барьер, если ее полная энергия Ε <UO не превышает «высоту» потенциального барьера. 5 Правильного ответа здесь нет.
|
|
34. Укажите формулу прозрачности прямоугольного потенциального барьера (рис 6 33)
![]() 35.
Укажите формулу прозрачности
потенциального барьера произвольной
формы
35.
Укажите формулу прозрачности
потенциального барьера произвольной
формы
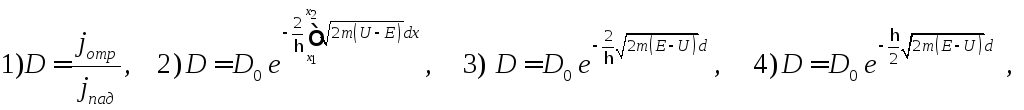
5) правильного ответа здесь нет.
36 . Какая из квантующихся физических величин в атоме водорода определяется главным квантовым числом п?
1) Собственный момент импульса электрона LS.
2) Орбитальный момент импульса электрона Ll.
3) Проекция вектора орбитального момента импульса электрона Ll,z на направление магнитного поля.
4) Проекция вектора орбитального момента импульса (спина) электрона на направление магнитного поля LS,Z.
5) Энергия электрона.
37. Какая из физических величин в атоме водорода определяется квантовым числом l?
1) Собственный момент импульса электрона LS.
2) Орбитальный момент импульса электрона Ll
3) Проекция вектора орбитального момента импульса электрона Ll,z на направление магнитного поля.
4) Проекция вектора орбитального момента импульса (спина) электрона LS,Z на направление магнитного поля .
5) Энергия электрона.
38. Какая из физических величин в атоме водорода определяется квантовым числомml
1) Собственный момент импульса электрона LS.
2) Орбитальный момент импульса электрона Ll
3) Проекция вектора орбитального момента импульса электрона Ll,z на направление магнитного поля.
4) Проекция вектора орбитального момента импульса (спина) электрона LS,Z на направление магнитного поля .
5) Энергия электрона.
39. Какие значения орбитального квантового числа возможны при n = 2?
![]()
40. Укажите формулу, по которой определяется величина орбитального момента импульса электрона
![]()
41. По какой формуле определяется проекция вектора орбитального момента импульса электрона на направление магнитного моля?
![]()
42. Какому состоянию электронов соответствует состояние, определяемое l= 2
![]()
43. На каких из приведенных рисунков
4 даны возможные ориентации проекции
вектора орбитального момента импульса
электрона
![]() в
магнитном поле вf-состоянии?
в
магнитном поле вf-состоянии?
44. На каких из приведенных рисунков
4 даны возможные ориентации проекции
вектора орбитального момента импульса
электрона
![]() в
магнитном поле вg-состоянии?
в
магнитном поле вg-состоянии?
45. На каких из приведенных рисунков
4 даны возможные ориентации проекции
вектора орбитального момента импульса
электрона
![]() в
магнитном поле вs-состоянии?
в
магнитном поле вs-состоянии?
46. На каких из приведенных рисунков
4 даны возможные ориентации проекции
вектора орбитального момента импульса
электрона
![]() в
магнитном поле вp-состоянии?
в
магнитном поле вp-состоянии?

рис. 4
47. Какие значения магнитного квантового числа mвозможны при значении орбитального квантового числаl = 1?
![]()
48. Какая из физических величин в атоме водорода определяется квантовым числом ms
1) Собственный момент импульса электрона LS.
2) Орбитальный момент импульса электрона Ll
3) Проекция вектора орбитального момента импульса электрона Ll,z на направление магнитного поля.
4) Проекция вектора орбитального момента импульса (спина) электрона LS,Z на направление магнитного поля .
5) Энергия электрона.
49. По какой формуле определяется собственный момента импульса (спин) электрона?
![]() 50.
Какие из перечисленных величин могут
быть выражены через магнетон Бора?
50.
Какие из перечисленных величин могут
быть выражены через магнетон Бора?
Собственный момент импульса электрона L s.
Проекция собственного магнитного момента (спина) электрона на направление магнитного поля pm s, z .
Проекция орбитального момента импульса электрона на направление внешнего магнитного поля pm l, z.
4) Орбитальный момент импульса электрона L l.
5) Дипольный электрический момент электрона.
51. Из решения какого уравнения следует, что электрон обладает собственным моментом импульса (спином)?
Волнового уравнения для электромагнитных волн.
Релятивистского волнового уравнения Дирака.
Уравнения Шредингера для частицы, находящейся в одномерной потенциальной яме.
Волнового уравнения для механических волн.
Уравнения Шредингера для атома водорода.
52. По какой из приведенных формул можно рассчитать значение магнетона Бора7
![]()
53. Каково максимальное число электронов, находящихся в состояниях, определяемых одним и тем же значением главного квантового числа n ?
![]()
54. Укажите максимальное число
электронов, находящихся в состояниях,
определяемых одинаковым набором двух
квантовых чисел
![]()
![]()
55. Укажите максимальное число
электронов, находящихся в состояниях,
определяемых одинаковым набором четырех
квантовых чисел
![]()
![]()
56. Какая из пар электронов с приведенными
значениями квантовых чисел
![]() находятся в атоме в состоянии 2s
находятся в атоме в состоянии 2s
![]()
57. Какому элементу таблицы Менделеева
соответствует структурная формула
![]()
1 Неону. 2 Натрию. 3 Магнию. 4 Алюминию. 5 Кремнию.
58. Какое максимальное количество электронов может находиться в L– оболочке
1) 4 2) 8 3) 18 4) 32 5) 50
59. От чего зависит длина волны характеристического рентгеновского излучения?
1 Температуры катода. 2 Материала катода. 3 Силы тока в рентгеновской трубке.
4 Разности потенциалов между катодом и анодом. 5 Материала антикатода.
81. Укажите основную задачу физики атомов и молекул
Расчет собственных значений энергии Е„ и собственных волновых функций Ψ электронов, характеризующих их состояние в атомах и молекулах.
Расчет состояний атомов и молекул производится на основе классической механики.
Расчет состояний атомов и молекул производится на основе квантово-волновых свойств микрочастиц.
Находить дебройлевскую длину волны движущихся частиц и вероятность прохождения их через потенциальный барьер.
Определять границы применимости законов классической физики по отношению к атомам и молекулам с помощью фундаментального закона природы соотношения неопределенностей Гейзенберга.


