
Obsh_chemical_1
.pdf
21 рите.ля, а также от температуры, но не зависит от концентрации рас
твора. Чем выше К , тем легче электролит распадается на ионы. Константа и степень диссоциации связаны между собой уравнени
ем, называемым законом разбавления Освальда. Для электролита, распадающегося на два иона, это уравнение имеет вид
где С - молярная концентрация электролита, моль/л.
При |
0,01, что имеет место |
для слабых |
электролитов, |
Из закона |
разбавления видно: степень |
диссоциации |
возрастает при |
разбавлении раствора. |
|
|
|
Слабые электролиты - это электролиты, диссоциирующие в раст ворах неполностью. В их растворах устанавливается равновесие меж ду молекулами и продуктами диссоциации - ионами. Условно к слабым электролитам относятся электролиты, у которых при обычных концен
трациях |
Например, уксусная кислота |
+Н+ , |
|
К слабым электролитам применим закон действия масс и закон разбав ления Освальда.
Сильные электролиты - это электролиты, диссоциирующие в раст ворах полностью. Например, поваренная соль  В ра створах сильных электролитов (согласно спектральным данным) нет нейтральных молекул. Поэтому закон действия масс для них неприме ним. Благодаря полной диссоциации в растворах сильных электролитов наблюдается высокая концентрация ионов, из-за чего большое значе ние приобретают силы межионного взаимодействия (в растворах слабых электролитов это взаимодействие не учитывается). В результате вза имного притяжения ионов их движение заторможено. Это приводит к изменению свойств растворов в том же направлении, что и при умень шении степени диссоциации, т . е . при частичном соединении ионов в молекулы. В различных процессах (электропроводность, химические реакции) ионы проявляют себя таким образом, будто их концентрации меньше действительной. Поэтому для сильных электролитов введено понятие кажущейся концентрации, которая названа активностью α ,
В ра створах сильных электролитов (согласно спектральным данным) нет нейтральных молекул. Поэтому закон действия масс для них неприме ним. Благодаря полной диссоциации в растворах сильных электролитов наблюдается высокая концентрация ионов, из-за чего большое значе ние приобретают силы межионного взаимодействия (в растворах слабых электролитов это взаимодействие не учитывается). В результате вза имного притяжения ионов их движение заторможено. Это приводит к изменению свойств растворов в том же направлении, что и при умень шении степени диссоциации, т . е . при частичном соединении ионов в молекулы. В различных процессах (электропроводность, химические реакции) ионы проявляют себя таким образом, будто их концентрации меньше действительной. Поэтому для сильных электролитов введено понятие кажущейся концентрации, которая названа активностью α ,
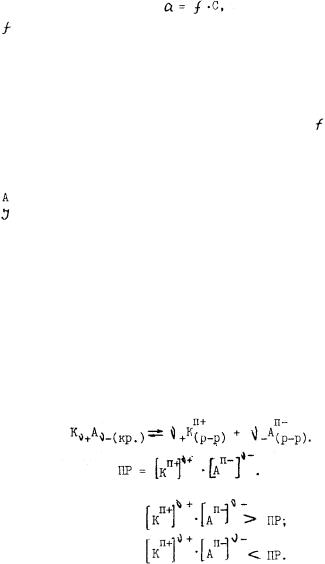
22 формально заменяющей в уравнении закона действия масс концентра цию.
где - коэффициент активности - величина, которая суммарно от ражает все возможные взаимодействия ионов в растворе. Иногда 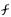 рассматривают как"кажущуюся степень диссоциации". Из-за сложности и многообразия взаимодействий в растворах сильных электролитов пока что не создана теория сильных электролитов, объясняющая ко
рассматривают как"кажущуюся степень диссоциации". Из-за сложности и многообразия взаимодействий в растворах сильных электролитов пока что не создана теория сильных электролитов, объясняющая ко
эффициент активности |
при любых концентрациях. Сейчас имеется тео |
||
рия Дебая |
и Хюккеля, |
которая позволяет рассчитать |
ионов при |
небольших |
концентрациях электролитов (до С,1 моль/л). |
|
|
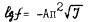 »
»
где п - заряд иона;
-теоретический коэффициент, при 25 °С равный 0,51;
-ионная сила раствора.
Ионная сила - это полусумма произведений концентраций ионов, из которых состоит электролит, умноженная на квадрат их зарядов. Правило ионной силы: при постоянной ионной силе раствора коэффи циенты активности любых электролитов постоянны.
Произведение растворимости ПР - произведение концентраций ионов,на которые распадается малорастворимый электролит в насыщен ном растворе, в степени, равной стехиометрическим коэффициентам. При постоянной температуре ПР есть величина постоянная, не завися щая от концентрации. Произведение растворимости вытекает из приме нения закона действия масс к равновесной системе, состоящей из кристаллов малорастворимого вещества и его ионов в насыщенном рас творе.
Из понятия ПР вытекают условия:
образования осадка
растворения осадка
Ионообменные реакции между ионами протекают в тех случаях, когда в результате их взаимодействия образуются вещества либо ме нее растворимые (осадки, газы), либо в меньшей степени диссоцииру ющие на ионы, чем исходные. Различают четыре типа обменных реакций:
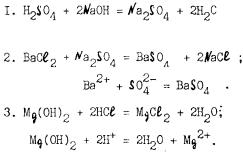
23
I) реакции, идущие с образованием осадка; 2) реакция, идущие с об разованием летучих (газообразных) веществ; 3) реакции, идущие с образованием слабых электролитов; 4) реакции, идущие с образовани ем комплексных соединений. При составлении ионных уравнений обмен ных реакций необходимо придерживаться следующих правил: а) силь ные электролиты записывают в виде ионов, так как именно в таком состоянии они находятся в растворе; б) слабые электролиты, газы, плохо растворимые соединения записывают в виде молекул независимо от того, являются ли они исходными веществами или продуктами реак ций. Ионное уравнение выражает сущность процесса.
Примеры:
(молекулярное уравнение);
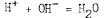 (ионное уравнение).
(ионное уравнение).
Оборудование и реактивы: прибор для определения электропрово дности растворов, стакан емкостью 100 мл - 6 шт., штатив с пробир ками, шпатель; растворы уксусной, соляной, серной кислот, гидроксида аммония, ацетата натрия, гидроксида натрия, хлорида натрия, хлорида калия, иодида калия; дистиллированная вода; сухие реакти вы - нитрат свинца, сульфат железа ( I I ) , сульфат меди; индикатор - фенолфталеин.
ХОД РАБОТЫ
Опыт I. Электропроводность растворов.
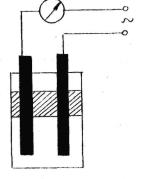
Для изучения электропроводности растворов применяют прибор, изображенный на рисунке. В стакан объемом 50 мл наливают раствор на 1/2 его объема, чтобы площади электродов, опущенных в жидкость, были каждый раз одинаковы. Затем в стакан опускают электроды и прибор включают в сеть переменного тока. Об электропроводности ра створов судят по показанию гальванометра, включенного в электриче скую цепь.
Испытайте электропроводность следующих растворов: дистиллиро ванной воды, уксусной кислоты, соляной кислоты, гидроксида аммо-
24
ния, гидроксида натрия, хлорида на трия. Расположите электролиты в по рядке их силы. Напишите уравнения диссоциации этих электролитов и примените к ним закон действия масс.
К сильным или слабым электролитам относятся гидроксид аммония и ук сусная кислота ? Слейте их в один стакан и проверьте электропровод ность. Объясните полученный резуль тат. Зарисуйте прибор.
Опыт 2. Влияние разбавления раствора на степень электролити ческой диссоциации.
Испытайте электропроводность концентрированной (30 %-ной) и разбавленной (в 4, в 3 и в 16 раз) уксусной кислоты. Как меняется электропроводность с разбавлением раствора ? Сделайте вывод о на правлении смещения равновесия диссоциации с разбавлением раствора.
Опыт 3. Влияние одноименного иона на степень диссоциации сла бого электролита.
В две пробирки влейте по 5-7 капель 0,1 н раствора уксусной кислоты и по одной капле индикатора метилового оранжевого. В одну из пробирок добавьте несколько кристалликов ацетата натрия и пере мешайте. Сравните цвет растворов в обеих пробирках. Пользуясь вы ражением константы диссоциации, объясните причину смещения равно весия..
Аналогичный опыт проделайте с 0,1 н раствором аммиака, приме няя в качестве индикатора фенолфталеин и добавляя хлорид аммония.
Опыт 4. Сравнение химической активности электролитов.
Поместите |
в две пробирки небольшие кусочки мрамора и добавьте |
|
в одну из них |
соляную, |
а в другую - уксусную кислоту одинаковой |
концентрации. |
Объясните |
различие в скорости реакций. |
Опыт 5. Реакции, идущие с образованием слабого электролита.
В пробирку с 5-7 каплями раствора ацетата натрия добавьте нес колько капель серной кислоты (1:1), растворы перемешайте и слегка подогрейте. Определите по запаху образование слабой уксусной кис лоты. Во вторую пробирку внесите 5-7 капель раствора хлорида аммо ния и несколько капель 4 н раствора щелочи, подогрейте раствор.

25 Определите по запаху выделение аммиака.
Опыт 6. Реакции нейтрализации.
В две пробирки внесите по 5-? капель 2 н раствора щелочи и по одной капле фенолфталеина. В одну пробирку добавляйте по кап лям 2 н раствор серной кислоты, в другую - 2 н раствор уксусной кислоты до обесцвечивания раствора. В каком случае обесцвечивание наступило быстрее ? Почему равновесие второй реакции смещается в сторону образования воды при наличии в левой части равенства малоциссоциированных молекул уксусной кислоты ?
Опыт 7. Реакции, идущие с образованием осадка. Условие выпа дения осадка.
В две пробирки налейте по 3-4 капли 0,005 м раствора нитрата свинца. В одну из них прибавьте такой же объем 0,05 м раствора хлорида калия, а в другую - иодида калия. В какой из пробирок вы пал осадок ? Объясните полученный результат, используя значения произведений растворимости (см. таблицу).
Опыт 8. Условия растворения осадков.
Получите осадки сульфидов железа (II) и меди (II). Для этого к 2-3 каплям раствора сульфата железа (II) и сульфата меди добавь те по 3-4 капли раствора сульфида аммония. К полученным осадкам прилейте немного 2 н раствора соляной кислоты. Какой из осадков растворяется ? Объясните различие в растворимости осадков, исполь
зуя значения произведений растворимости (ПР) при 25 |
С. |
|||
|
|
Таблица |
||
|
|
|
|
|
Соединение |
ПР |
Соединение |
|
ПР |
|
|
|
|
|
Контрольные вопросы и задачи
1.Что такое сильные и слабые электролиты ? Перечислите силь ные и слабые кислоты и основания.
2.В чем заключается основная причина диссоциации ? Как зави сит способность электролитов к диссоциации от вида химической свя зи ?

26
3.От каких факторов зависит степень диссоциации ? Как ее увеличить или уменьшить ?
4.Что такое константа диссоциации ? Чем она отличается от степени диссоциации и от чего зависит ?
5.Почему закон действия масс неприменим к сильным электро литам ? Что такое активность ? '
6.При каких условиях обменные реакции протекают до конца ? Приведите примеры.
7.Что называется произведением растворимости ? Каковы усло вия образования и растворения осадков ?
8.Написать все возможные уравнения электролитической диссо циации угольной и сернистой кислот, гидроксида железа (III) и вы разить в общем виде их константы диссоциации.
9.Составьте ионные и молекулярные уравнения следующих реак
ций:
10.Почему концентрация водородных ионов уменьшается от доба вления нитрита калия в раствор азотистой кислоты ?
11.Как влияет на растворимость карбоната бария добавление в раствор карбоната натрия ?
12.Зная, что произведение растворимости CaSO4 равно 6,1•10-5 , вычислить, выпадает ли осадок этой соли при сливании 100 мл
0,004 м 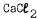 с IG0 мл 0,001 м
с IG0 мл 0,001 м
13.В 2 л раствора содержится 0,1 моль слабого бинарного эле ктролита (АВ), в том числе 0,004 моля находится в виде ионов. Най дите константу диссоциации, степень диссоциации и изотонический коэффициент.
Ответ: 8,3•10-5; 4 %; 1,04.
ЛАБОРАТОРНАЯ РАБОТА № 5. ХАРАКТЕРИСТИКА СРЕДЫ РАСТВОРОВ. ГИДРОЛИЗ СОЛЕЙ
Цель работы: научиться определять среду раствора при помощи универсального индикатора, изучить характер гидролиза различных солей.

27 ТЕОРЕТИЧЕСКОЕ ОБОСНОВАНИЕ
Гидролизом солей называется реакция обменного разложения меж ду водой и солью, сопровождающаяся взаимодействием ионов соли с молекулами воды, ведущая к образованию слабых электролитов, мало растворимых веществ, газов. При гидролизе нарушается равновесие
электролитической диссоциации воды, |
изменяется рН раствора. |
Так как вода слабый электролит, |
то для описания процесса ее |
электролитической диссоциации |
применим закон дейст |
вия масс: |
|
Концентрация недиссоциированных молекул примерно равна общему количеству молей в одном литре.
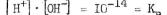 - это постоянная величина и называется ионным произведением воды. Концентрации ионов водорода Н и ОН" в чистой, воде
- это постоянная величина и называется ионным произведением воды. Концентрации ионов водорода Н и ОН" в чистой, воде
Для облегчения расчетов концентрацию ионов водорода выражают в логарифмической шкале, используя водородный показатель рН.
Следовательно, |
для нейтрального раствора рН = 7, .для кислого |
, |
для щелочного |
Зависимость |
между концентрацией ионов водорода, величиной рН |
и реакцией среды |
раствора можно выразить схемой |
Для приближенного определения рН раствора пользуются универ сальными индикаторами; представляющими собой смесь нескольких ин дикаторов и дающими различную окраску раствора в зависимости от рН среды (табл.I).
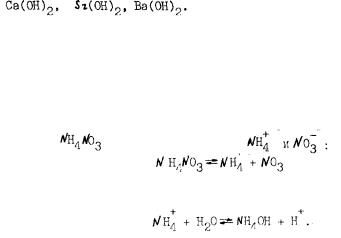
28
|
|
|
|
Таблица I |
|
|
|
|
|
|
|||
Индикатор |
Окраска индикатора в зависимости от |
Интервалы пере |
||||
|
|
рН , среды |
|
хода окраски |
||
|
|
|
|
|
индикатора, рН |
|
|
|
Среда |
|
|||
|
|
|
|
|
||
|
|
|
|
|
|
|
|
нейтральная |
кислая |
|
щелочная |
|
|
|
|
|
|
|
|
|
Лакмус |
Фиолетовая |
Розовая |
Синяя |
5,0 |
- 8,0 |
|
Фенол |
|
|
|
|
|
|
фталеин |
Бесцветная |
Бесцветная |
Малиновая |
3,0 |
- 9,3 |
|
Метилоранж |
Оранжевая |
Розовая |
Желтая |
3,1 |
- 3,4 |
|
Часто пользуются универсальной индикаторной бумагой. По прила гаемой к ней цветной шкале устанавливают, при каких значениях рН индикаторная бумага окрашивается в тот или иной цвет. При помощи такой бумаги можно определить рН раствора с точностью до единицы в интервале рН от I до 13. Для количественного определения рН среды используют приборы, называемые рН-метрами.
Гидролизу подвергаются только те соли, в состав которых вхо дят ионы слабой кислоты или. слабого основания. Соли, образованные сильным основанием и сильной кислотой, гидролизу не подвергаются, так как ионы таких солей не могут образовывать с ионами воды слабодиссоциирующие или малорастворимые вещества, а раствор имеет нейтральную реакцию рН = 7.
К сильным кислотам относятся: 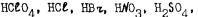
НМn04 .
К сильным основаниям относятся: 
При изучении гидролиза необходимо учитывать, что процесс яв ляется обратимым, зависит от рН среды, концентрации соли и темпе ратуры. Уменьшение концентрации соли и повышение температуры уве личивают полноту гидролиза.
Гидролизующиеся соли делятся на три группы.
I. Гидролиз солей, образованных слабым основанием и сильной
кислотой, идет по слабому звену |
- катиону. Например, соль - нитрат |
|
аммония |
диссоциирует на |
ион |
+
NH4 -IIOH образует с молекулами воды слабодиссоциирующее соединение NH•ОH. Ионное уравнение гидролиза нитрата аммония имеет вид

29
Вмолекулярной форме
Всистеме два слабых электролита: Н20 иNН4ОН. Поэтому наряду с реакцией гидролиза (прямая реакция) идет и реакция нейтрализации (обратная реакция), т.е. реакция гидролиза обратима. Константа диссоциации воды равна 1,86•10-16 _и меньше, чем константа диссоци ации гидроксида аммония (1,79•10- 5 ) поэтому реакция гидролиза идет в сторону образования более слабого электролита, т.е. в сто рону исходных веществ.
Если катион многозарядный, гидролиз идет ступенчато, в резуль
тате гидролиза по первой ступени образуется основная соль. Рассмо трим гидролиз хлорида никеля t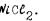
В водном растворе только ионы никеля |
могут |
взаимодействовать |
с ионами ОН-, так как образуется прочный ион |
- слабый элек |
|
тролит. Краткое ионное уравнение гидролиза, выражающее суть про цесса ,
В растворе накапливаются ионы Н+, которые создают кислую среду и препятствуют прохождению гидролиза по второй ступени. Молекулярное уравнение процесса
По второй ступени гидролиз возможен только при повышении температу ры или при большом разбавлении.
Молекулярная форма
I
2. Гидролиз соли, образованной сильным основанием и слабой кислотой, идет по слабому звену - аниону. Рассмотрим на примере карбоната калия, диссоциирующего по уравнению
Ионное уравнение гидролиза

30
Гидролиз в молекулярной форме
Гидролиз вдет практически только по первой ступени с образованием кислой соли, так как появившиеся гидроксид-ионы ОН- препятствуют прохождению гидролиза по второй ступени.
3. Гидролиз солей, образованных слабым основанием и слабой кислотой, идет и по катиону, и по аниону. Образующиеся ионы Н+ и ОН- одновременно связываются, сдвигая равновесие диссоциации воды. При этом в зависимости от заряда ионов могут образоваться:
слабая кислота и слабое основание
слабая кислота и основная соль (если катион многозарядный)
слабое основание и кислая соль (если анион многозарядный)
При гидролизе таких солей рН раствора может быть равен 7 |
(обычно |
6-8), если образующиеся кислота и основание одинаковы по |
силе. |
Гидролиз солей, образованных очень слабым основанием и очень слабой кислотой, будет необратимым (полным). Например, гидролиз сульфидов и карбонатов трехзарядных катионов 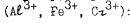
Поэтому сульфиды и карбонаты этих элементов в водных растворах не существуют, могут быть получены только сухим путем.
Количественно гидролиз характеризуют с помощью константы и
степени гидролиза. |
|
Степень гидролиза, |
- это отношение числа молекул, подвер |
гающихся гидролизу, к общему числу молекул в растворе. Степень ги дролиза зависит от концентрации (чем меньше концентрация, тем бо льше степень гидролиза), от температуры (с увеличением температу ры степень гидролиза увеличивается). Для того, чтобы растворы не подвергались гидролизу, их необходимо хранить при более низкой тем пературе и в более высокой концентрации. От гидролиза можно изба-
