
- •9. Углеродистые стали. Их структура, свойства, классификация, маркировка, применение.
- •10. Конструкционные стали. Их структура, свойства, классификация, маркировка, применение.
- •11. Инструментальные стали. Их структура, свойства, классификация, маркировка, применение.
- •12. Белый и серый чугун. Влияние различных факторов (скорости охлаждения и состава) на формирование структуры серых чугунов. Маркировка серых чугунов.
- •14. Чугуны с шаровидным графитом.
- •15. Процесс получения ковких чугунов. Влияние примесей на процесс графитизации. Применение ковких чугунов.
- •16. Влияние формы графитных включений на свойства чугуна со свободным графитом.
- •17. Превращение в сталях при нагреве. Процесс образования аустенита. Перегрев и пережог.
- •19. Мартенситное превращение в стали. Его особенности. Закаливаемость и прокаливоемость стали.
- •21. Назначение и технология отжигов 1-го и 2-го рода.
- •22. Практические способы закалки сталей. Достоинства и недостатки. Дефекты, возникающие при закалке.
- •33.Цементируемые стали. Структура и термообработка.
- •43. Бронзы. Состав, маркировка, свойства.
1.Общая
характеристика металлов. Металлический
тип межатомной связи. 1)Металлы-
группа элементов, обладающая характерными
металлическими свойствами, такими как
высокие тепло- и электропроводность,
положительный температурный коэффициент
сопротивления, термоэлектронная эмиссия
(способность испускать электроны при
нагреве), высокая пластичность и
металлический блеск. Ме представляют
собой поликристаллические тела,
состоящие из большого числа мелких
различно ориентированных по отношению
друг к другу кристаллов. 2) Атом состоит
из положительного ядра и отрицательных
частиц — электронов. Внешние (валентные)
электроны Ме в отличие от неМе слабо
связаны с ядром. Поэтому атомы Ме легко
теряют валентные электроны, превращаясь
в ионы, в освободившиеся электроны
образуют так называемый электронный
газ. Ме-ая межатомная связь не имеет
направленного характера. Электроны
электронного газа не связаны с отдельными
атомами, а в одинаковой степени
принадлежат всем ионам металла. Наличие
ме-ой связи и легкоподвижных
коллективизированных электронов
объясняет характерные свойства металлов.
3) Атомно-кристаллическая
структура-
взаимное расположение атомов, существующее
в кристалле. Кристалл состоит из атомов,
расположенных в определенном порядке,
который периодически повторяется в 3
измерениях. Для описания а-к структуры
используют понятие кристаллической
решетки-
воображаемая пространственная сетка,
в узлах которой располагаются атомы,
образующие металл. Элементарная
кристаллическая решетка-
наименьший объем кристалла, дающий
представление об атомной структуре Ме
во всем V.
4) Вследствие неодинаковой плотности
атомов в различных плоскостях и
направлениях решетки многие св-ва
каждого кристалла зависят от направления
решетки. Такая неодинаковость свойств
монокристалла в разных кристаллографических
направлениях-анизотропия.
Кристалл- тело анизотропное в отличии
от аморфных тел. Технические
Ме- поликристаллы
(состоят из большого числа анизотропных
кристаллитов), в этом случае анизотропии
нет, т.к. расстояние между атомами по
всем направлениям примерно одинаково.
Аллотропией,
или полиморфизмом-
способность металлов в твердом состоянии
иметь различное кристаллическое
строение, а следовательно, и свойства
при различных температурах. Процесс
перехода из одной кристаллической
формы в другую называется полиморфным
превращением. Аллотропические формы
обозначают начальными буквами греческого
алфавита: альфа а, бета , гамма у, начиная
с той формы, которая существует при
более низкой температуре.
2. Несовершенства кристаллического строения металлов и их влияния на свойства. Дефекты кристаллического строения делятся по геом. признакам: а) точечные: оказывают влияние на физ. Св-ва (электропроводность,магнитные св-ва) и предопределяют процессы диффузии в Ме.- 1)«вакансии»- узлы решетки, в которых атомы отсутствуют. Образуются в результате перехода атома из узлов на поверхность или их полного испарения ( повышение температуры, пластическая деформация, бомбардировка Ме), 2) Межузельный атом- образуется в рез-те перехода атома из узла решетки в междоузлие. б) линейные, дислокации- лишняя полуплоскость верхней или нижней части кристалла; имеют большую l, маленькую h и ширину. Бывают краевые и винтовые (|| направлению сдвига, в) поверхностные- малы только в 1 измерении, представляют собой поверхности раздела между отдельными зернами или их блоками в поликристаллическом Ме. Каждое зерно Ме состоит из отдельных блоков, образующих субструктуру. Зерна Ме разориентированы относительно друг друг; блоки повернуты по отношению друг к другу.
3. Механизм кристаллизации металлов. Самопроизвольная кристаллизация. Кристаллизация- переход Ме из Ж в Т, сопровождается образованием кристаллической структуры имеющей дальний порядок. Протекает в условиях, когда система переходит к термодинамически более устойчивому состоянию с меньшей свободной энергией. Процесс кристаллизации начинается с образования кристаллических зародышей (центров кристаллизации) и продолжается в процессе роста их числа и размеров. Рост продолжается только в направлениях, где есть свободный доступ «питающей» жидкости, поэтому кристаллы сначала геометрически правильные получают неправильную внешнюю форму. Рост зародышей происходит в рез-те перехода атомов из переохлажденной Ж к кристаллам. Кристалл растет послойно, при этом каждый слой имеет одноатомную толщину. Самопроизвольная кристаллизация обусловлена стремлением Ме перейти в более устойчивое состояние за счет уменьшения свободной энергии. Температура, при которой F в Т и Ж равна- Ts- равновесная т-ра кристаллизации, поэтому для того, чтобы началась крис-ция T должна быть ниже Ts, а для плавления-выше. Выше Ts меньшей F обладает Ме в Ж состоянии, ниже-в Т.
4. Сплавы. Фазовый состав сплавов: твердые растворы, промежуточные фазы (хим. соединения). Сплав — макроскопически однородный металлический материал, состоящий из смеси двух или большего числа химических элементов с преобладанием металлических компонентов. Сплавы являются одним из основных конструкционных материалов, в промышленности применяются чаще чистых, т.к. выше мех. св-ва. Наибольшее значение имеют сплавы на основе железа и алюминия. В сплавах хим. Элементы могут взаимодействовать между собой, образуя различные по хим. Составу, типу связи и по строению кристаллические фазы. Эти кристаллы, образующиеся в сплавах в зависимости от их строения делят на 2 вида: 1) Твердые растворы- кристаллы переменного состава, в которых атомы растворенного компонента В размещены в кристаллической решетке компонента растворителя А; либо замещают атомы в узлах решетки, либо внедряются между атомами в поры решетки. Поэтому твердые р-ры бывают 2 видов: замещения и внедрения. Замещения могут иметь различное кол-во замещенных атомов, т.е. переменную растворимость. Вокруг атома растворенного в-ва возникают искажения пространственной решетки, что приводит к изменению ее размеров и св-в. Возрастают электросопротивление, твердость, прочность, падает пластичность. Это делает сплав конструкционным материалом с требуемым комплексом св-в. Внедрения возникают при сплавлении переходных Ме с не Ме, имеющими маленький атомный радиус (N, C). Эти в-ва легко проникают в большие поры решеток ГЦК и ГПУ. Пример: Ф, А, карбиды. Тв. Р-ры наиболее близки по свойствам компоненту растворителю, т.к. сохраняют его решетку и являются основой сплавов, подвергаемых ОМД.2) Промежуточные фазы- кристаллы, образовавшиеся в рез-те хим. Реакции между компонентами сплава. Имеют свой тип кристаллической решетки. Пример: цементит. Отличие от твердых растворов- не пластичны. Характерные особенности хим. соединений: 1) крис. Решетка отличается от решеток компонентов, обр. соединение. Атомы расположены упорядоченно 2) в соединении всегда сохраняется простое кртаное соотношение компонентов. 3) свойства соединения резко отличаются от св-в образующих его компонентов. 4) Т плавления постоянная. 5) Образование хим. соединения сопровождается тепловым эффектом. В отличии от твердых р-ров обычно образуются между компонентами, имеющими большое различие в электронном строении.
5. Свойства пластически деформированных металлов. Наклеп и рекристаллизация. При пластическом деформировании Ме одновременно с изменением формы меняется ряд св-в (при холодном- ↑ прочность). Пластичность обеспечивает конструкционную прочность деталей под нагрузкой. Пласт. дефор. осуществляется путем сдвига одной его части относительно другой. Сдвиг вызывает касат.напр..2 вида: скольжение и двойникование. При возрастании касательных напряжений выше предела упругости деформация становится необратимой. При снятии нагрузки устраняется лишь упругая составляющая деформации, остается пластичная часть деформации. Пластически деформированный Ме по сравнению с недеформированным находится в неравновесном, термодинамически неустойчивом состоянии. Поэтому даже при комнатных температурах в наклепанном металле протекают самопроизвольные процессы, приводящие металл в более устойчивое состояние. В результате пласт. деформирования Ме упрочняется; ↑ прочностные характеристики, электросопротивление и ↓ пластичность и ударная вязкость. С ↑ степени холодной деформации св-ва, характеризующие сопротивление деформации повышаются, а способность к пластической деформации- пластичность ↓. Это явление роста упрочнения- наклеп. Наклеп объясняется увеличением числа дефектов кристаллического строения (дислокаций, вакансий). Ме с ГЦК упрочняются сильнее, чем с ОЦК. При нагреве наклепанного Ме не восстанавливается старое зерно, а появляется совершенно новое, размеры которого могут существенно отличаться от исходного. Образование новых, равноосных зерен вместо ориентированной волокнистой структуры деформированного Ме – рекристаллизация обработки/ первичная рек-ция. Для начала первичной рекристаллизации необходимы: предварительная деформация наклепанного Ме должна быть больше критической; t нагрева должна превысить критическое значение. В рез-те рекристаллизации наклеп практически полностью снимается и св-ва приближаются к исходным значениям. При рекр-ции предел прочности и предел текучести резко ↓, а пластичность ↑. Разупрочнение объясняется снятием искажения решетки и резким уменьшением плотности дислокаций. Собирательная рекристаллизация- самопроизвольный процесс укрупнения зерен, образовавшихся на стадии первичной рек-ции. Вторичная рекристаллизация представляет собой стадию неравномерного роста одних зерен по сравнению с другими. Мех-ие св-ва подобной разнозернистой структуры хуже, чем однородной структуры рекристаллизованного Ме.
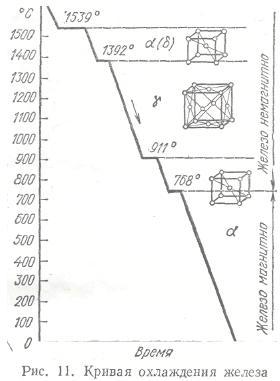
6. Компоненты и фазы в системе железо-углерод. Чистое железо- Ме серебристо-белого цвета. t плавления Fe- 1539. Известны 2 полиморфные модификации: α существует при t ниже 910 и выше 1392 и γ. Кристаллическая решетка α-железа- ОЦ куб. Кристаллическая решетка γ-железа- ГЦ куб. Углерод – неметаллический элемент II периода 4 группы, полиморфен. В обычных условиях он находится в виде модификации графита. Углерод растворим в Fe в Ж и Т состоянии, а также может быть в виде хим. соединения- Ц, а в высокоуглеродистых сплавах в виде графита. ФАЗЫ. В сис-ме Fe-C различают фазы: жидкий сплав, твердые растворы- Ф и А, а также Ц и графит. Феррит- твердый раствор углерода в α-железе. Атом углерода располагается в центре грани куба. Аустенит- твердый раствор углерода в γ-железе. Атом С располагается в центре элементарной ячейки и в дефектных областях кристалла. Цементит- хим. соединение железа с углеродом- карбид железа. В Ц. содержится 6,67% углерода. Ц. имеет сложную ромбическую решетку с плотной упаковкой атомов. Характерные особенности Ц : высокая твердость и малая пластичность, является метастабильной фазой ( в усл. равновесия в сплавах с высоким содержанием С образует графит). Графит. Кристаллическая решетка графита гексагональная слоистая. Графит мягок и обладает низкой прочностью. В лекции: сис-ма- совокупность фаз, находящихся в равновесии. Фаза- однородная составная часть сис-мы, имеющая свой хим. состав, кристаллическое строение или агрегатное состояние, свои св-ва и отделённая от другой части сис-мы поверхностью раздела.
7.
Диаграмма состояния системы
железо-цементит. Превращения при
нагревании и охлаждении. Диаграмма
состояния сис-мы сплавов в графической
форме показывает фазовый состав сплава
любой концентрации в зависимости от
t,
строится для условий равновесия.
Диаграмма состояния Fe-C
показывает фазовый состав и структуру
сплавов с концентрацией от чистого Fe
до цементита.
ABCD-
ликвидус (при ее пересечении начинается
кристаллизация). AHJEC-
солидус (конец кристаллизации). Между
L
и S
все сплавы в твердо-жидком состоянии.
По линии HJB
идет процесс полиморфизма (Ф→А).
Аустенит может существовать не ниже t
727 и содержание C-0,8%.
При 727 происходит эвтектоидное превращение
А в феррито-цементитную смесь- перлит.
Точка С показывает эвтектическое
превращение жидкого сплава с содержанием
С-4,3% в смесь кристаллов А и Ц, которая
называется ледебурит (высокотемпературный
и низкотемпературный). Относительно
точки С делятся на 3 структурных класса:
1) 2,14-4,3% доэвтектические (их отжигают
на ковкий чугун), 2) 4,3% эвтектические
(только ледебурит) переплавляют в сталь,
3) >4,3% заэвтектические, не находят
применение. Стали по структуре: 1)
эвтектоидные С=0,8 для ударного инструмента,
2) доэвтектоидная С=0,05-0,8 конструкционная,
3) заэвтектоидная С>0,8% в структуре Ц,
П. Первичная кристаллизация идет в
интервале температур, определяемых на
линиях ликвидус и солидус. Вторичная
кристаллизация вызвана превращением
Fe
одной модификации в другую и переменной
растворимостью углерода в А и Ф. Избыток
углерода из твердых растворов выделяется
в виде Ц. В системе Fe-C
происходят 3 изотермических превращения:
перитектическое HJB
1499°, эвтектическое
ECF
1147°, эвтектоидное PSK
727°. При охлаждении ледебурита до
температур ниже SK
входящий в него аустенит превращается
в перлит, и при 20° ледебурит представляет
собой смесь Ц и П.

8. Влияние углерода, постоянных примесей на свойства сталей. Влияние С: структура стали после медленного охлаждения состоит из Ф и Ц. Кол-во Ц возрастает прямо пропорционально содержанию углерода. Твердые и хрупкие частицы Ц повышают сопротивление деформации, уменьшают пластичность и вязкость. Вследствие этого с ↑ С возрастают твердость, пределы прочности и текучести, электросопротивление, ↓относительное удлинение, теплопроводность и ударная вязкость. Влияние кремния и марганца. В углеродистой стали кремния 0,35-0,4%, марганца 0,5-0,8%. Они переходят в сталь в процессе ее раскисления при выплавке. Они раскисляют сталь, т.е. соединяясь с кислородом закиси железа в виде окислов переходят в шлак. Эти процессы улучшают св-ва стали. Кремний, дегазируя Ме повышает плотность слитка, а также повышает предел текучести. Марганец повышает прочность, не снижая пластичности. Влияние серы: сера является вредной примесью в стали. С железом она образует соединение FeS, которое практически нерастворимо в нем в твердом состоянии. Сернистые включения сильно снижают мех. св-ва, особенно ударную вязкость и пластичность. Кроме того улучшают свариваемость и коррозионную стойкость. Содержание серы ограничивается 0,035-0,06%. Влияние фосфора: Фосфор вредная примесь и содержание его допускается 0,025-0,045%. Растворяясь в феррите, фосфор сильно искажает кристаллическую решетку и увеличивает пределы прочности и текучести, но ↓ пластичность и вязкость. Влияние N, O2, H2: Примеси внедрения (N, O2,) повышают порог хладноломкости и понижают сопротивление хрупкому разрушению. Неме-кие включения (окислы, нитриды) понижают предел выносливости и вязкости. Растворенный в стали водород охрупчивает сталь.
9. Углеродистые стали. Их структура, свойства, классификация, маркировка, применение.
В
зависимости от назначения стали
делят на: конструкционные (детали
машин, механизмов и различных конструкций,
болты, гайки, мосты, краны); инструментальные
стали (режущий инструмент, мерительный
инструмент, штампы). По структуре:-
доэвтектоидные;- эвтектоидные;-
заэвтектоидные. По содержанию углерода:-
малоуглеродистые (0,025ч0,25%С);-
среднеуглеродистые (0,25ч0,6%С); -
высокоуглеродистые (> 0,6%С). По качеству:
- обыкновенного качества ( <0,05%S;
<0,04%Р); - качественные; высококачественные.
Качество сталей определяется содержанием
в них вредных примесей: серы и фосфора.
Конструкционные стали изготавливают
обыкновенного качества и качественными;
инструментальные стали - качественными
и высококачественными. По
степени удаления кислорода из стали,
т. е. По степени её раскисления, существуют:
спокойные
стали, т. е.,
полностью раскисленные; такие стали
обозначаются буквами “сп” в конце
марки; кипящие
стали -
слабо раскисленные; маркируются буквами
"кп"; полуспокойные
стали,
занимающие промежуточное положение
между двумя предыдущими; обозначаются
буквами "пс".
По качеству
стали, классифицируют на: обыкновенного
качества,
качественные,
высококачественные. Под качеством
стали понимается совокупность свойств,
определяемых металлургическим процессом
ее производства. Стали обыкновенного
качества бывают только углеродистыми
(до 0,5 % С), качественные и высококач. –
углеродистыми и легированными.
Стали обыкновенного качества обозначают
буквами "Ст" и условным номером
марки в зависимости от химического
состава и механических свойств. Чем
выше содержание углерода и прочностные
свойства стали, тем больше её номер.
Буква "Г" после номера марки
указывает на повышенное содержание
марганца в стали. Перед маркой указывают
группу стали, причем группа "А" в
обозначении марки стали не ставится.
Качественные
конструкционные углеродистые стали.
Эти стали
выплавляют кислородно-конверторным
способом, в мартеновских печах или
электропечах. В зависимости от раскисления
они могут быть спокойными или кипящими.
К стали этой группы предъявляются
более высокие требования относительно
химического состава: меньше содержание
серы – ![]() 0,04%,
фосфора –
0,04%,
фосфора –![]() 0,035%;
меньше количество неме-их включений;
повышенные требования к макро- и
микроструктуре сплава. Поставляются
стали по гарантированному хим. составу
и механическим свойствам. Маркировка
производится цифрами по ГОСТ1050-88: 05,
08, 10, 15, 20, …70, 75, 85,…08ю (Al), 10кп. Цифры
указывают среднее содержание углерода
в сотых долях процента. Стали 65, 70, 75, 80
можно отнести к группе рессорно-пружинных
сталей (характеризуются высоким пределом
упругости). Сталь предназначается для
горячей обработки давлением, механической
обработки.Области
применения углеродистых качественных
конструкционных сталей. 05кп,
08, 08кп, 08ю – детали изготавливаемые
холодной штамповкой и глубокой вытяжкой
(кузова, крылья автомобилей, топливные
баки, змеевики, элементы сварных
конструкций); 10, 15 – используют для
деталей не испытывающих высоких
нагрузок: кулачковые валики, рычаги,
оси, втулки, болты, гайки, заклепки,
муфты. 20, 25 – крепежный материал,
соединительные муфты, шпиндели, толкатели
клапанов, пальцы рессор, рамы и другие
детали автотракторного с/х машиностроения.
30, 35 – слабонагруженные оси, валы
различных машин и механизмов, шпиндели,
шестерни ,рычаги, звездочки, кольца,
шатуны. 40, 45, 50 – средненагруженные оси,
валы, шестерни, втулки, коленчатые валы,
плунжеры, фрикционные диски. 60, 65, 70, 75,
80, 85 – пружины, рессоры, шпиндели,
замковые шайбы, прокатные валки, ж/д
рельсы, крановые колеса. Инструментальные
качественные углероды.
Маркируются углеродистые инструментальные
стали: У7, У8, У10, У11, У12, У13, У14. Цифра
показывает среднее содержание углерода
в десятых долях процента. Стали могут
быть качественные и высококачественные.
Обозначение высококачественных
углеродистых инструментальных сталей:
У7А, У8А, …, У13А. Эти стали не обладают
теплостойкостью, рабочая температура
не более 190-2000С (при нагреве выше
происходит резкое снижение твердости
режущей кромки) с HRC62-63 до HRC15-18 (НВ
170-180). Области применения инструментальных
сталей: У7, У7А – зубила, молотки,
плоскогубцы, кусачки, пневмоинструмент.
У8, У8А – фрезы, ножи, зенковки, штампы,
матрицы, пуансоны, ножницы,
деревообрабатывающий инструмент. У9,
У9А, У10, У10А – сверла, метчики, развертки,
плашки, матрицы для холодной штамповки.
0,035%;
меньше количество неме-их включений;
повышенные требования к макро- и
микроструктуре сплава. Поставляются
стали по гарантированному хим. составу
и механическим свойствам. Маркировка
производится цифрами по ГОСТ1050-88: 05,
08, 10, 15, 20, …70, 75, 85,…08ю (Al), 10кп. Цифры
указывают среднее содержание углерода
в сотых долях процента. Стали 65, 70, 75, 80
можно отнести к группе рессорно-пружинных
сталей (характеризуются высоким пределом
упругости). Сталь предназначается для
горячей обработки давлением, механической
обработки.Области
применения углеродистых качественных
конструкционных сталей. 05кп,
08, 08кп, 08ю – детали изготавливаемые
холодной штамповкой и глубокой вытяжкой
(кузова, крылья автомобилей, топливные
баки, змеевики, элементы сварных
конструкций); 10, 15 – используют для
деталей не испытывающих высоких
нагрузок: кулачковые валики, рычаги,
оси, втулки, болты, гайки, заклепки,
муфты. 20, 25 – крепежный материал,
соединительные муфты, шпиндели, толкатели
клапанов, пальцы рессор, рамы и другие
детали автотракторного с/х машиностроения.
30, 35 – слабонагруженные оси, валы
различных машин и механизмов, шпиндели,
шестерни ,рычаги, звездочки, кольца,
шатуны. 40, 45, 50 – средненагруженные оси,
валы, шестерни, втулки, коленчатые валы,
плунжеры, фрикционные диски. 60, 65, 70, 75,
80, 85 – пружины, рессоры, шпиндели,
замковые шайбы, прокатные валки, ж/д
рельсы, крановые колеса. Инструментальные
качественные углероды.
Маркируются углеродистые инструментальные
стали: У7, У8, У10, У11, У12, У13, У14. Цифра
показывает среднее содержание углерода
в десятых долях процента. Стали могут
быть качественные и высококачественные.
Обозначение высококачественных
углеродистых инструментальных сталей:
У7А, У8А, …, У13А. Эти стали не обладают
теплостойкостью, рабочая температура
не более 190-2000С (при нагреве выше
происходит резкое снижение твердости
режущей кромки) с HRC62-63 до HRC15-18 (НВ
170-180). Области применения инструментальных
сталей: У7, У7А – зубила, молотки,
плоскогубцы, кусачки, пневмоинструмент.
У8, У8А – фрезы, ножи, зенковки, штампы,
матрицы, пуансоны, ножницы,
деревообрабатывающий инструмент. У9,
У9А, У10, У10А – сверла, метчики, развертки,
плашки, матрицы для холодной штамповки.
