
- •Лекція № 1. Основні напрями розвитку біотехнології
- •Біоенергетика
- •Біотехнологія обробки стоків і контроль забруднення води важкими металами
- •Сільськогосподарська біотехнологія
- •Біогеотехнологія
- •Біоелектроніка
- •Біотехнологія в медицині
- •Біотехнології в харчовій промисловості
- •Біотехнологія молочних продуктів
- •Виробництво спиртів і поліолів
- •Виробництво вторинних метаболітів
- •Біотрансформація
- •Виробництво ферментів
- •Виробництво амінокислот, органічних кислот, вітамінів
- •Біоконверсія лігноцелюлозних об'єктів
- •Використання грибів у біотехнології
- •Найпростіші в біотехнології
- •Водорості
- •Рослини в біотехнології
- •Стадії біотехнологічного виробництва
- •Технологія виготовлення поживного середовища для біосинтезу
- •Підтримка чистоти культури
- •Ферментація, будова ферментера
- •Загальні принципи розділення речовин
- •Одержання готових товарних форм препаратів
- •Субстрати для культивування мікроорганізмів з метою одержання білка
- •Лекція № 6. Технологія одержання мікробних ліпідів
- •Мікроорганізми – продуценти ліпідів
- •Лекція № 7. Технологія одержання ферментних препаратів
- •Глибинний метод виробництва ферментів
- •Виробництво ферментів при поверхневому культивуванні продуцентів
- •Іммобілізація ферментів
- •Класифікація носіїв для ферментів
- •Методи іммобілізації ферментів
- •Застосування іммобілізованих ферментів
- •Іммобілізація клітин
- •Ентомопатогенні препарати грибів
- •Вірусні ентомопатогенні препарати
- •Бактеріальні добрива на основі бульбочкових бактерій
- •Виробництво азотобактерину
- •Бактеріальне добриво фосфобактерин
- •Антибіотики для сільського господарства
- •Лекція № 9. Культура клітин рослин
- •Сфери застосування культур рослинних клітин
- •Культури клітин вищих рослин. Історія методу
- •Морфофізіологічні характеристика каллусних тканин
- •Фактори, що впливають на морфогенез in vitro
- •Генетичні механізми, що обумовлюють диференціювання клітин у культурі
- •Суспензійні культури
- •Методики культивування одиночних рослинних клітин
- •Необхідність іммобілізації рослинних клітин, методи
- •Фізіологічні основи переваги іммобілізованих рослинних клітин перед традиційними способами культивування
- •1. Клітини, іммобілізовані в або на інертному субстраті, утворюють біомасу набагато повільніше, ніж зростаючі в рідких суспензійних культурах.
- •2. Крім повільного росту іммобілізація клітин дозволяє їм рости в тісному фізичному контакті одине з одним, що сприятливо позначається на хімічних контактах.
- •Системи культивування іммобілізованих клітин
- •Застосування ізольованих протопластів
- •Способи отримання і культивування протопластів
- •Способи культивування протопластів
- •Злиття протопластів (парасексуальная гібридизація)
- •Види соматичних гібридів
- •Конструювання клітин
- •Клітинна селекція. Методи клітинної селекції
- •Генетичні основи застосування культури клітин в селекційних цілях
- •Типи клітинних культур, які використовуються в селекції
- •Переваги клітинної селекції перед традиційними селекційними методами
- •Мікроклональне розмноження і оздоровлення рослин
- •Фактори, впливають на процес клонального мікророзмноження
- •Етапи мікроклонального розмноження рослин
- •Методи клонального мікророзмноження
- •Оздоровлення посадкового матеріалу від вірусів методами хіміотерапії і термотерапії
- •Створення штучних асоціацій клітин вищих рослин
- •Підвищення продуктивності сільськогосподарських рослин
- •Ендосимбіотичні асоціації
- •Екзосимбіотичні асоціації з водоростями, грибами, азотфіксаторами
- •Методи збереження генофонду. Методика кріоконсервації, способи уповільнення росту
- •Безклітинні системи в біотехнології. Мембрани хлоропластів
- •Одержання фотогальванічних елементів з використанням бактеріальних мембран
- •Безклітинні білоксинтезуючі системи (ббсс)
- •Лекція № 10. Біотехнологія одержання культури тваринних клітин і тканин
- •Культивування клітин. Історія методу
- •Введення клітин у культуру, їхнє походження
- •Характеристика клітин, що культивуються in vitro
- •Поживні середовища й умови культивування
- •Системи культивування клітин
- •Використання культури клітин людини
- •Культивування клітин і тканин безхребетних
- •Культивування органів
- •Гібридизація тваринних клітин. Історія методу
- •Методи створення експериментальних химер
- •1. Агрегаційний – був запропонований практично одночасно й незалежно один від одного Тарковським у Варшаві та Мінц у Філадельфії (1961-1962 р.).
- •2. Ін’єкційний – був розроблений р. Гарднером у 1968 р.
- •Механізм злиття клітин
- •Моноклональні антитіла. Функціональна структура антитіл
- •Одержання моноклональних антитіл
- •Методи аналізу: імуноферментний (іфа), імунолюмінесцентний, імунорадіологічний
- •Радіоактивні мітки
- •Застосування моноклональних антитіл
- •Клонування тваринних клітин. Історія клонування
- •Методи трансплантації ядер
- •Клонування ссавців. Історія клонування
- •Регулювання відтворення сільськогосподарських тварин
- •Суперовуляція
- •Аеробне очищення стічних вод
- •Анаеробні системи очищення
- •Показники забруднення стічних вод
- •Перелік питань які виносяться на підсумковий контроль
- •Література
Методи аналізу: імуноферментний (іфа), імунолюмінесцентний, імунорадіологічний
Висока специфічність антитіл відносно антигену перетворює їх у потужний інструмент для ідентифікації різних речовин, будь то макромолекули, клітинні фрагменти або цілі клітини.
Початок широкому використанню антитіл у діагностичних цілях поклав в 1955 році американський імунолог А. Кунс. Він приєднав до антитіл барвник, що світиться. Флуоресцентні антитіла зробили видимими місця розташування молекул, які його цікавили, у клітині. Цей метод отримав назву імунофлуоресцентного. Чутливість методу можна підвищити декількома шляхами.
У першому випадку імунна відповідь підсилюється за рахунок застосування антитіл декількох порядків:

Антиген іммобілізується на підкладці, до нього додаються антитіла 1-го порядку, що зв’язуються безпосередньо з антигеном. У досліджуваний зразок додаються антитіла 2-го порядку, що зв’язуються з антигенними детермінантами антитіл 1-го порядку. Антитіла 2-го порядку мають флуоресцентну (або іншу) мітку. Оскільки ділянок зв’язування може бути декілька, то реакція проявляється більш чітко.
Інша система посилення сигналу заснована на високій спорідненості біотину (низькомолекулярного розчинного вітаміну) до стрептовідину (бактеріального білка). В даному випадку можливі два варіанти:
А. Якщо можливо ковалентно зв’язати біотин безпосередньо з антитілами, то стрептовідин мітять маркером і використовують аналогічно антитілам другого порядку:
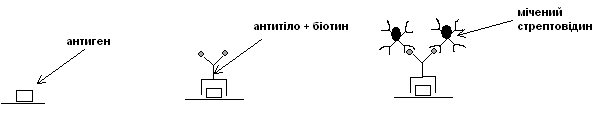
Б. Система “біотин-антитіло + стрептовідин + мічений біотин”:

У цьому випадку утвориться ціла сітка з молекул стрептовідину, зв’язаного з міченим біотином. Отже, відбувається багаторазове посилення сигналу.
Застосування антитіл другого й третього порядків дозволяє також спрощувати процедуру визначення мікроорганізмів у мазку. При цьому не обов’язково мати мічені антитіла проти всіх бактерій. Досить мати звичайні антитіла кролика або миші проти мікроорганізму, що цікавить, і мічені МКА проти цих імуноглобулінів. Якщо мікроорганізм у мазку присутній, то до нього “приклеються” специфічні антитіла, а до них уже – мічені. У результаті мазок буде світиться при люмінесцентній мікроскопії. Фотометричні або флуоресцентні методи можуть бути використані не у всіх випадках, наприклад, якщо вимірювання проводять в дуже мутному середовищі.
Крім барвника в якості мітки можна використати фермент (імуноферментний аналіз) або радіоактивний ізотоп (імунорадіологічний). Від чутливості детекції маркера залежить чутливість методу аналізу.
Радіоактивні мітки
Вибір маркера й способу його «прив’язки» до антигену є одним з важливих етапів у проведенні аналізу. Спочатку широко застосовувалися радіоізотопні мітки (радіоімуний аналіз – РІА), запропоновані американськими дослідниками (С. А. Берсон, Р. С. Ялоу, 1959). Однак в останні роки усе більше використовуються як маркери ферменти. Це обумовлено рядом принципових труднощів, пов’язаних із застосуванням ізотопниx маркерів. Так, ізотоп 125I має час напіврозпаду 60 діб, чим обмежується строк його використання. Ізотоп 3Н має тривалий час життя (12,5 років), однак під дією β-випромінювання відбувається розпад молекул антигену, у результаті чого час життя мічених 3Н-сполук теж обмежений. Крім того, ефективність тритію істотно нижча, ніж 125I. Обмежуючими факторами РІА є складність і висока вартість устаткування, необхідність централізованої системи розподілу імунохімічних наборів, мічених радіоактивними ізотопами, певна небезпека ізотопів для навколишнього середовища. З огляду на труднощі використання радіоізотопних міток, були запропоновані як маркери ферменти.
При імуноферментному аналізі антиген зв’язується з поверхнею лунки полістирольного планшета. У лунку додають антитіла, що несуть фермент у якості мітки, інкубують і відмивають. Далі доливають субстрат, що змінює забарвлення при взаємодії із цим ферментом. Зміну забарвлення можна виміряти за допомогою спектрофотометрії. Таким способом проводиться індикація й кількісна оцінка біоорганічних сполук із чутливістю до 10-12 г/літр.
У наш час відомо більше 2000 різних ферментів, однак тільки деякі знаходять застосування в імуноферментному аналізі. Це пояснюється високими вимогами, що висуваються до властивостей ферментів. Фермент повинен бути високо активний, а продукти його реакції детектуватися з високою чутливістю, він повинен бути стабільним, так щоб його активність зберігалася не менше одного року. Вміст фермента-маркера в певному зразку повинно бути мінімальним. Саме через це для різних об’єктів використовують різні ферменти. У багатьох випадках, коли необхідний якісний результат, оцінка імунохімічної реакції може бути проведена візуально.
Для введення ферментативної мітки розроблено багато різних хімічних, біохімічних й імунологічних способів.
Першим реагентом, використаним для синтезу імуноферментних кон’югатів, був глутаровий альдегід, що реагує з аміногрупами лізинових білкових молекул. За допомогою глутарового альдегіду отримані кон’югати антитіл й антигенів з пероксидазою, лужною фосфатазою, глюкоамілазою. У наш час широко використовуються імунопероксидазні кон’югати й кон’югати з β-галактозидазою.
Ковалентні методи одержання імуноферментних кон’югатів мають досить широке поширення, однак в деяких випадках дія зшиваючого реагенту, негативно позначається на ферментативній й імунологічній активності компонентів гібридної макромолекули. У зв’язку з цим певний інтерес представляють імунологічні методи введення ферментної мітки.
Один з підходів одержав назву методу «гібридних антитіл». Ферментативним гідролізом одержують Fab-фрагменти молекул антитіл проти антигену, який визначають й використовуваний фермент. Потім суміш продуктів гідролізу піддають відновленню меркаптоетанолом; при цьому Fab-фрагменти зворотно дисоціюють на симетричні частини. Після видалення відновлюючого агента молекули знову асоціюють, утворюючи гібридні молекули антитіл, специфічні до антигену, який визначається й ферменту. При додаванні ферменту утворюється комплекс антитіло-фермент. Гібридомна технологія відкриває принципово новий шлях одержання гібридних антитіл, що полягає в тому, що зливаються моноклональні клітини, специфічні проти даного антигену й ферменту-маркера, у результаті чого утворюються гібридоми другого покоління, які синтезують антитіла, з двома специфічностями.
Інший шлях полягає в тому, що одержують антитіла того самого виду тварини (наприклад, кролика) проти антигену, що визначається й ферменту, які з’єднують між собою через антитіла іншого виду тварин (антитіла барана проти кролика). Додавання ферменту до такої потрійної молекули також призводить до утворення комплексу антитіло-фермент. У наш час розробляються підходи одержання гібридних антитіл методами клітинної й генної інженерії, що дозволить істотно спростити спосіб їхнього одержання.
Стабільність імуноферментних кон’югатів при зберіганні – найважливіший параметр, що зумовлює можливість їхнього практичного використання. Методи спрямованої стабілізації кон’югатів поки ще не розроблені. Не існує також кореляції між стабільністю кон’югатів і методом їхнього одержання. Однак висока стабільність гібридних молекул забезпечує їхнє застосування на практиці й значно перевершує стабільність антитіл й антигенів, мічених радіоактивними ізотопами. У ліофілізованому стані ферментні кон’югати зберігають свої властивості до двох років.
Крім ферментів як маркери можуть бути використані субстрати. Зокрема, в імунокофакторному аналізі застосовуються як мітки АТФ і НАД, які можуть бути «пришиті» до молекули антигену через аденіновий залишок таким чином, що зберігається їхня здатність взаємодіяти з ферментом. Аналогічно були використані субстрати пероксидази (люмінол, ізолюмінол), які можуть бути окислені пероксидом водню в реакції хемілюмінесценції, що каталізується пероксидазою.
