
- •Міністерство освіти і науки україни
- •1. Об’єкт, предмет, завдання та методи аналітичної хімії.
- •1.1. Історія розвитку та завдання аналітичної хімії.
- •1.2. Характеристика методів аналізу
- •2. Якісний хімічний аналіз як перший ступінь аналітичного дослідження.
- •2.1. Якісний аналіз та методи якісного аналізу.
- •2.2. Системи якісного аналізу катіонів.
- •2.3. Систематичний і дробний хід аналізу
- •3.2. Теорія електролітичної дисоціації.
- •3.4. Теорія сильних електролітів.
- •Приклад: визначити іонну силу 0,15м NaCl
- •3.6. Буферні розчини.
- •3.7. Сучасні уявлення про природу кислот та основ
- •4. Теоретичні основи аналітичної хімії. Рівновага в гетерогенній систем.
- •4.1. Добуток розчинності.
- •Умови утворення і випадіння осаду
- •4.3. Дробне осадження
- •1Моль 1моль
- •4.4. Випадки розчинення осадів
- •5. Рівноваги у розчинах солей, що гідролізують, та амфотерних сполуках.
- •5.1.Реакції гідролізу.
- •1Моль 1моль
- •5.2. Значення гідролізу в якісному аналізі:
- •6. Використання комплексних сполук, колоїдних систем та окисно-відновних реакцій у якісному аналізі.
- •6.1. Класифікація комплексних сполук.
- •Класифікація комплексних сполук
- •6.2. Використання координаційних сполук
4.3. Дробне осадження
На практиці в якісному аналізі використовують дробне осадження. За правилом ДР в першу чергу, піде реакція при якій утворюється найменш розчинна сполука. Задачі, в яких розглядається додавання реактиву до суміші йонів, розв’язуються теж за правилом ДР.
Приклад. Яка з солей буде осаджатися першою, якщо до суміші 0,1М розчинів KCl і K2CrO4 додавати по краплям AgNO3.
C (KCl)
= C(K2CrO4)
= 0.1 моль/л Беремо з довідника ДР(AgCl) =
1,78 · 10-10
(KCl)
= C(K2CrO4)
= 0.1 моль/л Беремо з довідника ДР(AgCl) =
1,78 · 10-10
AgNO3 ДР (Ag2CrO4) = 1,1 · 10-12
Розраховуємо за якої молярної концентрації Ag+ буде утворюватися осад (AgCl)
AgCl ↔ Ag+ + Cl-
1Моль 1моль
х моль 0,1моль
ДР(AgCl) = [Ag+]·[Cl-]
![]()
2) Ag2CrO4 ↔ 2Ag++CrO42-
2 моль 1моль
2х моль 0,1моль
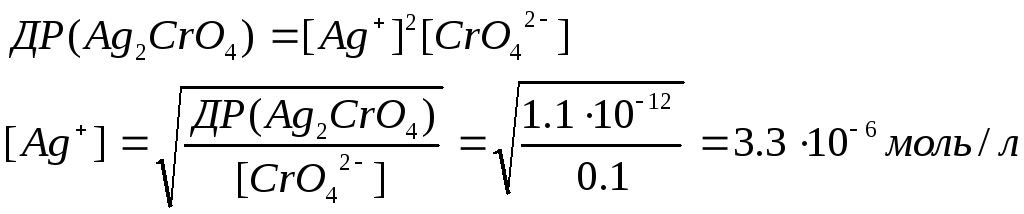
Отже, першим буде осаджуватися AgCl, оскільки для його осадження необхідно значно меншу молярну концентрацію речовини Ag+.
4.4. Випадки розчинення осадів
При проведенні хімічного аналізу часто необхідно розчинити осади.
1) Розчинення основ.
Основи, нерозчинні у воді, розчиняються в розведених кислотах. Це пояснюється тим, що у присутності кислоти порушується динамічна рівновага, яка є в насиченому водному розчині основних гідроксидів.
Щоб розчинити осад-основу, треба підібрати такий розчинник, один з йонів якого утворював би слабодисоційовану сполуку з одним з йонів основи, яку розчиняють.
Mg(OH)2 ↔ Mg2+ + 2OH-
Осад розчин
Додали 2НNO3 → 2H++2NO3-
2OH- + 2H+ = 2H2O або
Mg(ОН)2 + 2H+ = Mg2+ + 2H2O
Деякі основи (Mg(OH)2, Fe(OH)2, Mn(OH)2, Ni(OH)2) розчиняються в міцному розчині NH4Cl
Mn(OH)2 ↔ Mn2+ + 2OH-
Осад розчин
Додали 2NH4Cl ↔ 2NH4+ + 2Cl-
2NH4+ + 2OH - ↔ 2NH4OH або
Mn(OH)2 + 2NH4+ ↔ Mn2+ + 2NH4OH
Розчинення кислот (кислотних гідроксидів)
Малорозчинні кислотні гідроксиди (H2SiO3, H2WO4, H2MoO4) легко розчиняються в лугах
2NaOH → 2Na+ + 2OH-
H2SiO3 + 2OH-↔ SiO32- + 2H2O
5. Рівноваги у розчинах солей, що гідролізують, та амфотерних сполуках.
5.1.Реакції гідролізу.
Реакції гідролізу використовуються в якісному аналізі як характерні реакції відкриття ряду катіонів (наприклад: Sb3+, Bi3+, Fe3+) і аніонів (CH3COO-, SiO32-); для розділення Cr3+ і Al3+ - йонів; для регулювання рН і рОН розчинів (наприклад: додаванням катіонів чи аніонів – NH4+, CH3COO-). Залежно від складу солей розрізняють такі типи реакцій гідролізу:
Гідроліз солі, яка при дисоціації у водному розчині утворює катіон, який не виявляє поляризаційні та акцепторні властивості і аніон – сильний електронодонор (аніон слабкої кислоти – гідроліз за аніоном).
Приклад: CH3COONa + H2O ↔ CH3COOH + NaOH
CH3COO- +Na+ + H+OH- ↔ CH3COO- + H+OH-
CH3COO- + H+OH- ↔ CH3COOH + OH-
PH>7 лужне
Гідроліз солі, яка при дисоціації у водному розчині утворює катіон – сильний комплексоутворювач і аніон – слабкий електронодонор (катіон слабкої основи – гідроліз за катіоном)
Приклад: NH4Cl + H2O ↔ NH4OH + HCl
NH4+ + Cl- + H+OH- ↔ NH3 ·H2O + H+ + Cl-
NH4+ + H+OH- ↔ NH3 · H2O + H+
PH<7 кисле
Гідроліз солі, яка при досоціації у водному розчині утворює катіон – сильний комплексоутворювач і аніон – сильний електронодонор (катіон слабкої основи і аніон слабкої кислоти – гідроліз солі за катіоном і аніоном)
CH3COONH4 + H2O ↔ CH3COOH + NH4OH
CH3COO- + NH4+ + H+OH- ↔ CH3COOH + NH3 · H2O
Кількісно гідроліз характеризується ступенем гідролізу (h) і константою гідролізу (Кг).
Ступінь гідролізу (h) виражає відношення речовини солі Х (молярної концентрації речовини в моль/л), що прогідролізувала, до загальної кількості речовини Х (молярної концентрації моль/л)
![]()
![]() ,
,
![]() h
- виражається в частках одиниці або у
процентах (%)
h
- виражається в частках одиниці або у
процентах (%)
Константа гідролізу (Кг) показує відношення добутку молярних концентрацій речовин продуктів гідролізу до молярної концентрації речовин негідролізованих йонів солі у розчині (записують скорочене йонно-молекулярне рівняння реакції гідролізу).
Перший тип гiдролiзу солей чи солеподібних сполук.
Приклад, натрій ацетат (CH3COONa). При розчиненнi у водi натрій ацетату проходять процеси гiдратацiї i дисоцiацiї:
CH3COONa(к) + nH2O → Na+гiдр. + CH3COO–гiдр.
а потiм гiдролiзу:
Кiлькiсна оцiнка реакцiї гiдролiзу натрiй ацетату, CH3COONa:
CH3COO- + H+OH- ↔ СН3СОOH+ОН-
