
- •2011 Укладачі:Столяренко Геннадій Степанович, д.Т.Н., професор; Паранько н.Г., старший викладач. Рецензент: Вязовик Віталій Миколайович, к.Т.Н., доцент
- •1.2 Мембрани, що використовують в процесах зворотного осмосу і ультрафільтрації
- •1.3 Фізико-хімічні основи мембранних методів
- •1.4 Зворотній осмос
- •1.5 Ультрафільтрація
- •6 Розрахункова частина
- •1.2 Вплив в’язкості і температури на процес розділення
- •3 Розрахункова частина
- •1 Теоретичні основи
- •2 Опис лабораторної установки та послідовність виконання роботи
3 Розрахункова частина
Параметри вихідного розчину внести в таблицю 1.
Таблиця 1 – Параметри вихідного розчину
|
№ розчину |
Компонент, що вилучається з розчину
|
Динамічний коефіцієнт в’язкості, Па·с |
Концентрація компоненту, мг/дм3 |
|
|
|
|
|
Експериментальні дані заносимо у таблицю 2.
Таблиця 2 – Експериментальні дані
|
№ розчину |
Витрати концентрату, дм3/год |
Об’єм розчину, що пройшов через мембрану, дм3 |
Тиск робочий, Па |
Температура робоча, ºС |
|
|
|
|
|
|
Визначити концентрацію компоненту, що вилучається, у пермеаті та розраховати селективність та проникність мембрани за формулами (3) та (4) відповідно. Розрахункові дані занести у таблицю 3.
Таблиця 3 – Розрахункові дані
|
№ розчину |
Концентрація компоненту, що вилучається, у пермеаті, мг/дм3 |
Селективність мембрани, % |
Проникність мембрани, дм3/(м·год) |
|
|
|
|
|
Контрольні питання
Які основні принципи розділення розчинів речовин різної природи ?
Які закономірності розділення багатокомпонентних розчинів електролітів та розчинів, що містять одночасно органічні та неорганічні компоненти?
Як впливають добавки ПАР на селективність та проникність мембран?
Як впливає температура на селективність та проникність ацетатцелюлозних мембран для зворотного осмосу?
Яка залежність селективності та проникності мембрани від в’язкості розчину?
Пояснити рівняння залежності питомої проникності мембрани від температури.
Який принцип роботи установки розділення сумішей на високонапірних комірках?
За якими формулами визначаються селективність та проникність мембрани?
Перелік посилань
Ю. И. Дытнерский. Баромембранные процессы. Теория и расчет. М.: Химия, 1986. – 272 с.
Кочаров Р. Г. Теоретические основы обратного осмоса. Учебное пособие – М.: РХТУ им. Д. И. Менделеева, 2007. – 143 с.
Ю. И. Дытнерский. Обратный осмос и ультрафильтрация. – М.: Химия, 1978. – 356 с.
Міністерство освіти і науки України
освіти і науки України
черкаський державний технологічний університет
кафедра хімічної технології неорганічних речовин
Лабораторна робота №3
ТЕМА: «РОЗДІЛЕННЯ РОЗЧИНІВ МЕТОДАМИ ЗВОРОТНОГО ОСМОСУ І УЛЬТРАФІЛЬТРАЦІЇ ВІД ВАЖКИХ МЕТАЛІВ»
МЕТА РОБОТИ: вивчення
процесу розділення розчинів методами
зворотного осмосу і ультрафільтра ції
від важких металів
ції
від важких металів
1 Теоретичні основи
У промисловості часто доводиться розділяти розбавлені розчини, що містять іони важких металів з близькими властивостями. Для виділення з багатокомпонентних розчинів потрібного електроліту перспективно використовувати комбінований метод, що включає комплексоутворення і ультрафільтрацію. Він полягає в тому, що іони електроліту, що підлягають виділенню, утворюють з введеним в розчин, що розділяється, високомолекулярним поліелектролітом (так званим комплексоутворювачем) координаційні сполуки – полімерні комплекси. Розмір цих комплексів набагато більше розміру незв'язаних іонів, тому, при продавлюванні розчину через мембрану для ультрафільтрації, останні разом з розчинником проходять через неї, утворюючи пермеат, а полімерний комплекс залишається в концентраті.
З випробуваних полімерних добавок (полікислот, поліоснов, поліакриламіда, промислових полімерних флокулянтів і т. д.) якнайкращі результати були отримані при використанні поліетиленіміна (ПЕІ) з середньою молекулярною масою 30000 і розгалуженою будовою молекул. Цей полімер відрізняється здатністю утворювати з багатьма іонами кольорових і важких металів комплексні сполуки, які згодом легко можуть бути зруйновані, наприклад, підкисленням розчину або електролізом. Перераховані властивості поліетиленіміна дозволяють багато разів використовувати його для комплексоутворення.
Ефективність концентрації
полімерного комплексу ультрафільтрацією
в першу чергу визначається діаметром
пор і матеріалом мембрани. Великопористі
мембрани володіють високою питомою
продуктивністю, а мембрани з порами
невеликих розмірів краще затримують
полімерний комплекс. З мембран на основі
ароматичного поліаміду, ацетилцелюлози
і етилцелюлози найбільш відповідними
виявилися мембрани з перших двох
полімерів з порами середнім діаметром
20—30 нм. При затриманні комплексу
нікель-поліетиленімін при рН 9,0 на
ацетатцелюлозній мембрані з пора ми
діаметром 20 нм φ = 98%, тоді як на
этилцелюлозній мембрані з такими ж
порами φ = 45%. Така відмінність в
селективності мембран з різних матеріалів
пояснюється неоднаковою сорбцією на
них поліетиленіміна, що приводить до
зменшення ефективного розміру пор
різною мірою. Для виділення металів
методом комплексоутворення з подальшою
ультрафільтрацією можна рекомендувати
плоскі ацетатцелюлозні і поліамідні
мембрани УАМ і УПМ, а також поліамідні
мембрани УПА у вигляді порожнистих
волокон.
ми
діаметром 20 нм φ = 98%, тоді як на
этилцелюлозній мембрані з такими ж
порами φ = 45%. Така відмінність в
селективності мембран з різних матеріалів
пояснюється неоднаковою сорбцією на
них поліетиленіміна, що приводить до
зменшення ефективного розміру пор
різною мірою. Для виділення металів
методом комплексоутворення з подальшою
ультрафільтрацією можна рекомендувати
плоскі ацетатцелюлозні і поліамідні
мембрани УАМ і УПМ, а також поліамідні
мембрани УПА у вигляді порожнистих
волокон.
Для розрахунку селективності мембрани, узявши за основу модель «хелатных вузлів» металполімерного комплексу, запишемо реакцію взаємодії іона металу М з сукупністю n функціональних груп полімеру Ln (Ln відображає значення координаційного числа n) з утворенням комплексу MLn:
![]() (1.1)
(1.1)
Стійкість комплексу MLn характеризується константою Кк:
![]() (1.2)
(1.2)
де СМ, СL і СmLn — концентрації відповідно іонів металу, вільного комплексоутворювача (у перерахунку на мономірну ланку) і полімерного комплексу.
Одночасно з реакцією (1.1) для полімерних лігандів типу поліетиленіміна спостерігається побічна реакція протонування функціональних груп, причому протоновані групи виключаються з рівноваги комплексоутворення:
![]() (1.3)
(1.3)
Константа протонування Кn:
![]() (1.4)
(1.4)
де СН+
і СLН+
— концентрації
відповідно іонів водню, тобто 10-рН,
і протонованої форми
ліганда.
Загальна концентрація металу в розчині СМo рівна сумі концентрацій вільного і зв'язаного в комплексі металу:
![]() (1.5)
(1.5)
а загальна концентрація ліганда СLo рівна сумі концентрацій вільної, протонованої і зв'язаної в комплексі форм:
![]() (1.6)
(1.6)
Підставивши рівняння (1.2), (1.4) і (1.5) в рівняння (1.6), отримаємо:
![]() (1.7)
(1.7)
Якщо в комплексоутворенні бере участь m різних металів, які утворюють з полілігандом комплекси з константами стійкості ККі і координаційними числами ni, то рівняння (5.7) видозмінюється:
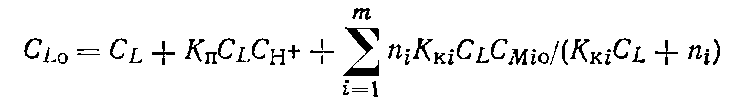
(1.8)
У рівнянні (1.8) тільки одне невідоме — концентрація вільного ліганда СL оскільки початкові концентрації ліганда, всіх металів, рН розчину, а також характеристики комплексів— константи стійкості і координаційні числа — зазвичай відомі. Рівняння (1.8) можна вирішити відносно СLi будь-яким ітераційним методом.
Якщо загальна концентрація
металу в початковому розчині рівна СМiо
то його брутто-концентрація в пермеаті
С2,
визначувана аналітично, рівна сумі
концентрацій незв'язаного металу і
металу, що пройшов у вигляді комплексу
зважаючи на його неповне затрим ання
мембраною. Знаючи з експерименту по
ультрафільтрації селективність мембрани
по полімерному ліганду
запишемо вираз для концентрації металу
в пермеаті С2:
ання
мембраною. Знаючи з експерименту по
ультрафільтрації селективність мембрани
по полімерному ліганду
запишемо вираз для концентрації металу
в пермеаті С2:
![]() (1.9)
(1.9)
Тоді з урахуванням рівнянь (1.2), (1.4) — (1.6) селективність мембрани по 1-у металу рівна:
![]() (1.10)
(1.10)
З рівняння (1.10) видно, що селективність мембрани по 1-у металу тим вище, чим більше константи стійкості його комплексу з полілігандом і вище ступінь затримання поліліганда.
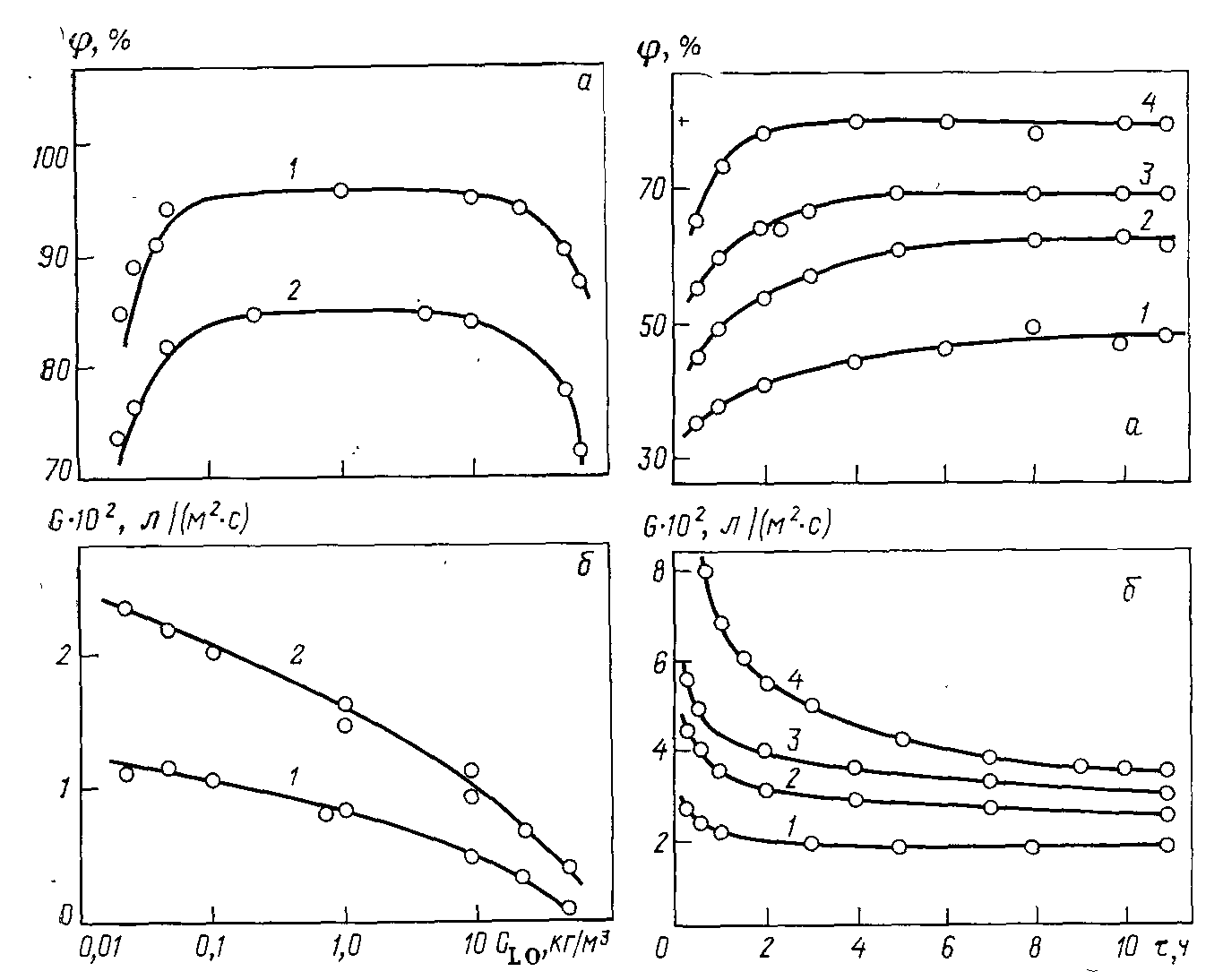
Рисунок 1.1 – Вплив початкової концентрації поліліганда СLo на селективність (а) і питому продуктивність (б) мембран УАМ-200(1) і УАМ-500(2):
крапки — експериментальні дані; рН 8,1; СNi2+ =10-2 кг/м3.
Рисунок 1.2 – Зміна селективності (а) і питомої продуктивності (б) мембрани в часі φ при різних швидкостях потоку W (м/с):
1 – 0,05; 2 – 0,19; 3 – 0,55; 4 – 1,88; мембрана поліамідна, середній діаметр пор 100 нм; Др=0,15 МПа; CПЭИ: СNi2+ = 10; рН 8,0.
Для першої і другої ділянки
кривих (залежності φL
від СLo
на рис. 1.1) отриманий хороший збіг
розрахованих таким чином значень
селективності з експериментальними
даними. Це означа є,
що запропоновані рівняння адекватно
описують реальні физико-хімічні процеси,
що відбуваються на стадії ультрафільтрації.
є,
що запропоновані рівняння адекватно
описують реальні физико-хімічні процеси,
що відбуваються на стадії ультрафільтрації.
На ефективність концентрації метал-полімерного комплексу ультрафільтрацією визначальний вплив роблять концентрація комплексоутворюючого полімеру і рН розчину, що розділяється, робочий тиск і швидкість розчину, що розділяється, в міжмембранному каналі апарату.
Вплив концентрації комплексоутворювача на селективність і питому продуктивність мембрани при постійній початковій концентрації металу СМo показаний на рис. 1.1. З рисунка видно, що із зростанням CLo питома продуктивність мембрани знижується. На кривих залежності φ від CLo можна виділити три ділянки. На першій ділянці із збільшенням концентрації поліетиленіміна збільшується φ, що обумовлене підвищенням частки металу, зв'язаного в комплекс. Після того, як весь метал виявиться зв'язаним, подальше зростання CLo не приводить до підвищення φ, що відповідає другій ділянці кривої. На третій ділянці наголошується зменшення ступеня затримання мембраною металу, не дивлячись на концентрацію полімеру, що збільшується, в розчині. Це можна пояснити, по-перше, дією концентраційної поляризації — у поверхні мембрани накопичуються макромолекули, що приводять до утворення гелевидного шару, який погіршує затримуючі властивості мембрани. По-друге, як показали дослідження в’язкісних властивостей розчинів метал-полімерних комплексів, даній ділянці кривої відповідає значне підвищення так званої «енергії активації в'язкої течії» — від 11∙103 до 25∙103 кДж/моль. Це свідчить про посилення структуризації розчинів в результаті утворення змішаних аміно-водних водневих зв'язків. За таких умов вода, проходячи через напівпроникну мембрану, захоплює за собою макромолекули полімерного комплексу, що також призводить до зниження φ.
Зміна концентрації хлоридів
лужних і лужноземельних металів від 0
до 100 г/л не робить помітного впливу на
φ і G, тоді як пониження рН
приводить до значного падіння φ із-за
протонування поліетиленіміна
і пов'язаного з цим зменшення його
здібності до комплексоутворення. Так,
при початкових концентраціях нікелю
10 мг/л і поліетиленіміна 100 мг/л
ацетатцелюлозна мембрана АМ-200 при рН
9,0 затримує 98% металу, при рН 5,1—40% і при
рН 3,0 — менше 8%. Отже, найефективніше
ультрафільтрацію використовувати для
виділення металів з розчинів, що мають
нейтральну або лужну реакцію, причому
ці розчини можуть містити великі
кількості домішок солей лужних і
лужноземельних металів.
комплексоутворення. Так,
при початкових концентраціях нікелю
10 мг/л і поліетиленіміна 100 мг/л
ацетатцелюлозна мембрана АМ-200 при рН
9,0 затримує 98% металу, при рН 5,1—40% і при
рН 3,0 — менше 8%. Отже, найефективніше
ультрафільтрацію використовувати для
виділення металів з розчинів, що мають
нейтральну або лужну реакцію, причому
ці розчини можуть містити великі
кількості домішок солей лужних і
лужноземельних металів.
З підвищенням робочого тиску φ мембрани знижується, причому тим помітніше, чим більше діаметр пор. Наприклад, при Р = 0,05 МПа φ мембрани по комплексу нікель — поліетиленімін рівна 90%, а при Р = 0,35 МПа φ = 81 %. Зниження φ з підвищенням Р можна пояснити посиленням деформації макромолекул в порах мембрани. Із збільшенням швидкості потоку знижується концентраційна поляризація, унаслідок чого зростає як φ, так і G процесу (рис. 1.2).
Приведені теоретичні залежності для розрахунку процесу виділення іонів металів методом комплексоутворення з ультрафільтрацією підтверджені експериментами по виділенню кольорових і важких металів з реальних розчинів. Показано, що цей метод може бути використаний при отриманні цінної мінеральної сировини з вод морів і океанів, а також дозволить комплексно вирішувати питання очищення і утилізації стічних вод [1].
