- •ФАЗОВЫЕ
- •Процессы, заключающиеся в превращении одной фазы данного вещества в другую фазу того же
- •Фаза - однородная часть гетерогенной системы, которая имеет границу раздела и может быть
- •Правило фаз Гиббса
- •Примеры применения правила фаз Гиббса
- •Плавление, кристаллизация
- •Виды измерителей
- •Кривые нагревания и охлаждения
- •Совмещенный ДТА и ЦТА методы
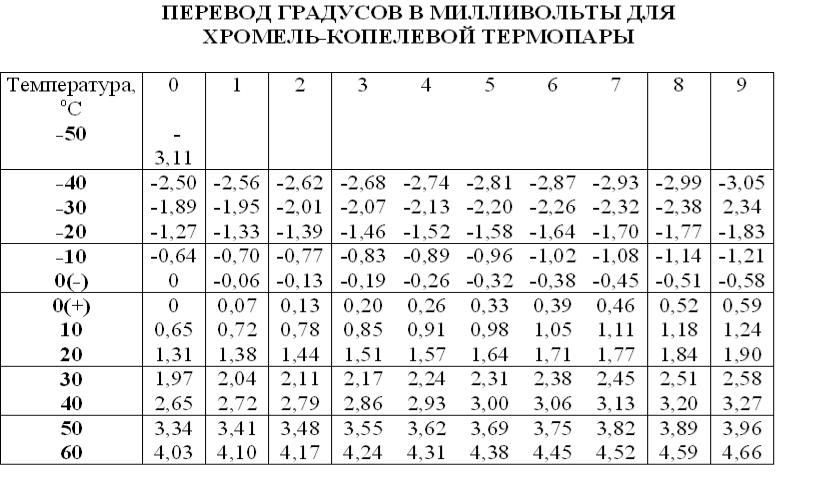
- •Термопары: хромель-алюмелевая,хромель-копелевая, медь-константан, платина-платинородий
- •Фазовые превращения в твердом состоянии
- •Кривая нагрева железа
ФАЗОВЫЕ
ПРЕВРАЩЕНИЯ
Процессы, заключающиеся в превращении одной фазы данного вещества в другую фазу того же вещества и, следовательно, протекающие без химических реакций, называются фазовыми превращениями.
Фазовые превращения протекают при постоянной температуре, с выделением или поглощением тепла и с изменением объема.
Фаза - однородная часть гетерогенной системы, которая имеет границу раздела и может быть отделена от общей системы механическим путем.
Гомогенной называется однородная система, каждой точке которой в условиях равновесия соответствуют одинаковые значения давления р, температуры Т и концентрации с (чистые вещества, твердые и жидкие растворы).
Гетерогенными называют сложные системы, состоящие из ряда однородных или гомогенных систем (вода-лед, суспензии, эмульсии, сплавы с нерастворимостью компонентов).
Правило фаз Гиббса
Компонентом называют независимую часть физической системы, имеющую свою химическую формулу. Компоненты образуют всю систему.
Закономерности всех изменений системы в зависимости от внутренних и внешних условий подчиняются правилу фаз Гиббса:
i = К – Ф + В,
где i - число степеней термодинамической свободы, К - число компонентов, Ф - число фаз,
В - внешние переменные факторы - (температура, давление, электромагнитные поля и пр.).
Если i = 0, система называется нонвариантной, если i = 1, то моновариантной, если i = 2 – бивариантной и т.д. При
i 0 система существовать не может.
Примеры применения правила фаз Гиббса
1.Имеется однокомпонентная система (чистый металл) (К=1), находящаяся в одной фазе (жидкой или твердой) (Ф=1). Число внешних факторов В=1 (изменяется только температура, p=Const). Тогда
i = 1 – 1 + 1 = 1.
2.Условие К=1, Ф=2, B=l (p=Const) соответствует однокомпонентной системе находящейся, например, в жидко-твердом состоянии: i = 1 – 2 + 1
=0.
3.Имеем систему лед-вода-пар К=1, Ф=3. При переменных р и Т (В=2). В этом случае i = 0.
4.Условие К=2, Ф=2, B=l (p=Const) относится, например, к двухкомпонентному сплаву, находящемуся в жидко-твердой фазе. В этом случае i = 2 – 2 + 1 = 1.
Плавление, кристаллизация
Отрицательные температуры: Т 0 С (водород, кислород, азот) Легкоплавкие (0-500 С)
(вода, висмут, олово, индий, свинец) Средние (600-1200 С)
(сурьма, алюминий, серебро, золото) Высокие (1400-2000 С)
(железо, кремний, титан, платина, ванадий) Тугоплавкие (2000-4000 С)
(вольфрам, молибден, бор)

Виды измерителей
Термопара, термометр, биметаллический термометр, пирометр
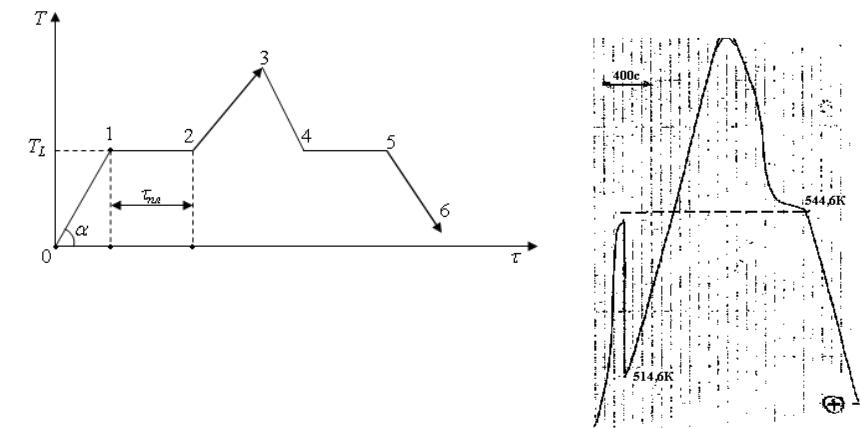
Кривые нагревания и охлаждения
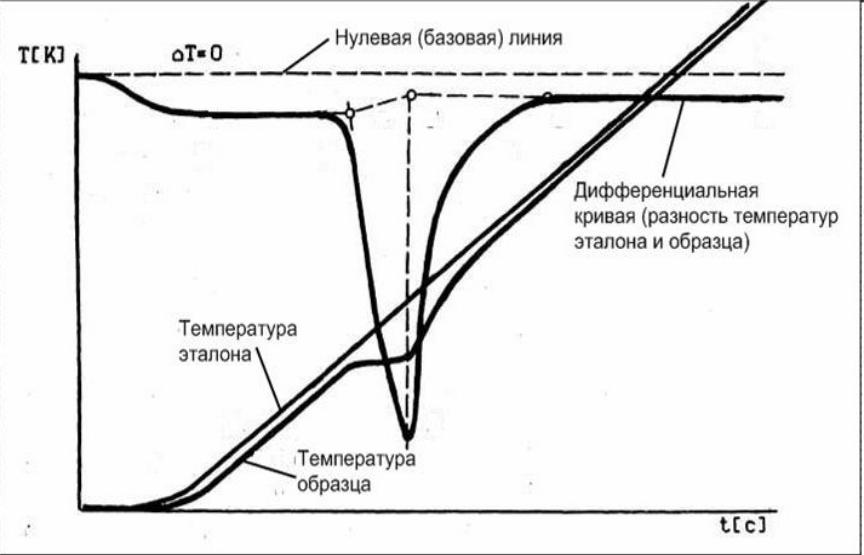
Совмещенный ДТА и ЦТА методы