
- •5.В чем суть закона Кольрауша.
- •13.Схема низкочастотного безэлектродного кондуктометра.
- •14.Описание схемы низкочастотного безэлектродного кондуктометра.
- •15. Высокочастотная кондуктометрия.
- •16. Индуктивная ячейка, принцип действия
- •17. Конденсаторная ячейка. Принцип действия (схема)
- •18. Оптические приборы. Колориметры
- •19. Колориметры. Закон Бугера - Ламберта – Бера
- •20. Оптическая плотность. Фотоколориметры
- •26. Действие рефрактометра
- •27- 28 РН метрия
- •29.Колориметрический и потенциометрический методы при измерении
- •30.Электрометрический способ измерения рН – растворов.
- •31. Схема датчика рН – метра с каломельным и стеклянным электродами.
- •32. В чем суть измерения рН – метром с каломельным и стеклянным электродами?
- •33.Описание электрической цепи pH-метра каломельным и стеклянными электродами.Сумарное эдс
- •34. Измерение плотности жидкости. Понятия. Определения.
- •35. Весовой плотномер. Схема.
- •36. Описание схемы и работы весового плотномера.
- •57. Термохимические газоанализаторы
- •58. Принципиальная схема газоанализатора. Принцип работы.
- •59 – 60. Термокондуктометрические газоанализаторы
- •69. Зачем нужентермокомпенсатор у кондуктометров? Электродная ячейка.
- •70. В чем отличия низкочастотной кондуктометрии от высокочастотной.
- •71. Сравните ячейки кондуктометров конденсаторного и индуктивного типа.
- •72. В чем суть колориметрического метода определения концентрации.
- •81. Влагосодержание. Влажность. Принцип работы емкостного влагомера
- •82. Если жидкость протекает по сечению трубопровода, каким равенством она определяется. Единицы измерения вязкости жидкостей.
- •83.Ультразвуковой вискозиметр. Принцип действия. Единицы измерения вязкости.
- •84.Ультразвуковой вискозиметр. Принцип действия.
- •89. Методы, которые используются в газоанализаторах для определения газов в смесях
- •93. Типы преобразователей. Дифференциально-трансформаторный преобразователь сигнала.
2. Основная цель контроля качества – гарантировать, что продукция (услуга, процесс) соответствуют конкретным требованиям и являются надежными, удовлетворительными и устойчивыми в финансовом отношении.
По сути, контроль качества предполагает проверку продукта, услуги или процесса для определения соответствия определенному минимальному уровню качества. Цель работы сотрудников, занятых контролем качества, - идентифицировать продукцию (услуги), которые не отвечают установленным стандартам качества компании. В случае выявления проблем, функции подразделения или специалиста по контролю качества могут включать временную остановку производства. В зависимости от конкретной услуги, продукции, а также типа установленной проблемы, производство товаров или оказание услуг может полностью не прекращаться.
Контроль состава материала
Данный вид контроля проводится с целью установления соответствия качественного и количественного химического состава металлопродукции нормам, заявленным в сертификате.
Норма отбора проб для контроля химического состава устанавливается в ТИ и составляет, как правило:
для листов и плит — от одного контрольного листа, плиты партии;
для лент, полос, проволоки — от одного контрольного рулона партии;
для прутков и профилей, имеющих поштучное клеймение завода-поставщика — от одного прутка, профиля, партии;
для прутков и профилей, имеющих маркировку на бирке — от 2-х, 3-х и 5-ти прутков, профилей для партий в количестве менее 30 шт., от 30 до 50 шт. и свыше 50 штук соответственно.
Отобранные пробы направляются в ЦЗЛ, где проводится контроль химического состава с использованием химических и/или спектральных методов анализа.
Необходимо отметить, что химиический анализ трудоемок, не является универсальным и не обладает высокой чувствительностью (особенно при малых концентрациях определяемых элементов).
Спектральный анализ — физический метод качественного и количественного определения состава вещества по его спектрам.
Спектральный анализ металлов проводят по ГОСТам, а именно:
сталей — ГОСТ 18895–81;
титановых сплавов — ГОСТ 23902–79;
алюминиевых сплавов — ГОСТ 7727–75;
магниевых сплавов — ГОСТ 7728–79;
меди — ГОСТ 9717.1–82, ГОСТ 9717.2–82, ГОСТ 9717.2–83;
медно-цинковых сплавов — ГОСТ 9716.0–79, ГОСТ 9716.1–79, ГОСТ 9716.2–79, ГОСТ 9716.3–79;
безоловянных бронз — ГОСТ 20068.0–79, ГОСТ 20068.1–79, ГОСТ 20068.2–79, ГОСТ 20068.3–79.
Рентгеноспектральный анализ. По сравнению с оптическими спектрами рентгеновские характеристические спектры содержат меньшее число линий, что упрощает их расшифровку. Это преимущество обусловливает все более широкое применение рентгеновского анализа в заводских лабораториях.
(флуоресцентный метод).
Флуоресцентный метод более предпочтителен т. к.:
имеет более высокую чувствительность (до 0,0005 %);
более оперативен и технологичен (нет необходимости делать трубку разборной и откачивать ее для поддержания вакуума);
проба не подвергается нагреву.
3. Концентрация вещества– отношение числа частиц компонента системы (смеси, раствора, сплава), его количества или массы к объёму системы. Величину концентрации волокна в воде обычно определяют по гидравлическим свойствам массных потоков. Существуют два метода косвенного измерения концентрации.По первому методу величину концентрации волокна в массе определяют по величине гидродинамического напора Н при истечении массы через местные сопротивления, обычно через изогнутую трубу определенного диаметра или через открытый наклонный лоток. При этом скорость истечения необходимо поддерживать постоянной.Приборы, основанные на принципе измерения концентрации по внутреннему трению, состоят из разного рода насадок, погружаемых и массу и вращающихся в ней с помощью двигателя. Реактивный момент, вызываемый торможением насадки массой, зависит от ее концентрации.
Измерение состава и свойств веществаПри анализе свойств и состава веществ в целлюлозно-бумажном производстве производят измерения:концентрации одной жидкости (или газа) в смеси других жидкостей или газов; концентрации ионов водорода в растворах (или расплавах) (рН – метры, оксредметры) и других;концентрации твердых частиц, пузырьков газа, капель жидкости (тумана) в жидкости или газе (концентратомеры механических смесей и др.);количества влаги в газе, жидкости или твердом теле (влагомеры);плотности массы определенных объемов или площадей веществ и материалов (плотномеры, массомеры, измерители массы 1м2бумажного полотна или картона);фракционного состава древесных волокон;качественных и количественных характеристик бумаги и картона;качественных показателей бумаги и картона (механические характеристики: вес 1м2, белизна, просвет, воздухопроницаемость, зольность, электроизоляционные свойства и др.).
Электрохимические измерителиЭлектрохимические измерители концентрации делятся на:кондуктометрические концентратомеры, основанные на измерении электрической проводимости или сопротивления электролитических ячеек;рН-метры - основанные на измерении электродных потенциалов;полярографические концентратомеры, в которых осуществляется снятие кривых поляризации или определение интенсивности прохождения света.Ионизационный принцип анализа основан на измерении ионного тока в исследуемой среде. Указанный метод позволяет измерить абсолютную концентрацию и состав газовых смесей. К группе ионизационных измерителей концентрации относятся широко распространенные масс-спектрометры, позволяющие разделить и идентифицировать положительные ионы анализируемого вещества по их массе.Ионизационные измерители
Спектрометрические измерителиПринцип анализа спектрометрических измерителей основан на избирательной способности различных веществ поглощать, излучать, отражать, рассеивать или преломлять различного рода излучения. Поэтому принципы построения измерительных средств очень широки, от звукового - 103Гц до гамма-излучения - 1018Гц. Отсюда и следует такое разнообразие измерительных приборов. Спектрометрические измерители имеют следующую классификацию:электроакустические, в которых используется зависимость скорости распространения звука от состава и концентрации исследуемой среды;ультразвуковые, основанные на различии затухания или скорости распространения ультразвуковых колебаний от состава, свойств жидкостей и газов;радиоспектрометрические, в которых используется принцип ядерного магнитного резонанса (ЯМР), электронного парамагнитного резонанса (ЭПР) и микроволновая спектроскопия. В последних используется взаимодействие сверхвысокочастотного электромагнитного поля с электрическим дипольным моментом молекул газа. Зависимость поглощения или отражения сверхвысокочастотных (СВЧ) колебаний от состава и свойств веществ, которые применяют для измерения толщины полотна, влажности и т.д.;
4. Кондуктометрический метод анализа основан на измерении электропроводности анализируемого раствора. Электропроводностью называют величину, обратную электрическому сопротивлению R. Единицей измерения электропроводности является Ом-1 или сименс (См). Растворы электролитов, являясь проводниками II рода, подчиняются закону Ома. По аналогии с сопротивлением проводников I рода, сопротивление раствора прямо пропорционально расстоянию между электродами l и обратно пропорционально площади их поверхности S
R = r (l / S),
где r - удельное сопротивление (Ом . см). При l = 1 см и S = 1 см2 имеем R=r, следовательно, удельное сопротивление равно сопротивлению 1 см3 раствора, находящегося между двумя параллельными пластинами площадью 1 см2, отстоящими друг от друга на 1 см.
Величину, обратную удельному сопротивлению, называют удельной электропроводностью c=1/r. Удельная электропроводность (См . см-1) численно равна току (в амперах) , проходящему через слой раствора с поперечным сечением, равным единице, под действием градиента потенциала 1 В на единицу длины.
Электропроводность разбавленных растворов электролитов зависит от числа ионов в растворе (т.е. от концентрации), числа элементарных зарядов, переносимых каждым ионом (т. е. от заряда иона), и от скорости движения одинаково заряженных ионов к катоду или аноду под действием электрического поля. С учетом всех этих факторов электропроводящие свойства ионов характеризуют эквивалентной ионной электрической проводимостью (подвижностью).
Эквивалентной электрической проводимостью называют проводимость раствора, содержащего 1 моль эквивалента вещества и находящегося между двумя параллельными электродами, расстояние между которыми 1 см. Ее единицей измерения является См . см2 . моль-1.
Удельная и эквивалентная проводимость связаны соотношением:
l = 1000 c / с,
где с – молярная концентрация эквивалента, моль-экв/л.
Методы прямой кондуктометрии основываются на том, что в области разбавленных и умеренно концентрированных растворов электрическая проводимость растет с увеличением концентрации электролита.
Закон Кольрауша (или закон аддитивности электропроводности при бесконечном разбавлении электролитов) гласит, что в бесконечно разбавленном растворе перенос электричества осуществляется всеми ионами независимо друг от друга; при этом общая молярная электропроводность раствора равна сумме молярных электропроводностей отдельных ионов. Закон был экспериментально установлен в 1879 году В. Кольраушем, позже получил объяснение исходя из теории электролитической диссоциации. При увеличении концентрации растворов увеличивается взаимодействие между ионами и закон Кольрауша не выполняется.
5.В чем суть закона Кольрауша.
КОЛЬРАУША
ЗАКОН:
в бесконечно разбавленном растворе
электролитаперенос электричества осуществляется
всемиионаминезависимо друг от друга. Вследствие
этого общая молярная электрич. проводимость
такого раствора L° равна сумме электрич.
проводимостей l°i
отдельных ионов, а разность молярных
электрич. проводимостей двух растворов
солейс общимкатиономне зависит от природы этого катиона,
например![]() .
При увеличенииконцентрациираствора вследствие взаимод. ионов их
движение уже не является независимым
икольрауша
закон
не выполняется.Практич. использование
кольрауша
закон
состоит в нахождении L° растворов слабых
электролитов. Для этого привлекают
данные о проводимости разб. растворов
сильных электролитов, которые полностью
диссоциируютна те же ионы, что и изучаемый
слабый электролит. Напр., для нахождения
L°СH3COOH
параллельно измеряют молярные электрич.
проводимости растворов НС1 и CH3COONa
и числа переноса ti
ионов Н+
и
СН3СОО-
при разл. концентрациях с; полученные
зависимости
.
При увеличенииконцентрациираствора вследствие взаимод. ионов их
движение уже не является независимым
икольрауша
закон
не выполняется.Практич. использование
кольрауша
закон
состоит в нахождении L° растворов слабых
электролитов. Для этого привлекают
данные о проводимости разб. растворов
сильных электролитов, которые полностью
диссоциируютна те же ионы, что и изучаемый
слабый электролит. Напр., для нахождения
L°СH3COOH
параллельно измеряют молярные электрич.
проводимости растворов НС1 и CH3COONa
и числа переноса ti
ионов Н+
и
СН3СОО-
при разл. концентрациях с; полученные
зависимости
![]() и
и![]() экстраполируют
кс=0.
Согласно кольрауша
закон,
экстраполируют
кс=0.
Согласно кольрауша
закон,
![]() и
и![]() =
=![]() .
Независимость l°-
при заданной температуре от природы
катиона соли служит эксперим. подтверждением
кольрауша
законЗакон
установлен экспериментально Ф. Кольраушем
в 1879.
.
Независимость l°-
при заданной температуре от природы
катиона соли служит эксперим. подтверждением
кольрауша
законЗакон
установлен экспериментально Ф. Кольраушем
в 1879.
6.Электродные кондуктометры.Схема.

7.Схема электродного кондуктометра.
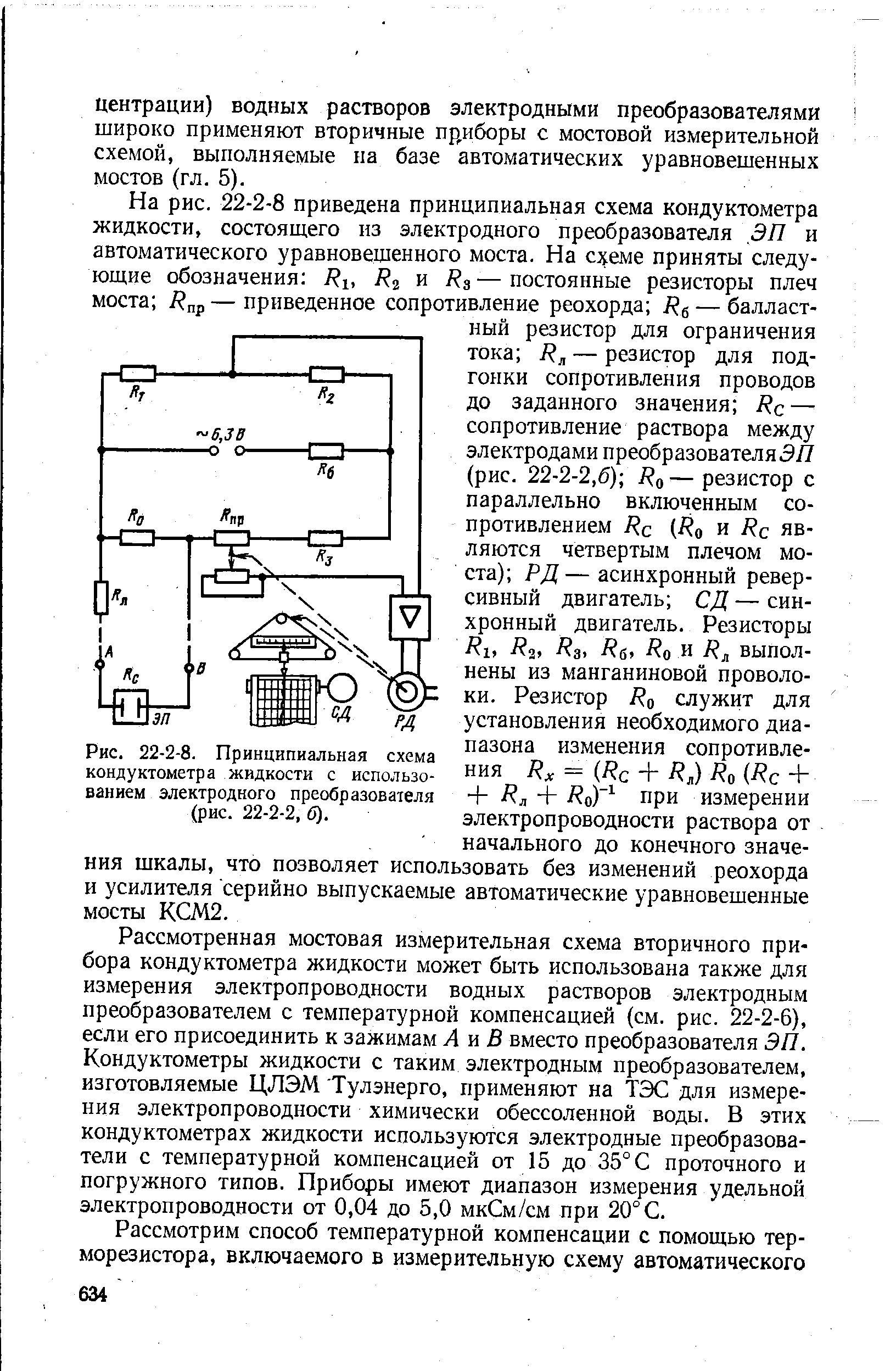
8.Схема кондуктометра с термокомпенсатором

9.

10.
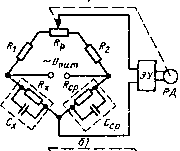
В автоматических контактных кондуктомерах применяются различные способы компенсации температуры. На рис представлена схема с жидкостной температурной компенсацией. В этой схеме температурный компенсатор представляет собой электродную ячейку с сопротивлением Rp и емкостью Сср, которые аналогичны параметрам и основной электродной ячейки При этом дополнительную электродную ячейку с параметрами R и С называют сравнительной, а основную электродную ячейку с параметрами и - измерительной. Сравнительную ячейку заполняют эталонной жидкостью, имеющей коэффициент, равный температурному коэффициенту контролируемой жидкости, и помещают в датчик с измерительной ячейкой Rj и Cj. Благодаря равенству температурных коэффициентов эталонной и контролируемой жидкостей, а также равенству их температур изменение сопротивления измерительной ячейки oi колебаний температуры компенсируется изменением сопротивления сравнительно R ячейки.
11. По принципу действия кондуктометрические концентратомеры подразделяются на электродные и безэлектродные.
Безэлектродные методы измерения концентрации растворов в значительной мере свободны от ошибок, присущих электродным методам (поляризация электродов, изменение величины их проводящей поверхности вследствие налипания твердых частиц или коррозии и др.). В связи с этим наиболее перспективной является безэлектродная кондуктометрия, которая в зависимости от частоты применяемого электрического тока делится на низкочастотную с использованием переменного тока промышленной и звуковой частоты обычно до нескольких килогерц и высокочастотную с использованием радиочастот до сотен мегагерц.
Принципы, положенные в основу безэлектродной кондуктометрии, были известны еще в 30-х годах, однако их практическое применение началось по существу только в последнем десятилетии.
Среди методов низкочастотной безэлектродной кондуктометрии наибольшее распространение получил трансформаторный метод, в котором трубка с анализируемым раствором является одной из обмоток трансформатора. Ввиду трудности осуществления температурной компенсации этот метод ранее не давал достаточной точности измерения. За последние годы разработан ряд схем температурной компенсации, что дает возможность широкого внедрения данного метода в измерительную технику.
Низкочастотные безэлектродные кондуктометры могут быть использованы для измерения концентрации как слабых, так и сильных электролитов, если их удельная электропроводность находится в пределах 10~6— 1 сим/см.
Высокочастотные кондуктометрические концентратомеры делятся на емкостные и индуктивные.
Высокочастотные кондуктометры с емкостными датчиками с наибольшей эффективностью используются для контроля растворов с низкой удельной электропроводностью, лежащей в пределах 10~5—10"1 сим/см.
Некоторые изменения конструкции и параметров датчиков емкостных высокочастотных концентратомеров позволяют несколько расширить пределы их измерения в сторону больших удельных электропроводностей.
12. Низкочастотная бесконтактная кондуктометрия реализуется на частоте до 1000 Гц и используется для измерения сильных электролитов и слабых, если их удельная электрическая проводимость находится в пределах 1-10-6 См/см.
Среди методов низкочастотной безэлектродной кондуктометрии наибольшее распространение получил трансформаторный метод, в котором трубка с анализируемым раствором является одной из обмоток трансформатора. Ввиду трудности осуществления температурной компенсации этот метод ранее не давал достаточной точности измерения. За последние годы разработан ряд схем температурной компенсации, что дает возможность широкого внедрения данного метода в измерительную технику.
