
Клиническая аллергология_учебное пособие_2007
.pdf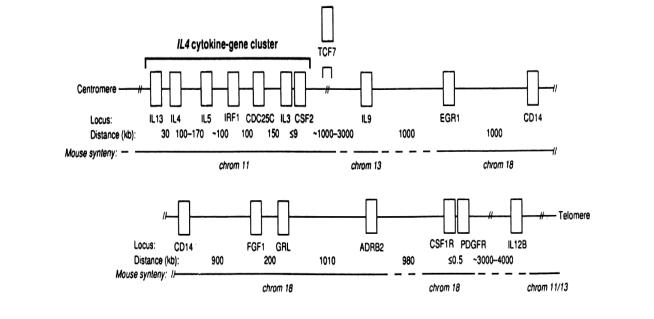
соседстве с геном IL-4 расположены гены факторов, регулирующих поликлональные IgE-ответы. Они включают гены IL-3, IL-4, IL-5, IL-9, IL-13, ГМКСФ, а также фактора транскрипции IRF1, продукт которого регулирует IFN- . Мало того, здесь же располагаются гены, кодирующие 2-адренорецепторы и рецепторы кортизола (рисунок 7).
Рисунок 7. У человека гены, кодирующие важные патогенетические факторы атопии сосредоточены в узкой области (регион 5q31–33) пятой хромосомы. По контрасту у мыши те же самые гены рассредоточены на трех различных хромосомах (11, 13 и 18).
Учитывая важную роль IL-4 в дифференцировке Th2-клеток и переключении синтеза антител с класса IgM на IgG4 и IgE, можно сделать предположение, что функциональный полиморфизм гена IL-4 или областей, регулирующих его синтез, отражается на уровне сывороточного IgE.
Факторы, увеличивающие риск развития аллергии
Контакт с большим количеством разнообразных аллергенов.
Отсутствие или небольшое количество контактов с инфекционными агентами.
Неблагоприятные факторы внешней среды, в том числе пассивное курение в первые месяцы жизни.
Ранняя персистирующая сенсибилизация. Кормление новорожденных смесями на основе коровьего молока в первые дни жизни в два раза увеличивает риск развития пищевой аллергией к концу первого года жизни.
Механизмы развития аллергических реакций
Предпосылкой активации тучной клетки или базофила является их
21
сенсибилизация – связывание специфического IgE с рецептором Fc RI.
Рецептор Fc RI был идентифицирован в 1970 г. вскоре после открытия IgE. Наиболее высоко Fc RI экспрессируется на тучных клетках и базофилах, в меньших количествах обнаруживается на дендритных клетках и моноцитах. Имеются сообщения о наличии Fc RI на эозинофилах. IgE обладает способностью стимулировать дополнительную экспрессию Fc RI на поверхности тучных клеток и базофилов. Всего тучная клетка или базофил могут экспрессировать на своей мембране более чем 100000 Fc RI.
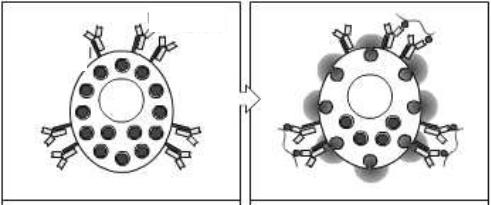
Базофил или тучная клетка могут быть сенсибилизированы одновременно IgE-антителами различной специфичности и поэтому могут реагировать на одновременное воздействие многих различных аллергенов. Активация этих клеток происходит при связывании аллергеном двух рядом расположенных молекул IgE («попарное сшивание», «перекрестное сшивание»). Показано, что необходимо «сшивание» нескольких сотен пар молекул IgE аллергенами, чтобы вызвать дегрануляцию тучной клетки или базофила (рисунок 8).
IgE
Fc R1
Рисунок 8. Сенсибилизация и дегрануляция тучной клети
Активация эффекторных клеток является началом скоординированной последовательности биохимических и морфологических событий, которые завершаются:
экзоцитозом секреторных гранул, содержащих заранее сформированные медиаторы: гистамин, гепарин, триптазу и др. (см. приложение 1).
синтезом и секрецией вновь сформированных медиаторов: простагландинов, лейкотриенов, PAF (см. приложение 1 и 2), цитокинов (IL-4, IL-5, IL-6, IL-13, TNF), аденозина.
Выброс этих мощных, биологически активных медиаторов представляет собой первичный эффекторный механизм в ответе IgE-зависимого типа. Под действием цитокинов и медиаторов происходит увеличение числа резидентных тучных клеток и усиление экспрессии на них FcεRI.
В зависимости от кратности контактов с аллергеном IgE-ассоциированный
22
иммунный ответ может проявляться в трех основных формах:
острые реакции, которые развиваются в пределах секунд или минут после воздействия аллергена;
отсроченные реакции, которые развиваются через часы после воздействия аллергена, когда многие из эффектов острой реакции исчезли или, по крайней мере, уменьшились;
хроническое аллергическое воспаление, которое может упорно сохраняться в течение многих дней и лет.
Острые аллергические реакции
Реакция Праустница–Кюстнера представляет одну из самых простых экспериментальных моделей острой аллергической реакции. В этой модели внутрикожное введение аллергена приводит к дегрануляции тучных клеток, которые были ранее сенсибилизированы путем внутрикожного введения сыворотки, содержащей IgE против этого аллергена. Медиаторы тучных клеток вызывают появление на коже специфических высыпаний. Острые местные аллергические реакции в дыхательном трактате, например, в слизистой бронхов, подвергшейся воздействию аллергена, также связаны с массивной, но ограниченной по площади, активацией специализированных эффекторных клеток. Это подтверждается при иммуногистохимическом исследовании – в воспаленной слизистой в месте введения аллергена обнаруживаются медиаторы тучных клеток.
В ходе дегрануляции происходит выброс гистамина, триптазы и гепарина. Параллельно эти клетки начинают секретировать:
анафилактические факторы хемотаксиса эозинофилов и нейтрофилов,
фактор активации тромбоцитов (PAF), IL-4, IL-5, IL-6, IL-13, TNF и др.,
лейкотриены, простагландины, тромбоксан,
серотонин, кинины, нейропептиды,
протеазы, свободные радикалы кислорода.
Под действием медиаторов:
увеличивается кровоток вследствие расширения артериол;
происходит увеличение сосудистой проницаемости, приводящее к выходу из посткапиллярных венул воды и плазменных белков (в том числе фибриногена), вследствие чего развивается отек ткани и депонирование фибрина. Потеря внутрисосудистой жидкости вызывает внутрисосудистый стаз эритроцитов.
появляется зуд из-за возбуждения рецепторов кожных сенсорных нервов;
развивается спазм гладкой мускулатуры;
наблюдается повышенное образование слизи;
развивается дегрануляция окружающих тучных клеток, реакция приобретает лавинообразный характер.
Подробный список медиаторов и описание их эффектов приведены в приложении 1. Как правило, такие реакции развиваются уже через нескольких
23
минут после введения аллергена, достигают максимума через 30–60 минут (в зависимости от типа ткани) и затем быстро уменьшаются. После выраженных реакций небольшие отеки и/или уплотнение ткани за счет отложения фибрина могут обнаруживаться даже спустя 24 часа и более после контакта с аллергеном. Наиболее ярким примером острой аллергической реакции является анафилаксия.
Анафилаксия – эта выраженная, угрожающая жизни, генерализованная и системная реакция гиперчувствительности. Анафилаксия может быть как аллергической, так и неаллергической, но последняя, вероятно, встречается гораздо реже. Аллергическая анафилаксия развивается у сенсибилизированных индивидуумов в пределах минут после воздействия аллергена. Чаще эта реакция обусловлена эффектами медиаторов, освобождаемых за счет IgE-зависимой активации тучных клеток. Однако у людей Fc RI может экспрессироваться не только на мастоцитах и базофилах, но и на макрофагах, клетках Лангерганса, мигрирующих дендритных клетках и эозинофилах. Поэтому, проявления некоторых острых аллергических реакций у людей могут быть обусловлены участием и этих типов клеток.
Отсроченные аллергические реакции
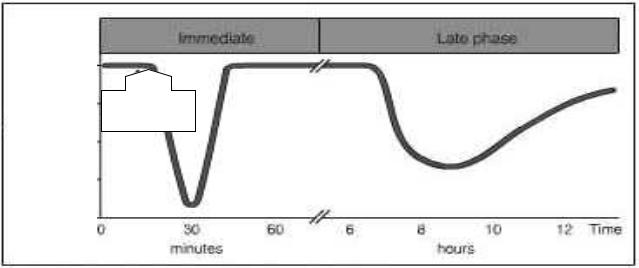
Первое описание отсроченной реакции дал Blackley в 1859. Он заметил, что признаки астмы могут повториться через несколько часов после ингаляции аллергена. В настоящее время известно, что большая доля пациентов с аллергической астмой (приблизительно 50% взрослых и более 70% детей) демонстрируют отсроченные реакции на аллергены (рисунок 9).
FEV1 л,/сек |
Острая реакция |
|
Отсроченная реакция |
|
|
|
|
400
300 Воздействие аллергена
200
100
0 |
30 |
60 |
6 |
8 |
10 |
12 |
|
минуты |
|
|
|
часы |
|
|
|
|
|
|
|
|
Рисунок 9. Типичный пример острого и отсроченного ответов, регистрируемых с помощью измерения объема форсированного выдоха (FEV). Обструкция появляется приблизительно через 10 минут после ингаляции аллергена, достигает максимума приблизительно через 30 минут и затем в период от 1 до 3 часов полностью или почти полностью исчезает. Вторая стадия
24
обструкции развивается в период от 6 до 12 часов и разрешается обычно в пределах суток.
Отсроченные реакции не удается промоделировать на животных – в этом причина трудностей, возникающих при попытках изучить гистохимические механизмы процесса. Поэтому многие вопросы патогенеза отсроченных реакций у людей остаются нерешенными. Тем не менее, косвенные данные свидетельствуют, что развитие отсроченных реакций зависит как от тучных клеток, так и от Th2лимфоцитов. При отсроченных аллергических ответах под влиянием цитокинов, продуцируемых активированными в ходе острой аллергической реакции тучными клетками и Th2-лимфоцитами, в зону аллергической реакции мигрируют другие лейкоциты – эозинофилы, базофилы и нейтрофилы. В том месте, где был отек, образуется клеточный инфильтрат. Естественно, клеточная ифильтрация сохраняется значительно дольше, чем отек. Кроме того, клетки инфильтрирата вызывают повреждение ткани при экзоцитозе содержимого своих гранул.
Отсроченные реакции характеризуются следующими общими чертами:
они могут возникать при любой локализации аллергического процесса;
отсроченной реакции всегда предшествует острая аллергическая реакция;
такие признаки, как гиперемия и отек кожи, заложенность носа, сужение дыхательных путей, а также такие симптомы, как чихание на фоне обструкции носовых ходов, появление хрипов и кашля после развития бронхиальной обструкции при отсроченных реакциях связаны с проникновением лейкоцитов из циркуляции к месту реакции;
средства, подавляющие хемотаксис лейкоцитов (ГКС), могут уменьшать проявления отсроченных реакций.
Хроническое аллергическое воспаление
Хроническое аллергическое воспаление типично формируется в тканях, в которых аллергические реакции развивались многократно и в течение длительного периода. При аллергической астме, аллергическом рините и атопическом дерматите пациенты регулярно подвергаются воздействию аллергена (или аллергенов). Хотя у каждой из этих патологий есть определенные особенности, основные патогенетические механизмы практически не различаются. В клеточном пейзаже воспалительного инфильтрата типично представлены эозинофилы и T- лимфоциты (особенно Th2). В тканях, хронически подвергаемых воздействию аллергена, развиваются устойчивые структурные и функциональные изменения.
Очевидно, что механизмы, по которым развивается хроническое аллергическое воспаление, в целом весьма схожи с обсужденным выше патогенезом отсроченных реакций, но имеются определенные отличия.
Регулярное повторное введение аллергена приводит к повышению уровня IgE, который в свою очередь повышает способность тучных клеток и базофилов секретировать IL-4, IL-13 и другие цитокины. Повышенный уровень IL-4 и IL-13
25
направляет дифференцировку Th0 в направлении Th2, которые в свою очередь стимулируют дальнейшее производство IgE.
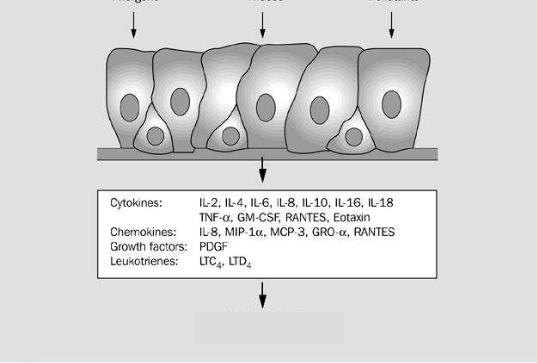
Постепенно в процессе повторяющихся актов поступления аллергена изменяется спектр клеток в тканях-мишенях. Наряду с эозинофилами здесь появляется много Т-лимфоцитов. В общем числе клеток, инфильтрирующих пораженную ткань, снижается доля нейтрофилов, но увеличивается количество В- лимфоцитов, моноцитов, резидентных макрофагов и базофилов. Перманентное поступление аллергена поддерживает клетки иммунной системы в стабильно активном состоянии, что проявляется активным производством цитокинов, хемокинов, медиаторов воспаления, которые в свою очередь воздействуют на эпителий и активно включают его в процесс синтеза биологически активных медиаторов (рисунок 10).
Воспаление
Рисунок 10. В очаге хронического аллергического воспаления эпителий является источником медиаторов.
Факторы воспаления нарушают местную иннервацию, микроциркуляцию, процессы репарации, стимулируют пролиферацию фибробластов, а все это приводит к развитию необратимых изменений в пораженной ткани. Снижение барьерных функций эпителия способствует повторным инвазиям аллергенов.
Лечение (например, ГКС) может только уменьшать проявления аллергического воспаления, связанные с проникновением эозинофилов и T- лимфоцитов, но не восстановят структурных и функциональных изменений.
26
Основные положения раздела
IgE-опосредованная гиперчувствительность характеризуется следующими основными чертами:
Этот ответ может быть вреден для хозяина, особенно когда он развивается на безвредные по существу аллергены. Следует однако отметить, что продукция IgE при паразитарных инвазиях служит проявлением противопаразитарного иммунитета.
Ответ развивается на некоторые антигены (аллергены), такие как компоненты паразитов, некоторые пищевые продукты, лекарства, пыльцу растений, белки животного происхождения, насекомых и т.д.
Длительная экспозиция
аллергена
Аллерген
Острая реакция |
Отсроченная реакция |
|
Клиника астмы |
|
|
|
|
|
|
|
|
|
Минуты |
|
Часы |
|
|
Дни |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
Медиаторы |
|
|
|
Медиаторы |
|
|
Медиаторы |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Моноцит Лимфоцит |
|
|
|
|
|
|
|
|
Эозинофил |
|
|
|
Эозинофил |
|
|
|
|
||
|
|
|
|
Нейтрофил |
|
|||
Дегрануляция тучной клетки |
|
|||||||
|
|
|
|
|
||||
|
|
|
|
|
|
|||
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Медиаторы Медиаторы
Тромбоциты
Макрофаг
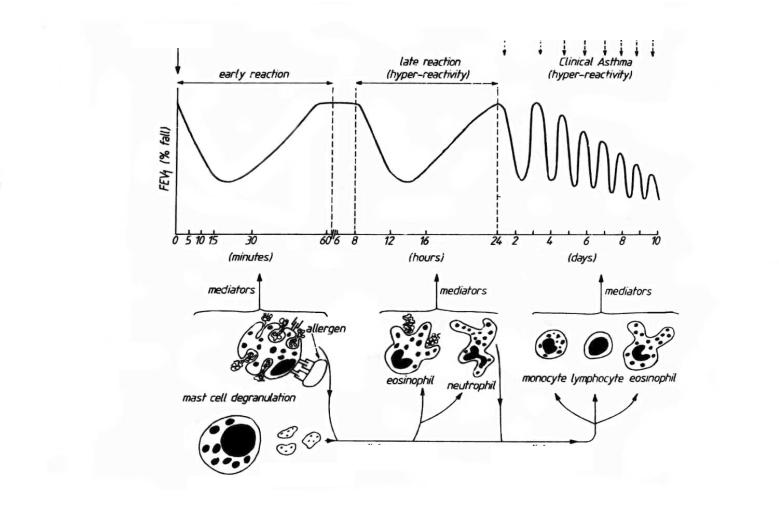
Рисунок 11. При острой аллергической реакции снижение FEV1 обусловлено главным образом дегрануляцией тучных клеток, при отсроченных реакциях – инфильтрацией эозинофилами и нейтрофилами, при хроническом аллергическом воспалении кроме эозинофилов в инфильтрате присутствуют лимфоциты и макрофаги.
27
В зависимости от обстоятельств ответы на введение аллергена могут протекать по типу острых и отсроченных реакций, а при длительной экспозиции – в виде хронического аллергического воспаления (рисунок 11).
Соотношение Th1/Th2 и ассоциированных с ними цитокинов определяют характер иммунного ответа.
Сенсибилизация FcεRI+-эффекторных клеток происходит путем их премирования IgE-антителами.
Взаимодействие аллергена с сенсибилизированной эффекторной клеткой может привести к развитию аллергической реакции.
Тканевые тучные клетки и в некоторых случаях базофилы крови, играют важную эффекторную роль в развитии острых реакций, а также вносят некоторый вклад в патогенез отсроченных реакций и хронического аллергического воспаления.
Острые реакции обусловлены действием медиаторов, высвобожденных из резидентных IgЕ-сенсибилизированных эффекторных клеток (особенно тучных клеток). В патогенез отсроченных реакций и хронического аллергического воспаления основной вклад вносят лейкоциты, мигрировавшие в ткани.
Острые реакции обычно не приводят к стабильным структурным изменениям в соединительной ткани, такие изменения, как правило, происходят на участках хронического аллергического воспаления.
28
Клиника и лечение аллергических заболеваний
Бронхиальная астма
Основные положения патогенеза, клиники, диагностики, лечения и профилактики бронхиальной астмы закреплены в международных и национальных соглашениях. Главным международным документом, на основе которого разработаны и скоординированы национальные программы, является
GINA (Global Initiative for Asthma, редакция 2002 г.) – «Глобальная стратегия по лечению и профилактике бронхиальной астмы». В Республике Беларусь 23.02.2006 г. Министерством здравоохранения РБ утвержден «Клинический протокол диагностики и лечения бронхиальной астмы».
Ключевые положения, определение
Бронхиальная астма (БА) – независимо от степени тяжести – является хроническим воспалительным заболеванием дыхательных путей.
Выработка избыточного количества антител IgE как реакция на воздействие аллергенов окружающей среды, является важнейшим идентифицируемым предрасполагающим фактором развития БА. Хроническое аллергическое воспаление дыхательных путей повышает их гиперреактивность и вызывает бронхиальную обструкцию и респираторные симптомы.
В результате воспалительного процесса возникает бронхиальная обструкция, обусловленная острым бронхоспазмом, отеком стенки бронха, хронической обтурацией слизью и ремоделированием стенки бронха.
Следует относиться к БА как к воспалительному заболеванию и при постановке диагноза, и при проведении профилактики и лечения.
Признание ключевой роли лежащего в основе БА воспалительного процесса привело к более полноценному определению БА.
Бронхиальная астма – это заболевание, в основе которого лежит хроническое аллергическое воспаление дыхательных путей. Хроническое воспаление усиливает бронхиальную гиперреактивность и может приводить к возникновению обратимой бронхиальной обструкции, обусловленной гиперсекрецией, спазмом гладкой мускулатуры, отеком и клеточной инфильтрацией слизистой бронхов и проявляющейся повторяющимся эпизодами свистящих хрипов, одышки, чувства стеснения в груди и кашля, особенно ночью или ранним утром.
Бронхиальная астма – одно из самых частых хронических заболеваний легких. В развитых странах частота этого заболевания составляет 10–20%. Среди
29
детей, больных бронхиальной астмой, мальчиков на 30% больше, чем девочек, причем у мальчиков заболевание протекает более тяжело. В подростковом возрасте и у взрослых заболевание чаще встречается у женщин.
Бронхиальная астма больше распространена среди городского населения с низким уровнем жизни, а также среди лиц, живущих в индустриальных районах и в странах с холодным климатом.
Существует наследственная предрасположенность к бронхиальной астме. Об этом свидетельствует повышенная заболеваемость бронхиальной астмой близких родственников больных.
Прогноз
Если бронхиальная астма начинается в раннем детском возрасте, то прогноз, как правило, благоприятный: к периоду полового созревания у 80% больных все проявления заболевания исчезают или становятся менее выраженными. Примерно у 20% из них после 45 лет возникает рецидив заболевания. Случаи выздоровления среди взрослых больных бронхиальной астмой отмечаются реже.
У детей бронхиальная астма течет тяжелее, если она сочетается с аллергическими заболеваниями верхних дыхательных путей или атопическим дерматитом. Прогноз особенно неблагоприятен у больных с аспириновой триадой, которая обычно наблюдается у взрослых, чаще у женщин.
Летальность бронхиальной астмы увеличивается с возрастом: у детей она составляет не более 1% (1–1,5:100000 в популяции), у взрослых 2–4%.
Факторы риска смерти можно условно разделить на 2 группы:
1.Объективные:
частые, длительные и плохо поддающиеся лечению приступы,
астматический статус в анамнезе,
низкая эффективность противовоспалительного лечения.
2.Субъективные:
бесконтрольное применение β-адреностимуляторов,
низкий уровень знаний больного о своем заболевании,
отсутствие взаимопонимания между больным и врачом,
низкий уровень жизни больного,
недоступность медицинской помощи.
Патогенез
Ведущую роль в патогенезе бронхиальной астмы играют два взаимосвязанных фактора: хроническое аллергическое воспаление и повышенная реактивность бронхов, которые приводят к периодической обратимой бронхиальной обструкции.
Периодическая обратимая бронхиальная обструкция сопровождается:повышением сопротивления дыхательных путей,
30
