
лекция Аналитикалык химия дістері
.docxАНАЛИТИКАЛЫҚ ХИМИЯҒА КІРІСПЕ.
АНАЛИЗ ӘДІСТЕРІНІҢ ЖІКТЕЛУІ
Негізгі әдебиеттер:
1. Құлажанов Қ.С. Аналитикалық химия, Алматы, «Білім», 1994
2. Шоқыбаев Ж. «Анорганикалық және аналитикалық химия». Алматы «Қайнар», 1992
Қосымша әдебиеттер:
1. Цитович И.К. Курс аналитической химии, М.: Высшая школа, 1977
2. Логинов Н.Я. Аналитичексая химия, М.: Просвещение, 1979
Дәріс жоспары:
1. Аналитикалық химия пәні, маңызы.
2. Аналитикалық химия анализ түрлері, әдістері
3. Сандық анализ кезінде жасалатын қателіктер
4. Аналитикалық химияның теориялық негіздері
Аналитикалық химия – бұл заттардың химиялық құрамын, материалдар құрамына кіретін молекулалардың құрылымдық және кеңістік құрылысын анықтайтын әдістер туралы ғылым.
Химиялық анализ ауыл шаруашылығында кеңінен қолданылады. Егіннен мол, сапалы өнім алу үшін топырақ құрамын, өсімдікке қажет болғанда тыңайтқыш салу керек. Бұл істерді дұрыс жүргізу үшін аналитикалық химияның әдістерін дұрыс қолданып анализ жасап қажет мөлшерлері анықталады. Сонымен қатар, мал шаруашылығынының өнімдерін арттыру үшін азық-түлік, судың, жайылымдардың сапасын химиялық анализ жасап, бақылап отырады. Химиялық анализ көмегімен мал өнімінің (сүт, ет, май т.б.) сапасын қадағалап отырады. Кәзіргі кезде ауыл шаруашылығындағы мамандар өздеріне күнделікті қажет клиникалық диагностика, зоогигиена, микробиология, фармакология, азық-түлік анализі және т.б. мәселелерімен тікелей араласқан кезде аналитикалық химия әдістерін білу қажет.
Аналитикалық химияның негізгі мақсаты – химиялық қосылыстардың сапалық және сандық құрамын анықтау, сондықтан оны екі үлкен бөлімге бөлуге болады: сапалық және сандық талдау.
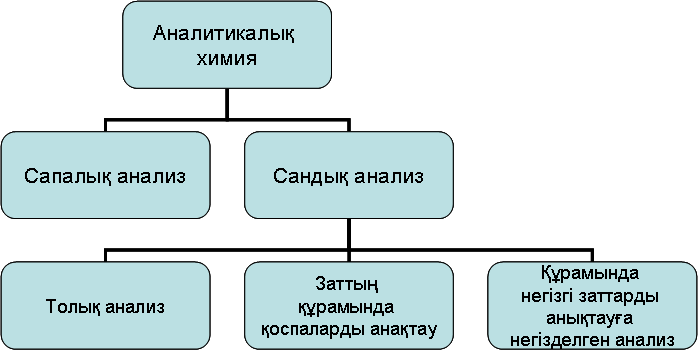
2. Сапалық талдау заттардың қандай элементтерден, иондардан, атом топтарынан немесе молекулалардан тұратынын анықтайды. Сандық талдау заттар құрамындағы элементтердің, иондардың сандық мөлшерін анықтайды.
Біріншіден сапалық, содан кейін сандық талдау жасалады, өйткені сандық анализ әдісін дұрыс таңдау зерттелетін заттардың құрамына тікелей байланысты.
Кәзіргі кезде аналитика көптеген әртүрлі әдістерді қолданады. Оларды барлығын 3 үлкен топқа бөледі:
1. химиялық
2. физикалық
3. физика-химиялық
2.1 Химиялық әдістер заттар арасында жүретін химиялық реакцияларға негізделген, олар көбінесе ерітінділерде (суда немесе қышқылда жиі ерітіледі), кейде құрғақ күйде жүреді және әр затқа тән тұнба түзілуі, немесе түсті қосылыс пайда болады немесе газ тәрізді заттарға әкеледі. Анализ мақсатында қолданылатын химиялық процестер аналитикалық реакциялар д.а.
Мысалы, калий ионын анықтау үшін мынадай реакция қолданылады:
NaCl + KSb(OH)6 = NaSb(OH)6 + RCl
калий гексагидроксиантимонаты (V)
Реакция нәтижесінде ақ тұнба түзіледі.
Химиялық анализ ыңғайлығы: оны кез-келген жерде жүргізуге болады, оған тек қолданылатын реактивтер және қарапайым зертханалық ыдыстар ғана қажет
Химиялық әдістерді 3 топқа бөледі:
1. Гравиметриялық (өлшемдік)талдау анықталатын заттың және реакция нәтижесінде түзілген заттын массасын дәлдікпен өлшеуге негізделген әдіс.
2. Титриметриялық (көлемдік) талдау реакцияға жұмсалған реактивтің көлемін анықтауға негізделген.
3. Газдық талдау.
2.2 Физикалық әдіс – элементтің, ионның тұрақты физикалық қасиеттеріне негізделген (түсі, спектрі, тығыздығы, т.б.)
1. Заттың сәулемен (излучение) әрекеттесуіне негізделген (радиоактивті, атомды-эмиссиялық, атомды-абсорбциялық)
2. Заттың электр және магнит қасиеттерін анықтауға негізделген (кондуктометриялық – электрөткізгіштігін анықтау, потенциометрия – электродтық потенциалдар арқылы ерітінді рН анықтау, масс-спектроскопиялық әдістер).
3. Заттың механикалық қасиеттерін анықтау (тығыздығы, дыбыс жылдамдығы, тұтқырлығы, қайнау температурасы т.б.)
2.3 Физика-химиялық талдау әдістері белгілі бір химиялық реакция барысында талданатын жүйедегі өзгерістердің: жарық сіңіру, жарықтың сынуы, электрөткізгіштік сияқты физикалық сипатын бақылауға негізделген. Бұл кезде алдымен химиялық реакция жүргізіліп анықталатын затқа тән айырықша қосылыс алынады. Содан соң оны физикалық әдіспен зерттейді. Бұл әдістер үшін арнайы құрал-жабдықтар қажет, сондықтан бұл әдістер тек лабораториялық жағдайда жасалынады.
Физика-химиялық талдау әдістерінің артықшылығы: 1) сұрыптамалығы – құрамдас бөліктері арасынан бір мезгілде тек керектісін сұрыптап, таңдап алу; 2) анализ жылдам жасалады; 3) физика-химиялық әдістерді автоматтандыру оңай.
3. Сандақ анализде есептеулерді және өлшеуді мұқият жүргізу керек. Химиялық анализ жасағанда есептеулер дәлдігі ГОСТпен немесе ТЖ /техникалық жағдайлар/ мен анықталады. Мысалы, концентрация есептегенде және гравиметриялық анализде аналитикалық таразыда заттың массасы төрт ондық белгілері бар санға дейін (0,1322 моль/л және 74,5744г) өлшейді. Титриметриялық анализде ерітіндінің көлемін бюреткамен өлшегенде екі ондық санға дейін (0,22мл).
Анализдің нәтижелері мен өлшемдеріне келесі талаптар қойылады: олар дұрыс, дәл және қайталанғыш болу керек.
Анализдің дұрыстығы орташа және ақиқат нәтижелерінің арасындағы айырмашылықпен сипатталанады. Өлшемдердің қайталанғыштығы әр түрлі жағдайларда жасаған өлшеулер нәтижелерінің бір біріне жуықтығын білдіреді, талдау қайталанымды, бірақ дұрыс емес бола алатынын ескерген жөн. Өлшемдердің дәлдігі анықтаулар нәтижелерінің өлшенетін шаманың ақиқат мәніне жуықтығын бейнелейді. Анализдің дәлдігі дұрыстық ұғымымен де сипатталанады. Дәлдік және қайталанғыштық ұғымдары бірін бірі толықтырады. Қайталанғыштық жоқ болғанда дәлдікке қол жеткізу мүмкін емес, бірақ жақсы қайталанғыштық та жоғары дәлдікті бере алмайды.

Абсолютті қателік – талдау нәтижесінің және өлшенетін шаманың ақиқат мәнімен айырмасына тең, яғни ол ақиқат мәнінен қаншалықты ауытқуын көрсетеді:
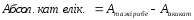
Салыстырмалы қателік – өлшеудің абсолютті қателігінің ақиқат мәнге қатынасы:

Талдау кезінде жасалатын қателіктерді өздерінің сипатына қарай келесідей жіктеуге болады:
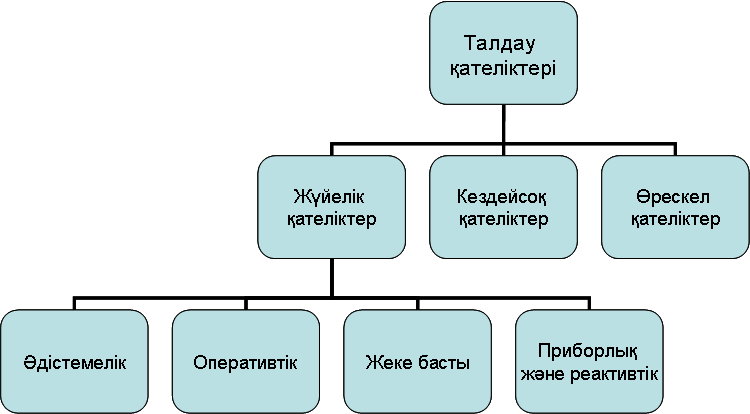
Жүйелік қателігі – өлшеудің әрдайым тұрақты болып қалатын немесе қайталанатын талдауларда заңдылық бойынша өзгеріп отырады. Олар тұрақты таңбаға ие болады, яғни анализ нәтижесін тек арттырып не кемітіп отырады. (өсетін не төмендейтін) қателіктер. Жүйелік қателіктерді түзетулерді енгізу, эталонмен (стандарт үлгісі) салыстыру сияқты тәсілдер арқылы азайтуға болады. Жүйелік қателіктердің келесі түрлері жие кездеседі:
а) Әдістемелік қателіктері қолданатын әдісінің ерекшелігіне тәуелді болады (реакцияның толық өтпеуі, тұнбаның жартылай еруі, индикатор қасиеттері).
б) Оперативтік қателіктері талдау барысында жасалатын опреациялардың дұрыс не толық орындалуына тәуелді болады (фильтрде тұнбаның жеткіліксіз шайлуы, құралдар мен реактивтердің қателіктері, таразының тегііс жерге дұрыс орнатпауы).
в) Жеке басты қателіктер лаборанттың бойындаға жеке физиологиялық, психикалық қасиеттеріне тәуелді болады (титрлеу кезінде ерітіндінің бояуының өзгеруін дұрыс анықтау қасиеті).
г) Приборлық немесе реактивтік қателіктері талдауда қолданатын құралдардың дәлдіктеріне және лабораттың қателіктеріне тәуелді болады.
Кездейсоқ қателіктері кез келген өлшеуде кездеседі, олардың санын параллельді өлшеулерді өткізу нәтижесінде азайтуға болады.
Өрескел қателіктері тәжірибені қайталаған сайын елеулі түрде өзгеріп отырады (тұнбаны шашып алу, ерітіндіні төгіп алу, өлшемдерді қате есептеу).
Стандарт үлгілер (эталондар) деп құрамындағы анықталатын элементтердің мөлшері жоғары дәрежелі дәлдікпен белгілі болатындай әр түрлі материалдар аталады. Стандарт үлгінің құрамы барлық немесе кейбір анықталатын компоненттер бойынша арнайы куәлікпен расталады. Стандарт үлгінің құрамы уақыт өткен сайын өзгермеу қажет.
4. Аналитикалық химияның теориялық негізін жаратылыстанудың іргелі заңдары құрайды: заттың массасын және энергиясының сақталу заңы, зат құрамының тұрақтылығы, әрекеттесуші массалар және эквиваленттер заңы және т.б.
Аналитикалық химия элементтердің, иондардың қасиеттеріне және бейорганикалық химияның теориялық мәселелеріне – массалардың әсер заңына, химиялық тепе-теңдік, электролиттік диссоциация теориясына, амфотерлік, тұз гидролизі, ТТР, комплексті қосылыстар теориясына және т.б. сүйнеді.
Гравиметриялық анализ әдістері
1. Гравиметриялық анализдің мақсаты, әдіс түрлері
2. Гравимтериялық анализдің тұндыру әдісі
Химиялық әдістер зерттелетін үлгі мен арнайы дайындалған реактивтің арасында жүретін реакцияларға негізделген. Жұмсалған реактивтің немесе реакция өнімдерінің мөлшеріне байланысты зерттелетің заттың құрамын есептейді. Химиялық әдістің гравиметриялық және титриметриялық анализ түрлері белгілі.
Гравиметриялық анализ анықталатын ионды не элементі химиялық реакция көмегімен ерімейтін тұнбаға түсіріп, оның нақты массасын дәл өлшеуге негізделген. Сонымен қоса, гравиметрияда анықталатын компоненті газ түрінде де шығарып анықтау мүмкін, бұл әдісті айдау деп атайды. Бұл жағдайда айдалған заттың массасын немесе қалдықтың массасын анықтайды.
Сонымен гравиметриялық анализдің әдістерін үш топқа бөледі:
1. Айдау әдісі анықталатын құрамдас бөлікті ұшқыс қосылыс түрінде толық бөліп алып, қалдықтың не тұтылған ұшқыш өнімінің дәл массасын өлшеуге негізделген. Айдау әдісінің бірнеше түрлері қолдану мүмкін:
анықталатын затты қоспадан айдап, түзілген заттың массасын өлшейді;
анықталатын затты айдап, оны белгілі бір сіңіргішке (сорбент, ерітінді және т.б.) сіңіреді де өлшейді, сіңіргіштің бастапқы массасымен салыстырғандағы массасының қосылуы бойынша айдалған заттын массасы анықталады;
анықталатын затты дәл өлшендіден айдап, айдау аяқталған соң оны қайтадан өлшейді де массаларының айырмасы бойынша айдалған заттың мөлшерін анықтайды.
2. Тұндыру әдісі анықталатын құрамдас бөлікті аз еритін белгілі химиялық құрамына сәйкес болатын қосылыс түрінде тұндырып, оны өндеп болған соң, оның мөлшерін анықтауға негізделген.
3. Бөлу әдісі зерттелетін заттан анықталатын құрамдас бөлікті бос күйінде бөліп алып, оның немесе қалдықтың массасын дәл өлшеуге негізделген.
Гравиметриялық анализде тұнбаны екі түрге бөледі:
тұнбаның тұндыру формасы – ерітіндіні лайықты реагентпен әрекеттестіргендегі ерітіндіде түсетін тұнба;
тұнбаның гравиметриялық формасы – ерітіндіден арнайы операциялармен бөлінген, өлшену түрінде алынған тұнба.
Сонымен бірге тұнбаның екі агрегаттық түрі белгілі – аморфты және кристалды тұнбалар.
Гравиметриялық анализдің барысында орындалатын операциялар тұндыру әдістің әдістемесін өткізіледі. Тұндыру әдісін келесі ретпен орындайды:
орташа татпаны іріктеу (алғашқы, лабораториялық және анализдік татпалар);
орташа татпадан өлшендіні өлшеу;
өлшендіні сәйкес еріткіште еріту;
арнайы реактивпен анықталатын компонентті тұнбаға толық тұндыру (тұндырушы реагенттің мөлшері есептелген мөлшерінен 1,5 есе артық алыну керек);
тұнбаны сүзіп алу (майда тұнбаны алдын ала центрифугалау), тұнбаны түріне қарай сүзуде үш түрлі фильтр қағаздары қолдану мүмкін: қара (қызыл) жолағы бар фильтрмен аморфты түнбаларды сүзеді, ақ жолағы бар фильтрмен кристалды тұнбаны, ал көк жолағы бар фильтрмен майда кристалды тұнбаларды сүзеді.
тұнбаны шаю, жуу;
тұнбаны кептіру және қатты қыздыру;
гравиметриялық түрдегі тұнбаны өлшеу;
анализ нәтижелерін есептеп шығару.
Орташа татпа дегеніміз химиялық құрылысы, физикалық және химиялық қасиеттері барлық алынатын топтамаларға сай келетін салыстырмалы түрде алынған материалдың немесе шикі заттың шағын мөлшері. Орташа татпаны алғашқы татпадан кварталау әдісі бойынша іріктеп алады.
Өлшенді дегеніміз нақты анализ жасауға қажетті зерттелетін заттың анализдік орташа татпасының шағын массасы (аморфты тұнбалар үшін m»0,1г дейін, ал ұсақ және ірі кристалды тұнбалар үшін m»0,3-0,5г дейін зат өлшенеді).
Гравиметриялық анализде кез келген тұнбаны қолдануға болмайды. Тұнбаның кейбір қасиеттеріне келесі талаптар қойылады:
тұнбаның ерігіштігіне – тұнба толық тұну үшін оның ерігіштік көбейтіндісінің (ЕК) мәні өте төмен болу қажет;
тұнбаның құрамына – тұнбаның құрамы тұрақты болып, яғни өзгермеу қажет;
тұнбаның құрылысына – тұнба оңай сүзіліп, қоспалардан жеңіл жуатындай болу қажет;
тұнбаның тұндыру формасы гравиметриялық формасына толық ауысу қажет.
Сонымен қоса гравиметриялық формадағы тұнбаға қосымша талаптар қойылады:
өлшенетін тұнбаның құрамы белгілі химиялық формулаға сәйкестігі;
гравиметриялық формадаға тұнба ауада химиялық тұрақты және температураға төзімді болу қажет;
өлшенетін тұнбаның құрамында анықталатын ионның немесе элементтің мөлшері аз, ал салыстырмалы молекулалық массасы үлкен болғаны жөн.
