
- •Как решать тесты по неорганической
- •Пример.
- •Пример.
- •Пример.
- •Пример.
- •Пример.
- •Реакции в растворах электролитов
- •Пример.
- •Пример.
- •Пример.
- •Пример.
- •Гидролиз, пр
- •Пример.
- •Пример.
- •Пример.
- •Пример.
- •Примеры.
- •Пример.
- •Примеры.
- •Пример.
- •Пример.
- •Пример.
- •Пример.
- •Основы электрохимии
- •Пример.
- •Пример.
- •Пример.
- •Пример.
- •Пример.
- •Комплексные соединения
- •Пример.
- •Пример.
- •Пример.
- •Пример.
- •Пример.
Пример.
1.Электродный процесс, уравнение которогоFe2++ 2e =Fe, протекает в гальваническом элементе, обозначаемом схемой ...
А)Mn│HI│Fe;Б)In│InCl3║FeCl3│Fe;В)Zn│ZnSO4║FeSO4│Fe; …
Решение.
А)Mn│HI│Fe; эта схема не содержит символ ║, значит, это неверный ответ.
Б)In│InCl3║FeCl3│Fe; эта схема соответствует вышеприведенному описанию, однако степень окисления металлаМ =Fe в соли MbAnc= FeCl3равна +3, а не +x= +2, данной в условии, значит, это неверный ответ.
В)Zn│ZnSO4║FeSO4│Fe; эта схема соответствует вышеприведенному описанию, степень окисления металлаМ =Fe в соли MbAnc= FeSO4равна +2, значит, это верный ответ.
1.Электродный процесс, уравнение которого 2H++ 2e=H2, протекает в гальваническом элементе, обозначаемом схемой ...
А)In│InCl3║FeCl3│Fe;Б) Mn│HI│Fe; ...
Решение.
Надо найти схему, правая часть которой имеет вид ... HyAn│... (An – кислотный остаток;y – индекс).
А)In│InCl3║FeCl3│Fe; правая часть этой схемы (║FeCl3│Fe) не соответствует вышеприведенному описанию, значит, это неверный ответ.
Б) Mn│HI│Fe; правая часть этой схемы (HI│Fe) соответствует вышеприведенному описанию, значит, это верный ответ.
1.Электродный процесс, уравнение которогоM–xe =Mx+, протекает в гальваническом элементе, обозначаемом схемой ...
Решение.
Надо найти схему, левая часть которой имеет вид M│... (М – металл).
Пример.
1.Электродный процесс, уравнение которогоCo– 2e=Co2+, протекает в гальваническом элементе, обозначаемом схемой ...
А) Cd│Cd(NO3)2║Co(NO3)2│Co; Б) Co│HBr│Cu; …
Решение.
А)Cd│Cd(NO3)2║Co(NO3)2│Co; в этой схеме слева (Cd│), а неCo│, значит, это неверный ответ.
Б)Co│HBr│Cu; в этой схеме слеваCo│, значит, это верный ответ.
2.В гальваническом элементе, обозначаемом схемойMа│HyAn│Mк, протекают электродные процессы, уравнения которых ... и
Решение.
Ма
– хае
= М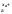 ,2Н+
+ 2е
= Н2.
,2Н+
+ 2е
= Н2.
Пример.
2.В гальваническом элементе, обозначаемом схемойMn│HI│Fe, протекают электродные процессы, уравнения которых ... и
Решение.
Mn– 2e=Mn2+,2Н+ + 2е = Н2.
2.В гальваническом элементе, обозначаемом схемойMа│сольMа║сольMк│Mк, протекают электродные процессы, уравнения которых ... и
Решение.
Ма
– хае
= М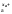 ,
М
,
М + хкe
= Мк
+ хкe
= Мк
Пример.
2.В гальваническом элементе, обозначаемом схемойIn│InCl3║CuCl2│Cu, протекают электродные процессы, уравнения которых ... и
Решение.
In – 3e = In3+, Cu2+ + 2e = Cu.
3. При электрохимической коррозии в нейтральной среде системы «... – ...» на катоде образуется частица, формула которой ...
Решение.
OH–.
3. При электрохимической коррозии в кислой среде системы «... – ...» на катоде образуется частица, формула которой ...
Решение.
H2.
3. При электрохимической коррозии в ... среде системы «M1 –M2» на аноде образуется частица, формула которой ...
Решение.
Надо найти в табл. 3 стандартные потенциалы
e и e
и e обоих
металлов (M1 иM2) и сравнить их
между собой. Еслиe
обоих
металлов (M1 иM2) и сравнить их
между собой. Еслиe < e
< e ,
то на аноде образуется частица, формула
которойM
,
то на аноде образуется частица, формула
которойM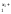 .
Еслиe
.
Еслиe > e
> e ,
то на аноде образуется частица, формула
которойM
,
то на аноде образуется частица, формула
которойM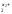 .
.
Пример.
3. При электрохимической коррозии в ... среде системы «Bi –In» на аноде образуется частица, формула которой ...
Решение.
Из табл. 3 видно, что e =
=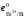 =
+0,214 В,e
=
+0,214 В,e =
=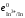 = –0,343 В. Т.к.e
= –0,343 В. Т.к.e = +0,214 >e
= +0,214 >e = –0,343, то на аноде образуется частица,
формула которойIn3+.
= –0,343, то на аноде образуется частица,
формула которойIn3+.
Таблица 3.
Стандартные потенциалы металлове0при 298 К
|
Mx+/M |
e0, В |
Mx+/M |
e0, В |
Mx+/M |
e0, В |
Mx+/M |
e0, В |
|
Ac3+/Ac |
–2,600 |
Со2+/Со |
–0,277 |
La3+/La |
–2,522 |
Rb+/Rb |
–2,925 |
|
Al3+/Аl |
–1,662 |
Сr2+/Cr |
–0,913 |
Li+/Li |
–3,045 |
Rh3+/Rh |
+0,800 |
|
Ag+/Аg |
+0,799 |
Сu2+/Cu |
+0,337 |
Mg2+/Mg |
–2,363 |
Ru2+/Ru |
+0,450 |
|
Аu3+/Au |
+1,498 |
Fе2+/Fе |
–0,440 |
Мn2+/Мn |
–1,180 |
Sb3+/Sb |
+0,240 |
|
Ва2+/Ва |
–2,906 |
Ga3+/Ga |
–0,560 |
Nа+/Nа |
–2,711 |
Sc3+/Sc |
–2,077 |
|
Ве2+/Ве |
–1,847 |
Н+/Н2 |
0,000 |
Ni2+/Ni |
–0,250 |
Sn2+/Sn |
–0,136 |
|
Вi3+/Bi |
+0,214 |
Нg2+/Hg |
+0,854 |
Рb2+/Pb |
–0,126 |
Sr2+/Sr |
–2,888 |
|
Cа2+/Са |
–2,864 |
In3+/In |
–0,343 |
Pd2+/Pd |
+0,915 |
Тl+/Тl |
–0,336 |
|
Cs+/Сs |
–2,923 |
Ir3+/Ir |
+1,000 |
Pt2+/Pt |
+0,963 |
Y3+/Y |
–2,372 |
|
Cd2+/Cd |
–0,403 |
K+/K |
–2,924 |
Rа2+/Rа |
–2,916 |
Zn2+/Zn |
–0,763 |
4.Формула металла, который может быть получен при электролизе водного раствора его соли с нертутными катодами – это ...
Решение.
Это металл, стандартный потенциал которого (см. табл. 3) е0> –1,6 В.
4.Формула металла, которыйнеможет быть получен при электролизе водного раствора его соли с нертутными катодами – это ...
Решение.
Это металл, стандартный потенциал которого (см. табл. 3) е0< –1,6 В.
5.При электролизе водного раствора соли на нертутных катодах и инертных анодах выделяютсятолькоH2 иAn2 (An=Br,Cl,I). Формула этой соли – ...
Решение.
Формула этой соли – MAnx, гдеM– металл, стандартный потенциал которого (см. табл. 3)е0< –1,6 В;An=Br,Cl,I.
5.При электролизе водного раствора соли на нертутных катодах и инертных анодах выделяются металл иAn2 (An=Br,Cl,I). Формула этой соли – ...
Решение.
Формула этой соли – MAnx, гдеM– металл, стандартный потенциал которого (см. табл. 3)е0> –1,6 В;An=Br,Cl,I.
5.При электролизе водного раствора соли на нертутных катодах и инертных анодах выделяютсятолькоH2 иS. Формула этой соли – ...
Решение.
Формула этой соли – MbSc, гдеM– металл, стандартный потенциал которого (см. табл. 3)е0< –1,6 В.
5.При электролизе водного раствора соли на нертутных катодах и инертных анодах выделяютсятолькоH2 иO2. Формула этой соли – ...
Решение.
Формула этой соли – MbAnc, гдеM– металл, стандартный потенциал которого (см. табл.3) е0 < –1,6 В; An = AsO4, CO3, ClO4, F, PO4, NO3, SO4, SeO4.
5.При электролизе водного раствора соли на нертутных катодах и инертных анодах выделяются металл и O2. Формула этой соли – ...
Решение.
Формула этой соли – MbAnc, гдеM– металл, стандартный потенциал которого (см. табл.3) е0 > –1,6 В; An = AsO4, CO3, ClO4, F, PO4, NO3, SO4, SeO4.
