
- •Глава 1 Химическая термодинамика.
- •1.1 Основные понятия и определения в термодинамике.
- •Термодинамические процессы.
- •Внутренняя энергия
- •Формы обмена энергией
- •1.2. Первый закон термодинамики.
- •Теплоемкость
- •Влияние температуры на теплоемкость
- •Термохимия
- •Энтальпии образования и сгорания
- •Закон Гесса и следствия из него
- •Зависимость теплового эффекта от температуры. Уравнение Кирхгофа.
- •Второй закон термодинамики Самопроизвольные и несамопроизвольные процессы.
- •Содержание и формулировки второго закона термодинамики. Энтропия как функция состояния системы.
- •Статистический характер второго закона термодинамики.
- •Некоторые закономерности в изменении энтропии веществ.
- •Изменение энтропии в химических реакциях.
- •Температурная зависимость стандартной энтропии реакции.
- •Изменение энергии Гиббса
- •Термодинамическая зависимость стандартной энергии Гиббса химической реакции - ∆rG0т
- •Направление процессов в открытых многокомпонентных системах. Химический потенциал.
- •Термодинамика химических равновесий
- •Уравнение изотермы химической реакции.
- •Зависимость константы равновесия от температуры. Уравнение изобары реакции.
- •Глава 2 Химическая кинетика.
- •2.1 Общие представления о скорости химических реакций.
- •2.2 Зависимость скорости реакции от концентрации. Закон действующих масс.
- •Скорость гетерогенных химических реакций.
- •2.3 Влияние температуры на скорость химических реакций.
- •2.4 Кинетическая классификация реакций
- •Кинетические уравнения реакций различных порядков
- •Кинетические представления о химическом равновесии.
- •Смещение химического равновесия.
- •2.5 Теоретические подходы к трактовке элементарного акта химической реакции.
- •Теория активных соударений (тас)
Зависимость теплового эффекта от температуры. Уравнение Кирхгофа.
Согласно закону Гесса можно вычислить тепловой эффект реакции при той температуре (обычно 298 К), при которой известны теплоты образования или сгорания всех реагентов. Часто бывает необходимо знать тепловой эффект реакции при различных температурах.
Запишем термодинамическое уравнение в виде:
v1А1 + v2А2= v3А3+v4А4; ΔrН0(т)
Обозначив энтальпию образования i –того компонента, отнесенную к 1 молю через Нi, энтальпию реакции представим в виде
ΔrН0(т)= (v3Н3+v4Н4) - (v1Н1+v2Н2)
Продифференцируем данное уравнение по температуре при постоянном давлении:
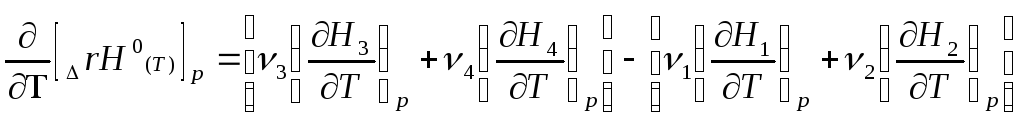 (1.37)
(1.37)
Как следует из уравнения (1.30), производная
![]() является
истинной теплоемкостьюi– того реагента. Из уравнения (1.37) получим
является
истинной теплоемкостьюi– того реагента. Из уравнения (1.37) получим
![]() [ΔrН0(т)]
[ΔrН0(т)]![]() (1.38)
(1.38)
или
![]() [ΔrН0(т)]
[ΔrН0(т)]![]() =ΔСр0(1.38а)
=ΔСр0(1.38а)
Частную производную от теплового эффекта по температуре можно заменить на полную:
![]() (ΔrН0(т))р=ΔСр0(1.39)
(ΔrН0(т))р=ΔСр0(1.39)
Или
d(ΔrН0(т)) =ΔСр0· dТ (1.40)
Выражения (1.39) и (1.40) называют уравнениями Кирхгофа в дифференциальном виде. Для практического применения интегрируют (1.40), используют неопределенный интеграл
ΔrН0(т)=ΔНI
+
![]() (1.41)
(1.41)
Где ΔНI - постоянная интегрирования или интегрируют в пределах от Т1до Т2.
В качестве нижнего предела интегрирования обычно выбирают Т1= 298 К, так какΔrН0298легко вычислить по следствиям из закона Гесса
ΔrН0(т![]() )=ΔrН0298+
)=ΔrН0298+
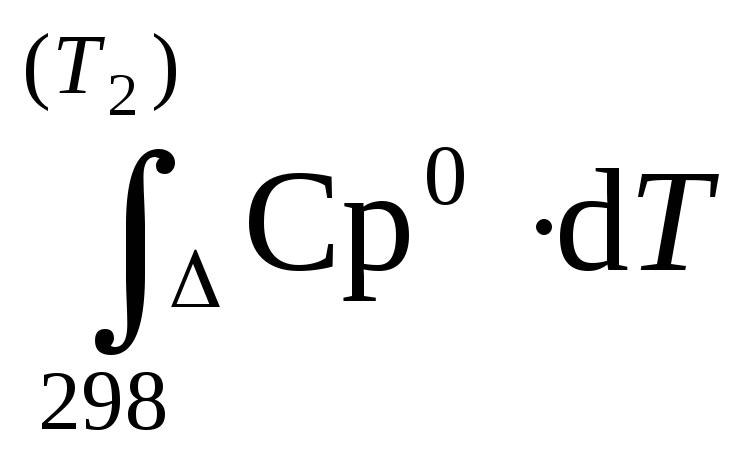 (1.42)
(1.42)
В практике используют обе интегральные формулы. Формулы Кирхгоффа применяют в трех приближениях. В первом наиболее грубом полагают ΔСр = 0, т.е. считают равными суммарные теплоемкости продуктов и исходных веществ.
Тогда ΔrН0(т![]() )=ΔrН0(т
)=ΔrН0(т![]() )= const, т.е. тепловой эффект считают
независящим от температуры. Во втором,
более точном приближении считают
разность теплоемкостей постоянной
величинойΔСр0 = const;
тогдаΔСр0 можно
вывести за знак интеграла и для уравнения
(1.42) получим следующую формулу второго
приближения.
)= const, т.е. тепловой эффект считают
независящим от температуры. Во втором,
более точном приближении считают
разность теплоемкостей постоянной
величинойΔСр0 = const;
тогдаΔСр0 можно
вывести за знак интеграла и для уравнения
(1.42) получим следующую формулу второго
приближения.
ΔrН0(т![]() )=ΔrН0298+ΔСр(Т2- 298)
)=ΔrН0298+ΔСр(Т2- 298)
В третьем, наиболее точном, приближении использования формулы Кирхгоффа учитывают зависимость ΔСрот температуры в виде степенного ряда Ср0= а + вТ. ЗависимостьΔСр0 =f(T) в общем виде записывается следующим образом:ΔСр0 =Δа +ΔвТ, гдеΔа = Σviai(продуктов реакции) - Σvjaj(исходных веществ)
Аналогично для Δв. При использовании формулы (1.42) при расчете в третьем приближении получим:
ΔrН0(т![]() )=ΔrН0298+
)=ΔrН0298+
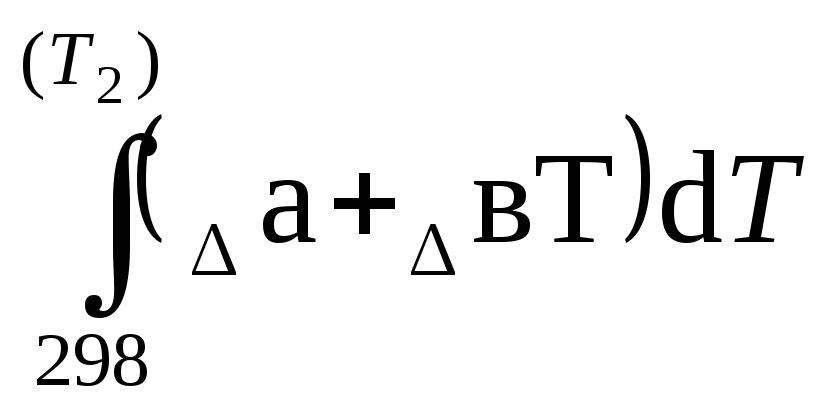
После интегрирования будем иметь:
ΔrН0(т![]() )=ΔrН0298+Δа (Т2- 298) +
)=ΔrН0298+Δа (Т2- 298) +![]() (Т22– 2982)
(Т22– 2982)
Рассмотрим примеры решения задач, основанных на первом и втором следствиях из закона Гесса.
Пример № 1.
Рассчитайте стандартную энтальпию (стандартный )тепловой эффект при постоянном давлении реакции
СН4(г) + 2О2(г) → СО2(г) + 2Н2О(ж)
Используя стандартные энтальпии образования исходных веществ и продуктов реакции.
Решение: По первому следствию из закона Гесса.
ΔгН0298=
![]() -
-![]() =
=
= -393,5 + 2(- 285,8) - (-74,9) - 0 = -890,2 кДж < 0
Пример № 2.
По термохимическому уравнению рассчитайте стандартную энтальпию образования исходного вещества
2КС1О3(кр)→ КС1(кр)+ 3О2(г); ΔгН0298 = -75,4 кДж.
Решение: По первому следствию из закона Гесса.
ΔгН0298= 2![]()
![]() ,
,
Следовательно,
![]() 0,5 (2
0,5 (2![]()
![]() ,)
= 0,5 [(2(-436,7) + 0 – (-75,4)] =
,)
= 0,5 [(2(-436,7) + 0 – (-75,4)] =
= 0,5 (-873,4 + 75,4) = -399 кДж/моль
Пример № 3.
Для реакции 2NO(г)+ О2(г)→ 2NO2(г)рассчитайте стандартные тепловые эффекты при постоянном давлении (Qр=ΔгН0298) и объеме (Qv=ΔгU0298)
Решение:
Стандартный тепловой эффект при постоянном давлении найдем по первому следствию из закона Гесса
Qр=ΔгН0298=
![]() –
–
![]() 2 * 34,2 – 2 * 91,3 - 0 = -114,2 кДж =
2 * 34,2 – 2 * 91,3 - 0 = -114,2 кДж =
= - 114200Дм
По уравнению ΔгН0298=ΔгU0298+ΔVгRT
Qv=ΔгU0298=ΔгН0298-ΔVгRT
Для данной реакции ΔVг = 2 – (2+1) = - 1 моль
Стандартный тепловой эффект при постоянном объеме
Qv=ΔгU0298= - 114200 – (-1) * 8,31 * 298 = - 111724 Дж = - 111,7 кДж
Пример № 4.
Стандартные энтальпии сгорания ацетилена С2Н2(г) и бензола С6Н6(г)соответственно равны – 1300 и – 3302 кДж /моль. Рассчитайте стандартную энтальпию реакции циклизации ацетилена.
3С2Н2(г)→ С6Н6(г)
Решение: По второму следствию из закона Гесса
ΔгН0298=
![]() =
3 (- 1300) – (- 3302) = - 598 кДж
=
3 (- 1300) – (- 3302) = - 598 кДж
