
- •Белки-2
- •Содержание лекции
- •Пути утилизации Аминокислот:
- •Кроме индивидуальных путей обмена, известен ряд превращений, общий почти для всех аминокислот. Это
- •Окислительное дезаминирование
- •Трансаминирование аминокислот
- •Первая стадия яв-ся ферментативной с образованием промежуточного продукта- иминокислоты, которая спонтанно, без участия
- •ГДГ- состоит из 6 субъединиц и
- •Все остальные аминокислоты могут окисляться и дезаминироваться только непрямым путем ( т.е. через
- •Это главный путь удаления азота у аминокислот. Выделены трансаминазы, катализирующие переаминирование большинства аминокислот.
- •Исключением являются аминокислоты с разветвленным углеводородным радикалом, для которых в печени нет соответствующих
- •Непрямое окислительное дезаминирование.
- •Любая а/к
- •Поскольку обе эти реакции – и трансаминирование, и прямое дезаминирование- обратимы, то
- •Т.о. можно сказать, что путь синтеза заменимых а/к в организме- это непрямое окислительное
- •Существует еще один механизм непрямого дезаминирования α- а/к, при которм ГЛУ, АСП, и
- •О2--- малат
- •ГДГ выполняет следующие функции:
- •Трансаминирование-это главный путь удаления азота у аминокислот. Выделены трансаминазы, катализирующие переаминирование большинства аминокислот.
- •Аланиновая трансаминаза АЛТ
- •Исключением являются аминокислоты с разветвленным углеводородным радикалом, для которых в печени нет соответствующих
- •Клиническое значение определения
- •В сыворотке крови здоровых людей активность этих трансаминаз в среднем составляет- 15-20 Е.,
- •Наибольшая активность АлАТ приходится на печень, а АсАТ на миокард. Поэтому определение активности
- •Определение активностиАсАТ используется для ранней диагностики ИМ. Причем увеличение активности наблюдается через 24-36
- •Токсичность аммиака и пути его обезвреживания
- •3.Аммиак изменяет соотношение ионов натрия и калия т.к. близок к ним по физико-
- •Пути обезвреживания аммиака
- •1.Восстановительное аминирование
- •2.Образование амидов дикарбоновых кислот
- •3. Основная масса ГЛН и АСН захватывается почками, где под действием глутаминазы от
- •4. Амидирование свободных карбоксильных групп белков (амидированные формы белков устойчивы к протеазам)
- •Биосинтез мочевины
- •Орнитиновый цикл синтеза мочевины (ОЦСМ) протекает в гепатоцитах,т.к. них наиболее высокая активность ферментов
- •Это еще один путь детоксикации аммиака- синтез пиримидиновых оснований. Первая и вторая р-ции
- •Энергетическая стоимость ЦСМ
- •2- когда синтез-ся карбомоилфосфат
- •Биологическая роль ЦСМ
- •Перипортальный гепатоцит
- •Врожденные дефекты ЦСМ
- •Заболевание
- •Гиперамонийеми
- •Регуляция ЦСМ
- •Пути вступления аминокислот в ЦТК
- •Но в экстремальных ситуациях (диабет, голод, алкогольная интоксикация) роль аминокислот резко возрастает. На
- •Дальше, после истощения запасов гликогена, происходит переключение метаболизма на утилизацию липидов (10- 15
- •После истощения запасов липидов наступает терминальная стадия- утилизация а/к--увеличение аммиака в крови---- увеличению
- •Реакции декарбоксилирования аминокислот лежат в основе образования биогенных аминов.
- •и психических заболеваний оказывают влияние на метаболизм указанных соединений. Активная форма витамина В6
- •Норадреналин - основной нейромедиатор симпатических постганглионарных окончаний. И норадреналин и его метилированное производное,
- •Обмен катехоламинов происходит при участии катехоламин-O- метилтрансферазы, (КOMT) и тираминазы, (MAO). Оба эти
- •Нарушения метаболизма дофамина служат причиной
- •Из триптофана через промежуточный 5- гидрокситриптофан образуется серотонин, соединение с широким спектром действием
- •Синтез серотонина, мелатонина
- •Серотонин присутствует в самых высоких концентрациях в тромбоцитах и в желудочно- кишечном тракте.
- •После высвобождения из серотонинергических нейронов, большая часть высвобождаемого серотонина возвращается
- •Мелатонин образуется из серотонина
- •Синтез и секреция мелатонина увеличиваются в течение темнового периода дня и поддерживаются в
- •Эти суточные колебания синтеза мелатонина регулируются с
- •Гистамин образуется путем декарбоксилирования гистидина.
- •Эту реакцию катализирует декарбоксилаза ароматических L- аминокислот. Этот фермент не обладает выраженной
- •Декарбоксилаза in vitro и in vivo ингибируется а- метиламинокислотами, применяемыми в клинике в
- •На первом этапе амин окисляется с передачей водородов на ФАД и образованием аммиака
- •Окислительное дезаминирование
- •Ингибиторы МАО находят применение при лечении гипертонической болезни, депрессивных состояний и т.д.
- •Подобно другим биогенным аминам, гистамин разрушается путем окислительного дезаминирования при помощи моноаминоксидаз- флавинзависимых
- •В головном мозге концентрация аминокислот почти в 8 раз выше, чем в
- •В тканях мозга интенсивно протекают метаболические превращения аминокислот,
- •g аминомасляная
- •Она локализована главным образом в нейронах центральной нервной системы, преимущественно в сером веществе
- •В особенности важной для нормального функционирования головного мозга является реакция декарбоксилирования, в результате
- •Биосинтез и деградацию глутамата можно рассматривать, как побочный путь цитратного цикла (ГАМК-
- •ГАМК-шунт характерен для клеток центральной нервной системы, но не играет существенной роли в
- •Декарбоксилирование L- глутамата - это основной
- •Катаболизм g-аминобутирата
- •ГАМК оказывает тормозящий эффект на деятельность ЦНС.
- •Глутамат, ГАМК, выполняют в
- •Эти аминокислоты образуются в реакции трансаминирования из промежуточных метаболитов цитратного цикла, 2-оксоглутарата и
- •Многие моноамины и катехоламины инактивируются аминоксидазой

Белки-2
Тканевой обмен аминокислот
лекция 18 доцент Свергун В.Т.

Содержание лекции
1.Основные реакции обмена аминокислот
-реакции по радикалу -реакции на карбоксильную группу -реакции на аминогруппу
2.Аммиак, пути его образования,токсичность
3.Пути детоксикации аммиака
4.Пути вступления аминокислот в ЦТК
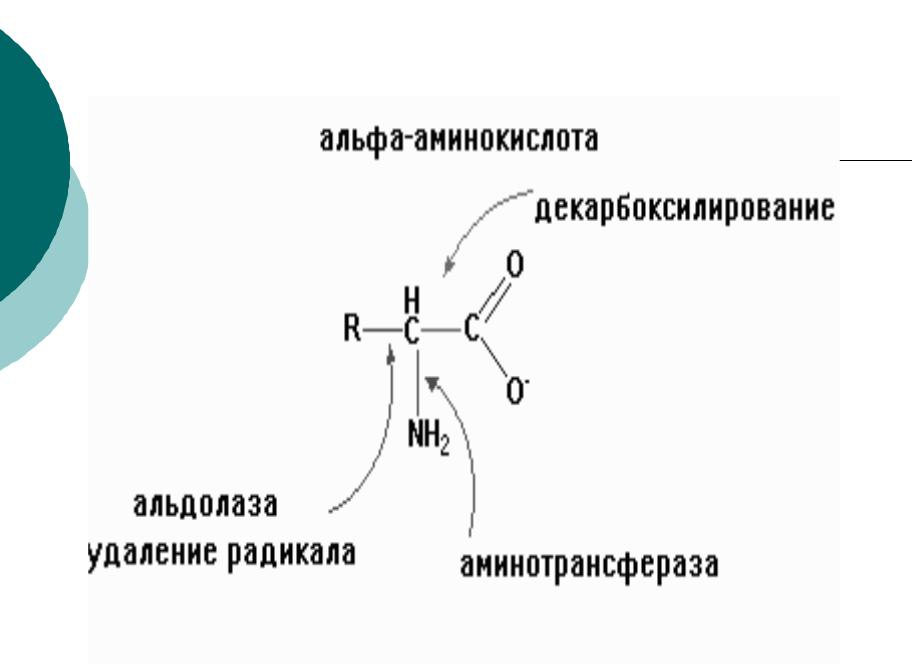

Пути утилизации Аминокислот:
статинов )
АК
энергообмена
1.Биосинтез белка
2.Синтез олигопептидов (либеринов,
3.Биогенных аминов 4.Мочевины
5.Креатина, креатинфосфата 6.Азотистые основанания
7.Аминоспирты
8.Никотинамид
9.Желчные кислоты 10.Реакции обезвреживания и

Кроме индивидуальных путей обмена, известен ряд превращений, общий почти для всех аминокислот. Это реакции:
1.по радикалу (R)- реакции гидроксилирования ( про----> o-про)
разрыва радикала( образование Vit PP и ТРП);
2.Реакции на --СООН группу- декарбоксилирование( образование биогенных аминов, ГИС гистамин)
3. Реакции на группу NH2- дезаминирование 4х типов:
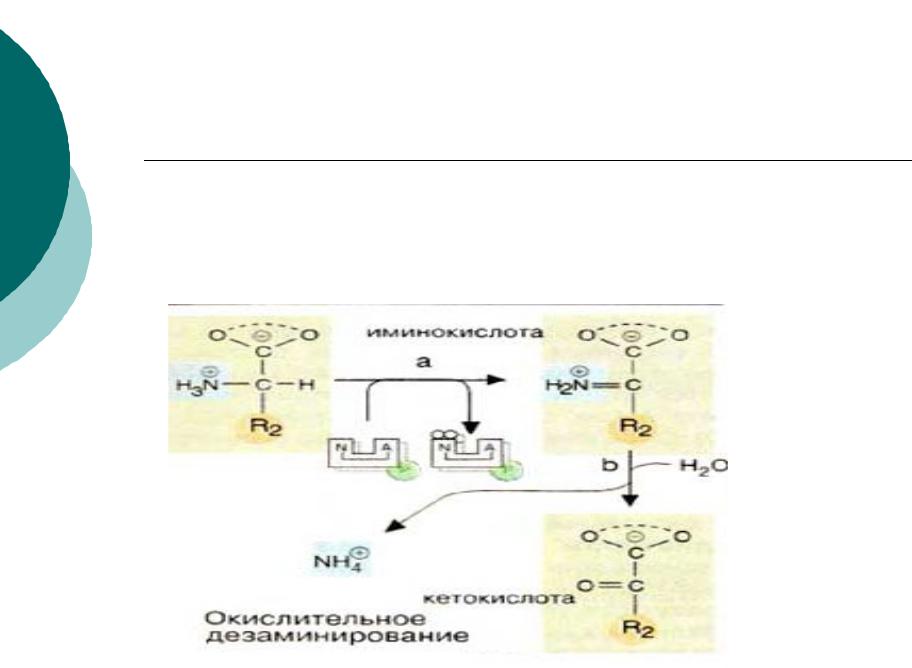
Окислительное дезаминирование
R-CH-COOH |
|
R-CH-COOH |
NH2 |
|
NH |
Флавин |
Флавин-Н2 |
H2O |
|
|
NH3 |
H2O2 |
O2 |
R |
Каталаза |
|
C=O |
|
|
|
|
|
COOH |
H2O + 1/2O2 |
|
|

|
Восстановительное дезаминирование |
|
|||||||||
R-CH-COOH |
+ |
2H |
|
|
R-CH 2-COOH |
+ |
NH 3 |
||||
|
|||||||||||
|
|
|
|||||||||
NH 2 |
|
|
|
|
|
|
|
|
|
||
|
Гидролитическое дезаминирование |
|
|||||||||
R-CH-COOH |
+ |
H2O |
|
|
R-CH-COOH |
+ |
NH 3 |
||||
|
|
||||||||||
|
|
|
|||||||||
|
|
|
|
|
|||||||
NH 2 |
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
OH |
|
|
||||
Внутримолекулярное дезаминирование
R-CH-COOH |
|
R-CH=CH-COOH + |
NH 3 |
|
|
NH 2 |
|
||
|
|
|
|
|
Трансаминирование аминокислот
окислительное дезаминирование- прямое

Первая стадия яв-ся ферментативной с образованием промежуточного продукта- иминокислоты, которая спонтанно, без участия фермента, распадается на аммиак и α- кетокислоту.
Этот тип реакций наиболее распространен в тканях

ГЛУ+NAD+--- иминоглут кислота + НОН-
--- α- кетоглутарат+NADH+H+ +
NH3
Первая стадия катализируется ГДГ (анаэробный фермент). Вторая стадия проходит спонтанно. Реакция- обратима!
