
- •Содержание
- •§ 2. Краткий исторический очерк возникновения и развития отечественной токсикологической химии
- •Глава I. Общие вопросы химико-токсикологического анализа
- •§ 1. Объекты химико-токсикологического анализа. Вещественные доказательсва
- •§ 2. Особенности химико-токсикологического анализа
- •§ 3. Осмотр объектов исследования и определение некоторых их свойств
- •§ 4. Предварительные пробы в химико-токсикологическом анализе
- •§ 5. План химико-токсикологического анализа
- •§ 6. Организация органов судебно-медицинской и судебно-химической экспертизы в ссср
- •§ 7. Эксперт-химик
- •§ 8. Правила судебно-химической экспертизы вещественных доказательств
- •§ 9. Акт судебно-химической экспертизы вещественных доказательств
- •§ 10. Некоторые вопросы терминологии в токсикологической химии
- •§ 11. Классификация ядовитых и сильнодействующих веществ в токсикологической химии
- •Глава II. Отравления и некоторые вопросы токсикокинетики ядов
- •§ 1. Отравления и их классификация
- •§ 2. Пути поступления ядов в организм
- •§ 3. Всасывание ядов в организме
- •§ 4. Распределение ядов в организме
- •§ 5. Связывание ядов в организме
- •§ 6. Выделение ядов из организма
- •§ 7. Факторы, влияющие на токсичность химических соединений
- •§ 8. Методы детоксикации
- •§ 9. Метаболизм чужеродных соединений
- •§ 10. Окисление чужеродных соединений
- •§ 11. Восстановление чужеродных соединений
- •§ 12. Гидролиз чужеродных соединений
- •§ 13. Дезалкилирование, дезаминирование и десульфирование чужеродных соединений
- •§ 14. Другие метаболические превращения
- •§ 15. Реакции конъюгации
- •§ 16. Посмертные изменения лекарственных веществ и ядов в трупах
- •§ 17. Разложение биологического материала после наступления смерти
- •§ 18. Изменение ядов при разложении трупов
- •Глава III. Методы анализа, применяемые в токсикологической химии
- •§ 1. Метод экстракции
- •§ 2. Микрокристаллоскопический анализ
- •§ 3. Метод микродиффузии
- •Глава IV. Ядовитые и сильнодействующие вещества, изолируемые из биологического материала перегонкой с водяным паром
- •§ 1. Аппараты для перегонки с водяным паром
- •§2. Влияние рН среды на перегонку химических соединений с водяным паром
- •§ 3. Перегонка ядовитых веществ с водяным паром из подкисленного биологического материала
- •§ 4. Перегонка ядовитых веществ с водяным паром из подкисленного, а затем из подщелоченного биологического материала
- •§ 5. Фракционная перегонка веществ, содержащихся в дистиллятах
- •§ 6. Синильная кислота
- •§ 7. Формальдегид
- •§ 8. Метиловый спирт
- •§ 9. Этиловый спирт
- •§ 10. Изоамиловый спирт
- •§ 11. Ацетон
- •§ 12. Фенол
- •§ 13. Крезолы
- •§ 14. Хлороформ
- •§ 15. Хлоралгидрат
- •§ 16. Четыреххлористый углерод
- •§ 17. Дихлорэтан
- •§ 18. Реакции, позволяющие отличить хлорпроизводные друг от друга
- •§ 19. Тетраэтилсвинец
- •§ 20. Уксусная кислота
- •§ 21. Этиленгликоль
- •Глава V. Ядовитые и сильнодействующие вещества, изолируемые из биологического материала подкисленным этиловым спиртом или подкисленной водой
- •§ 1. Развитие методов выделения алкалоидов и других азотистых оснований из биологического материала
- •§ 2. Влияние рН среды на изолирование алкалоидов и других азотистых оснований из биологического материала
- •§ 3. Влияние состава извлекающих жидкостей на изолирование алкалоидов и других азотистых основании из биологического материала
- •§ 4. Влияние подкисленной воды и подкисленного спирта на извлечение примесей, переходящих в вытяжки из биологического материала
- •§ 5. Очистка вытяжек из биологического материала от примесей
- •§ 6. Экстракция алкалоидов и других токсических веществ из вытяжек
- •§ 7. Обнаружение ядовитых веществ, изолируемых подкисленной водой или подкисленным этиловым спиртом
- •§ 8. Количественное определение токсических веществ, изолированных подкисленной водой или подкисленным спиртом
- •§ 9. Метод выделения токсических веществ, основанный на изолировании их этиловым спиртом подкисленным щавелевой кислотой
- •§ 10. Метод выделения токсических веществ, основанный на изолировании их водой, подкисленной щавелевой кислотой
- •§ 11. Метод выделения токсических веществ, основанный на изолировании их водой, подкисленной серной кислотой
- •§ 12. Барбитураты и методы их исследования
- •§ 13. Барбамил
- •§ 14. Барбитал
- •§ 15. Фенобарбитал
- •§ 16. Бутобарбитал
- •§ 17. Этаминал-натрий
- •8.Обнаружение этаминала-натрия по уф- и ик-спектрам.
- •§ 18. Бензонал
- •§ 19. Гексенал
- •§ 20. Производные ксантина
- •§ 21. Кофеин
- •§ 22. Теобромин
- •§ 23. Теофиллин
- •§ 24. Наркотин
- •§ 25. Меконовая кислота
- •§ 26. Меконин
- •§ 27. Ноксирон
- •§ 28. Салициловая кислота
- •§ 29. Антипирин
- •§ 30. Амидопирин
- •§ 31. Фенацетин
- •§ 32. Хинин
- •§ 33. Опий и омнопон
- •§ 34. Морфин
- •§ 35. Кодеин
- •§ 36. Папаверин
- •§ 37. Галантамин
- •§ 38. Анабазин
- •§ 39. Никотин
- •§ 40. Ареколин
- •§ 41. Кониин
- •§ 42. Атропин
- •§ 43. Скополамин
- •§ 44. Кокаин
- •§ 45. Стрихнин
- •§ 46. Бруцин
- •§ 47. Резерпин
- •§ 48. Пахикарпин
- •§ 49. Секуренин
- •§ 50. Эфедрин
- •§ 51. Аконитин
- •§ 52. Новокаин
- •§ 53. Дикаин
- •§ 54. Аминазин
- •§ 55. Дипразин
- •§ 56. Тизерцин
- •§ 57. Хлордиазепоксид
- •§ 58. Диазепам
- •§ 59. Нитразепам
- •§ 60. Оксазепам
- •§ 61. Апоморфин
- •§ 62. Дионин
- •§ 63. Промедол
- •Глава VI. Вещества, изолируемые из объектов минерализацией биологического материала
- •§ 1. Связывание «металлических ядов» биологическим материалом
- •§ 2. Методы минерализации органических веществ
- •§ 3. Сухое озоление и сплавление органических веществ
- •§ 4. Окислители, применяемые для минерализации органических веществ
- •§ 5. Отбор и подготовка проб биологического материала для минерализации
- •§ 6. Разрушение биологического материала азотной и серной кислотами
- •§ 7. Разрушение биологического материала хлорной, азотной и серной кислотами
- •§ 8. Разрушение биологического материала пергидролем и серной кислотой
- •§ 9. Дробный метод и систематический ход анализа «металлических ядов»
- •§ 10. Маскировка ионов в дробном анализе
- •§ 11. Реактивы, применяемые в дробном анализе «металлических ядов» для маскировки ионов
- •§ 12. Реакции, применяемые в химико-токсикологическом анализе для обнаружения ионов металлов
- •§ 13. Соединения бария
- •§ 14. Соединения свинца
- •§ 15. Соединения висмута
- •§ 16. Соединения кадмия
- •§ 17. Соединения марганца
- •§ 18. Соединения меди
- •§ 19. Соединения мышьяка
- •§ 20. Соединения серебра
- •§ 21. Соединения сурьмы
- •§ 22. Соединения таллия
- •§ 23. Соединения хрома
- •§ 24, Соединения цинка
- •§ 25. Соединения ртути
- •§ 26. Количественное определение «металлических ядов» в минерализатах
- •§ 27. Количественное определение ртути
- •§ 28. Экстракционно-фотоколориметрическое определение меди
- •Глава VII. Вещества, изолируемые из биологического материала настаиванием исследуемых объектов с водой
- •Минеральные кислоты и щелочи
- •§ 1. Серная кислота
- •§ 2. Азотная кислота
- •§ 3. Соляная кислота
- •§ 4. Гидроксид калия
- •§ 5. Гидроксид натрия
- •§ 6. Аммиак
- •§ 7. Нитриты
- •Глава VIII. Ядохимикаты и методы их химико-токсикологического анализа
- •§ 1. Классификация ядохимикатов
- •§ 2. Гексахлорциклогексан (гхцг)
- •§ 3. Гептахлор
- •§ 4. Фосфорсодержащие органические соединения и методы их анализа
- •§ 5. Хлорофос
- •§ 6. Карбофос
- •§ 7. Метафос
- •§ 8. Карбарил
- •§ 9. Гранозан
- •Глава IX. Вещества, определяемые непосредственно в биологическом материале
- •§ 1. Оксид углерода (II)
- •§ 2. Спектроскопический метод обнаружения оксида углерода (II) в крови
- •§ 3. Химические методы обнаружения оксида углерода (II) в крови
- •§ 4. Количественное определение оксида углерода (II) в крови
- •Приложение 1. Приготовление реактивов
- •Приложение 2. Приготовление хроматографических пластинок
- •Список рекомендуемой литературы
§ 42. Атропин
Атропинявляетсяалкалоидом, содержащимся в белладонне, скополии и в некоторых других растениях.Атропинпредставляет собойсложный эфиртропина и троповой кислоты.Стереоизомероматропинаявляется гиосциамин, вращающий плоскостьполяризациивлево. Под влияниемщелочейитемпературылевовращающий гиосциамин превращается ватропин, который оптически неактивен. Он состоит из активного левовращающего и малоактивного правовращающегоизомеров. В растениях в основном содержится гиосциамин, а при выделении его из растительного материала он превращается в рацемическую форму —атропин. Основаниеатропинарастворяется вхлороформе(1:1),диэтиловом эфире(1 : 60),этиловом спирте(1 : 3), хуже растворяется вводе(1 : 400).Сульфат атропинарастворяется вводе(1 : 1),этиловом спирте(1:4), практически не растворяется вдиэтиловом эфиреихлороформе.
Атропинэкстрагируется органическимирастворителямииз щелочных водныхрастворов. Максимальные количестваатропинаэкстрагируютсяхлороформомпри рН = 9...П (О. А. Акопян).
Применение. Действие на организм. В медицинской практике используетсясульфат атропина. Он применяется при язвенной болезни желудка и двенадцатиперстной кишки, холецистите, жел-чекаменной болезни, при спазмах кишечника и мочевых путей, бронхиальной астме. В офтальмологииатропинприменяется для расширения зрачка и т. д.
Атропинбыстро всасывается через слизистые оболочки,кожу, кишки (но не через желудок). Принятаядозаатропинапочти полностью всасывается в тонкой кишке в течение двух часов. Примерно половина поступившего ворганизматропинациркулирует в крови, а вторая — связывается сбелкамиплазмы.
Метаболизм. Атропинразлагается ворганизмена тропин и троповую кислоту. Однако это разложение не является основным путемметаболизмаатропина. Об этом свидетельствует то, что только около 2 % троповой кислоты выделяется с мочой. В моче обнаружено 3, а в печени 4метаболитаатропина, которые не идентифицированы. Около 50 % введенного ворганизматропинавыделяется с мочой в неизмененном виде.
Обнаружение атропина
Реакции с реактивами группового осаждения алкалоидов.
Атропиндаетосадки с реактивами Бушарда, Драгендорфа, Майе-ра и др.
Реакция Витали — Морена. Эта реакция основана на том, что при нагреванииатропинасазотной кислотойон разлагается на тропин и троповую кислоту. При действииазотной кислотына троповую кислоту образуется тринитропроизводное этой кислоты, имеющее желтую окраску:
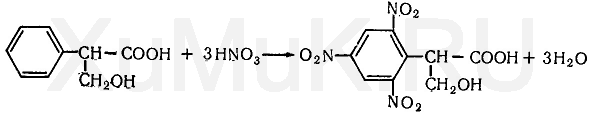
При действии щелочина тринитропроизводное троповой кислоты появляется фиолетовая окраска:

Выполнение реакции. В фарфоровуючашкувносят несколько капель хлороформногораствораисследуемоговеществаи при комнатнойтемпературевыпаривают досуха. К сухому остатку прибавляют 1 мл концентрированнойазотной кислоты,жидкостьна кипящей водяной бане выпаривают досуха. При этом сухой остаток приобретает желтую окраску. К сухому остатку с одной стороны помещают 3—5 капельацетона, а с другой — 1—2 капли 10 %-го спиртовогорастворагидроксида калия. При соприкосновении указанныхрастворовс сухим остатком появляется быстроисчезающая фиолетовая окраска. Появление этой окраски указывает на наличиеатропинав исследуемомрастворе. Предел обнаружения: 1 мкгатропинав пробе.
Кроме атропинаэту реакциюдают: гиосциамин,скополамин, вератрин,стрихнини другиевещества. При наличии перечисленныхвеществокраска имеет несколько иной оттенок и исчезает быстрее, чем окраскаатропина.
Реакция с п -диметиламинобензальдегидом и серной кислотой. К 2—3 каплям исследуемогораствораприбавляют 3—5 капель 0,5 %-горастворап -диметиламинобензальдегида в концентрированнойсерной кислоте.Жидкостьвзбалтывают, а затем нагревают на кипящей водяной бане 5—10 мин. При наличииатропинапоявляется красная окраска, которая переходит в вишнево-красную, а затем в фиолетовую.
Эту реакцию даютгиосциамин искополамин. При наличииморфинаикодеинапоявляется красная окраска, которая не переходит в фиолетовую.Кокаиннедаетокраски с п -диметиламинобензальдегидом.
Реакция с п -диметиламинобензальдегидом и серной кислотойиспользуется главным образом для обнаруженияатропинав лекарственных смесях и для отличия этогоалкалоидаоткокаина.
Реакция с солью Рейнеке. Сухой остаток исследуемоговеществарастворяют в капле 0,1 н.растворасоляной кислоты. Рядом с полученнымрастворомпомещают каплю свежеприготовленного 1 %-горастворасолиРейнеке (NH4[Cr(NH3)2(SCN)4]). При соединении этихрастворовобразуется сиреневого цвета аморфный осадок, быстро переходящий в кристаллический. Образование сростковкристалловс ромбовидными концами указывает на наличиеатропинав пробе. Предел обнаружения: 0,1 мкгатропинав пробе.
Реакция с пикриновой кислотой. Атропинс 0,5 %-мрастворомпикриновой кислотыдаетсветло-желтый кристаллический осадок в виде пластинок или сростков из них. Этот осадок появляется через 15—20 мин. Реакцию спикриновой кислотойвыполняют так, как и ссольюРейнеке. Предел обнаружения: 5 мкгатропинав пробе.
Обнаружение атропина методом хроматографии. Для обнаруженияатропинаметодомхроматографиив тонком слоесиликагеляиспользуется та же методика, которая применяется для обнаружениякодеина. Пятнаатропинана хроматографической пластинке имеют розовато-бурую окраску (Rf = 0,26 ± 0,01).
Обнаружение атропина по УФ- и ИК-спектрам.Атропинв 0,1 н.растворесерной кислотыимеет максимумы поглощения при 252, 258 и 264 нм; в ИК-области спектра основаниеатропина(диск с бромидом калия) имеет основные пики при 1720, 1035 и 1153 см-1.
