
- •Содержание
- •§ 2. Краткий исторический очерк возникновения и развития отечественной токсикологической химии
- •Глава I. Общие вопросы химико-токсикологического анализа
- •§ 1. Объекты химико-токсикологического анализа. Вещественные доказательсва
- •§ 2. Особенности химико-токсикологического анализа
- •§ 3. Осмотр объектов исследования и определение некоторых их свойств
- •§ 4. Предварительные пробы в химико-токсикологическом анализе
- •§ 5. План химико-токсикологического анализа
- •§ 6. Организация органов судебно-медицинской и судебно-химической экспертизы в ссср
- •§ 7. Эксперт-химик
- •§ 8. Правила судебно-химической экспертизы вещественных доказательств
- •§ 9. Акт судебно-химической экспертизы вещественных доказательств
- •§ 10. Некоторые вопросы терминологии в токсикологической химии
- •§ 11. Классификация ядовитых и сильнодействующих веществ в токсикологической химии
- •Глава II. Отравления и некоторые вопросы токсикокинетики ядов
- •§ 1. Отравления и их классификация
- •§ 2. Пути поступления ядов в организм
- •§ 3. Всасывание ядов в организме
- •§ 4. Распределение ядов в организме
- •§ 5. Связывание ядов в организме
- •§ 6. Выделение ядов из организма
- •§ 7. Факторы, влияющие на токсичность химических соединений
- •§ 8. Методы детоксикации
- •§ 9. Метаболизм чужеродных соединений
- •§ 10. Окисление чужеродных соединений
- •§ 11. Восстановление чужеродных соединений
- •§ 12. Гидролиз чужеродных соединений
- •§ 13. Дезалкилирование, дезаминирование и десульфирование чужеродных соединений
- •§ 14. Другие метаболические превращения
- •§ 15. Реакции конъюгации
- •§ 16. Посмертные изменения лекарственных веществ и ядов в трупах
- •§ 17. Разложение биологического материала после наступления смерти
- •§ 18. Изменение ядов при разложении трупов
- •Глава III. Методы анализа, применяемые в токсикологической химии
- •§ 1. Метод экстракции
- •§ 2. Микрокристаллоскопический анализ
- •§ 3. Метод микродиффузии
- •Глава IV. Ядовитые и сильнодействующие вещества, изолируемые из биологического материала перегонкой с водяным паром
- •§ 1. Аппараты для перегонки с водяным паром
- •§2. Влияние рН среды на перегонку химических соединений с водяным паром
- •§ 3. Перегонка ядовитых веществ с водяным паром из подкисленного биологического материала
- •§ 4. Перегонка ядовитых веществ с водяным паром из подкисленного, а затем из подщелоченного биологического материала
- •§ 5. Фракционная перегонка веществ, содержащихся в дистиллятах
- •§ 6. Синильная кислота
- •§ 7. Формальдегид
- •§ 8. Метиловый спирт
- •§ 9. Этиловый спирт
- •§ 10. Изоамиловый спирт
- •§ 11. Ацетон
- •§ 12. Фенол
- •§ 13. Крезолы
- •§ 14. Хлороформ
- •§ 15. Хлоралгидрат
- •§ 16. Четыреххлористый углерод
- •§ 17. Дихлорэтан
- •§ 18. Реакции, позволяющие отличить хлорпроизводные друг от друга
- •§ 19. Тетраэтилсвинец
- •§ 20. Уксусная кислота
- •§ 21. Этиленгликоль
- •Глава V. Ядовитые и сильнодействующие вещества, изолируемые из биологического материала подкисленным этиловым спиртом или подкисленной водой
- •§ 1. Развитие методов выделения алкалоидов и других азотистых оснований из биологического материала
- •§ 2. Влияние рН среды на изолирование алкалоидов и других азотистых оснований из биологического материала
- •§ 3. Влияние состава извлекающих жидкостей на изолирование алкалоидов и других азотистых основании из биологического материала
- •§ 4. Влияние подкисленной воды и подкисленного спирта на извлечение примесей, переходящих в вытяжки из биологического материала
- •§ 5. Очистка вытяжек из биологического материала от примесей
- •§ 6. Экстракция алкалоидов и других токсических веществ из вытяжек
- •§ 7. Обнаружение ядовитых веществ, изолируемых подкисленной водой или подкисленным этиловым спиртом
- •§ 8. Количественное определение токсических веществ, изолированных подкисленной водой или подкисленным спиртом
- •§ 9. Метод выделения токсических веществ, основанный на изолировании их этиловым спиртом подкисленным щавелевой кислотой
- •§ 10. Метод выделения токсических веществ, основанный на изолировании их водой, подкисленной щавелевой кислотой
- •§ 11. Метод выделения токсических веществ, основанный на изолировании их водой, подкисленной серной кислотой
- •§ 12. Барбитураты и методы их исследования
- •§ 13. Барбамил
- •§ 14. Барбитал
- •§ 15. Фенобарбитал
- •§ 16. Бутобарбитал
- •§ 17. Этаминал-натрий
- •8.Обнаружение этаминала-натрия по уф- и ик-спектрам.
- •§ 18. Бензонал
- •§ 19. Гексенал
- •§ 20. Производные ксантина
- •§ 21. Кофеин
- •§ 22. Теобромин
- •§ 23. Теофиллин
- •§ 24. Наркотин
- •§ 25. Меконовая кислота
- •§ 26. Меконин
- •§ 27. Ноксирон
- •§ 28. Салициловая кислота
- •§ 29. Антипирин
- •§ 30. Амидопирин
- •§ 31. Фенацетин
- •§ 32. Хинин
- •§ 33. Опий и омнопон
- •§ 34. Морфин
- •§ 35. Кодеин
- •§ 36. Папаверин
- •§ 37. Галантамин
- •§ 38. Анабазин
- •§ 39. Никотин
- •§ 40. Ареколин
- •§ 41. Кониин
- •§ 42. Атропин
- •§ 43. Скополамин
- •§ 44. Кокаин
- •§ 45. Стрихнин
- •§ 46. Бруцин
- •§ 47. Резерпин
- •§ 48. Пахикарпин
- •§ 49. Секуренин
- •§ 50. Эфедрин
- •§ 51. Аконитин
- •§ 52. Новокаин
- •§ 53. Дикаин
- •§ 54. Аминазин
- •§ 55. Дипразин
- •§ 56. Тизерцин
- •§ 57. Хлордиазепоксид
- •§ 58. Диазепам
- •§ 59. Нитразепам
- •§ 60. Оксазепам
- •§ 61. Апоморфин
- •§ 62. Дионин
- •§ 63. Промедол
- •Глава VI. Вещества, изолируемые из объектов минерализацией биологического материала
- •§ 1. Связывание «металлических ядов» биологическим материалом
- •§ 2. Методы минерализации органических веществ
- •§ 3. Сухое озоление и сплавление органических веществ
- •§ 4. Окислители, применяемые для минерализации органических веществ
- •§ 5. Отбор и подготовка проб биологического материала для минерализации
- •§ 6. Разрушение биологического материала азотной и серной кислотами
- •§ 7. Разрушение биологического материала хлорной, азотной и серной кислотами
- •§ 8. Разрушение биологического материала пергидролем и серной кислотой
- •§ 9. Дробный метод и систематический ход анализа «металлических ядов»
- •§ 10. Маскировка ионов в дробном анализе
- •§ 11. Реактивы, применяемые в дробном анализе «металлических ядов» для маскировки ионов
- •§ 12. Реакции, применяемые в химико-токсикологическом анализе для обнаружения ионов металлов
- •§ 13. Соединения бария
- •§ 14. Соединения свинца
- •§ 15. Соединения висмута
- •§ 16. Соединения кадмия
- •§ 17. Соединения марганца
- •§ 18. Соединения меди
- •§ 19. Соединения мышьяка
- •§ 20. Соединения серебра
- •§ 21. Соединения сурьмы
- •§ 22. Соединения таллия
- •§ 23. Соединения хрома
- •§ 24, Соединения цинка
- •§ 25. Соединения ртути
- •§ 26. Количественное определение «металлических ядов» в минерализатах
- •§ 27. Количественное определение ртути
- •§ 28. Экстракционно-фотоколориметрическое определение меди
- •Глава VII. Вещества, изолируемые из биологического материала настаиванием исследуемых объектов с водой
- •Минеральные кислоты и щелочи
- •§ 1. Серная кислота
- •§ 2. Азотная кислота
- •§ 3. Соляная кислота
- •§ 4. Гидроксид калия
- •§ 5. Гидроксид натрия
- •§ 6. Аммиак
- •§ 7. Нитриты
- •Глава VIII. Ядохимикаты и методы их химико-токсикологического анализа
- •§ 1. Классификация ядохимикатов
- •§ 2. Гексахлорциклогексан (гхцг)
- •§ 3. Гептахлор
- •§ 4. Фосфорсодержащие органические соединения и методы их анализа
- •§ 5. Хлорофос
- •§ 6. Карбофос
- •§ 7. Метафос
- •§ 8. Карбарил
- •§ 9. Гранозан
- •Глава IX. Вещества, определяемые непосредственно в биологическом материале
- •§ 1. Оксид углерода (II)
- •§ 2. Спектроскопический метод обнаружения оксида углерода (II) в крови
- •§ 3. Химические методы обнаружения оксида углерода (II) в крови
- •§ 4. Количественное определение оксида углерода (II) в крови
- •Приложение 1. Приготовление реактивов
- •Приложение 2. Приготовление хроматографических пластинок
- •Список рекомендуемой литературы
§ 40. Ареколин
Ареколин(метиловый эфир 1-метил-1,2,5,6-тет-рагидроникотиновой кислоты) относится калкалоидам, содержащимся вплодахарековой пальмы. В этихплодахкромеареколинасодержатся и другиеалкалоиды(арекаидин, норареколин, норарекаидин). Основаниеареколинапредставляет собой бесцветную густую маслянистуюжидкость, летучую с водянымпаром, смешивающуюся сводойи многими органическимирастворителями.Ареколиноптически не активен.
Ареколинэкстрагируется органическимирастворителямииз щелочных водныхрастворов.
Водные растворыоснованияареколинаимеют сильно щелочную реакцию, о чем свидетельствует то, что при действии этого основания насолиряда тяжелыхметалловвыпадают их гид-роксиды. Израстворовсолейсеребрапод влиянием основанияареколинавыделяется металлическоесеребро.
Применение. Действие на организм.Гидробромидареколинав основном применяется в ветеринарной практике в качестве слабительного и глистогонного средства, а также как заменительпилокарпинаи эзерина в офтальмологии. По действиюареколинблизок к мускарину иацетилхолину. Под влияниемареколинаусиливается слюноотделение, снижается кровяноедавление, происходит сокращение гладкой мускулатуры, суживаются зрачки.Ареколинв небольшихдозахвозбуждает, а в большихдозахпарализует центральную нервную систему. Он оказывает сильное влияние на органы пищеварения, усиливаетсекрециюпищеварительныхжелези вызывает сокращение мускулатуры кишок.
Выделение ареколина из биологического материала.Для этой цели может быть использован методперегонкис водянымпаром, а также методы, основанные на изолировании еговодой, подкисленной серной илищавелевой кислотой.
Обнаружение ареколина
Для обнаружения ареколинаприменяют ряд реакций и методыспектроскопии.
Реакция с реактивом Драгендорфа.2—3 капли хлороформногораствораисследуемоговеществананосят на предметное
стекло и выпаривают досуха. Остаток растворяют в 1 капле 0,1 н. растворасоляной кислотыи прибавляют каплю реактива Драгендорфа. После этого предметное стекло вносят во влажную камеру (см. гл. III, § 2) на 10—30 мин. При наличииареколинаобразуются оранжево-красныекристаллы, представляющие собой сростки из ромбов или параллелограммов. Предел обнаружения: 0,2 мкгареколинав пробе.
Реакция с пикриновой кислотой.2—3 капли хлороформногораствораисследуемоговеществананосят на предметное стекло и выпаривают досуха. Сухой остаток растворяют в 1 капле 0,1 н.растворасоляной кислоты, а затем прибавляют 1 каплю 0,5 %-горастворапикриновой кислоты. Через несколько минут появляются темно-зеленыекристаллы(сферолиты, со временем распадающиеся на отдельные призматические кристаллы). Предел обнаружения: 0,2 мкгареколинав пробе.
Обнаружение ареколина по УФ- и ИК-спектрам.Спиртовойраствороснования!ареколинаимеет максимум поглощения при 214 нм. В ИК-облвсти спектра основаниеареколина(диск с бромидом калия) имеет основные пики при 1712, 1262 и 1135 см-1.
§ 41. Кониин
Кониин (α-пропилпиперидин) относится к числу алкалоидов, содержащихся в болиголове, в котором содержатся и другиеалкалоиды(N-метилкониин, коницеин, конгидрин и др.). Аналогичная смесьалкалоидовнайдена в кокорыше. Болиголов широко распространенное растение, произрастающее в зоне умеренного климата. Он давно известен своей ядовитостью. Кониин и другиеалкалоидысодержатся во всех частях болиголова, однако наиболее богатые конииномплодыэтого растения до их полного дозревания.
Кониин представляет собой бесцветную жидкостьс сильным запахом, напоминающим запах мышиной мочи, имеющую сильно щелочную реакцию. Кониин разлагается навоздухе, в результате этого приобретаетбуруюокраску. Он перегоняется с водянымпаромбез разложения. Основание кониина растворяется вводе(1 : 100), слабее растворяется вхлороформе, смешивается сэтиловым спиртомидиэтиловым эфиром. При повышениитемпературырастворимостькониина вводепонижается. Поэтому при нагревании насыщенных водныхрастворовкониина они мутнеют. Кониин экстрагируется органическимирастворителямииз щелочных водныхрастворов. Его можно изолировать подкисленнойводойилиперегонкойс водянымпаромиз подщелоченных объектов.
Применение. Действие на организм.В связи с высокойтоксичностьюкониина он не применяется в медицине. Токсические свойства кониина были известны еще в глубокой древности. Согласно литературнымданным, в Древней Греции кониин применялся для отравления инакомыслящих, приговоренных к смертной казни. В частности, кониином был отравлен видный древнегреческий философ Сократ (469—399 г. до н. э.).
В настоящее время встречаются случайные отравления растениями, содержащими кониин. Это имеет место при употреблении в пищу корня болиголова (вместо хрена) или его листьев (вместо петрушки). Отмечены случаи отравления плодамиболиголова, при ошибочном применении их вместоплодов аниса. Также имели место случаи отравления скота свежей травой, в которой находились растения, содержащие кониин.
Кониин быстро всасывается в кровь из пищевого канала. После всасывания кониина в кровь он вызывает паралич окончаний двигательных нервов. Кониин сначала возбуждает, а затем парализует центральную нервную систему. Под влиянием кониина вначале усиливается, а затем ослабляется дыхание. После приема кониина усиливается слюнотечение, появляются тошнота, рвота, понос, головокружение, расстройство зрения. На лягушек кониин действует аналогичнокурарину. При отравлении кониином смерть наступает от параличадыхания.
Патологоанатомическая картина при отравлении кониином не характерна. Кониин выделяется из организмас мочой и выдыхаемымвоздухом.Метаболитыкониина не изучены.
Обнаружение кониина
Для обнаружения кониина предложено ограниченное число реакций.
Реакции с реактивами группового осажденияалкалоидов. Конииндаетосадки с реактивами Бушарда, Драгендорфа, Майера и др.
Реакция образования дитиокарбамата меди.Кониин и другие вторичныеаминыссероуглеродоми аммиачнымрастворомсульфата медиобразуют нерастворимые вводедитиокарбаматы:
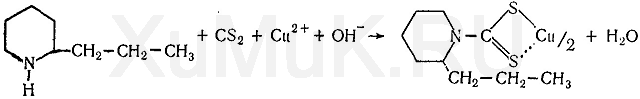
Выполнение реакции:В микропробирку вносят каплю подкисленногораствораисследуемоговещества, прибавляют каплю 5 %-горастворасульфата меди, а затем 5 %-йраствор аммиакадо щелочной реакции и взбалтывают. После этого прибавляют 2 капли смесисероуглеродаибензола(1 : 3). При наличии кониина бензольный слой приобретает коричневую или желтую окраску. Предел обнаружения: 1 мкг кониина в пробе.
Эту реакцию даетэфедрини ряд других вторичныхаминов. Первичные и третичныеаминынедаютэтой реакции. Реакция образования дитиокарбаматамедиприменяется для обнаружения кониина в растительном сырье. При хорошей очистке вытяжек эта реакция может быть использована и для обнаружения кониина, выделенного из биологического материала.
Реакция с реактивом Драгендорфа.На предметное стекло наносят 2—3 капли хлороформногораствораисследуемоговеществаи выпаривают досуха. Сухой остаток растворяют в одной капле 0,1 н.растворасоляной кислоты. К полученномурастворуприбавляют каплю реактива Драгендорфа. После этого предметное стекло помещают во влажную камеру на 10—15 мин (см. гл. III, § 2), а затем под микроскопом рассматривают форму образовавшихсякристаллов. При наличии кониина образуются оранжево-красныекристаллы, имеющие форму ромбов, параллелограммов или сростков из них. Предел обнаружения: 3,5 мкг кониина в пробе.
Получение сублимата хлоргидрата кониина.Несколько капель хлороформногораствораисследуемоговеществавносят в маленький тигель и при комнатнойтемпературевыпаривают досуха. К остатку прибавляют 2—3 капли 1 %-горастворасоляной кислоты.Жидкостьоставляют при комнатнойтемпературепочти до полноговыпаривания. Затем тигель накрывают предметным стеклом и 20—30 мин нагревают на песочной бане (120—130 °С), постоянно охлаждая предметное стекло влажнымватным тампономили влажнойфильтровальной бумагой. После этого образовавшийся на предметном стекле сублимат рассматривают под микроскопом. При наличии кониина в поле зрения микроскопа видны бесцветные игольчатыекристаллы. Предел обнаружения: 0,33 мкг кониина в пробе.
Обнаружение кониина по УФ-спектру.Кониин в 0,2 н.растворесерной кислотыимеет максимум поглощения при 266—270 нм.
