
- •Содержание
- •§ 2. Краткий исторический очерк возникновения и развития отечественной токсикологической химии
- •Глава I. Общие вопросы химико-токсикологического анализа
- •§ 1. Объекты химико-токсикологического анализа. Вещественные доказательсва
- •§ 2. Особенности химико-токсикологического анализа
- •§ 3. Осмотр объектов исследования и определение некоторых их свойств
- •§ 4. Предварительные пробы в химико-токсикологическом анализе
- •§ 5. План химико-токсикологического анализа
- •§ 6. Организация органов судебно-медицинской и судебно-химической экспертизы в ссср
- •§ 7. Эксперт-химик
- •§ 8. Правила судебно-химической экспертизы вещественных доказательств
- •§ 9. Акт судебно-химической экспертизы вещественных доказательств
- •§ 10. Некоторые вопросы терминологии в токсикологической химии
- •§ 11. Классификация ядовитых и сильнодействующих веществ в токсикологической химии
- •Глава II. Отравления и некоторые вопросы токсикокинетики ядов
- •§ 1. Отравления и их классификация
- •§ 2. Пути поступления ядов в организм
- •§ 3. Всасывание ядов в организме
- •§ 4. Распределение ядов в организме
- •§ 5. Связывание ядов в организме
- •§ 6. Выделение ядов из организма
- •§ 7. Факторы, влияющие на токсичность химических соединений
- •§ 8. Методы детоксикации
- •§ 9. Метаболизм чужеродных соединений
- •§ 10. Окисление чужеродных соединений
- •§ 11. Восстановление чужеродных соединений
- •§ 12. Гидролиз чужеродных соединений
- •§ 13. Дезалкилирование, дезаминирование и десульфирование чужеродных соединений
- •§ 14. Другие метаболические превращения
- •§ 15. Реакции конъюгации
- •§ 16. Посмертные изменения лекарственных веществ и ядов в трупах
- •§ 17. Разложение биологического материала после наступления смерти
- •§ 18. Изменение ядов при разложении трупов
- •Глава III. Методы анализа, применяемые в токсикологической химии
- •§ 1. Метод экстракции
- •§ 2. Микрокристаллоскопический анализ
- •§ 3. Метод микродиффузии
- •Глава IV. Ядовитые и сильнодействующие вещества, изолируемые из биологического материала перегонкой с водяным паром
- •§ 1. Аппараты для перегонки с водяным паром
- •§2. Влияние рН среды на перегонку химических соединений с водяным паром
- •§ 3. Перегонка ядовитых веществ с водяным паром из подкисленного биологического материала
- •§ 4. Перегонка ядовитых веществ с водяным паром из подкисленного, а затем из подщелоченного биологического материала
- •§ 5. Фракционная перегонка веществ, содержащихся в дистиллятах
- •§ 6. Синильная кислота
- •§ 7. Формальдегид
- •§ 8. Метиловый спирт
- •§ 9. Этиловый спирт
- •§ 10. Изоамиловый спирт
- •§ 11. Ацетон
- •§ 12. Фенол
- •§ 13. Крезолы
- •§ 14. Хлороформ
- •§ 15. Хлоралгидрат
- •§ 16. Четыреххлористый углерод
- •§ 17. Дихлорэтан
- •§ 18. Реакции, позволяющие отличить хлорпроизводные друг от друга
- •§ 19. Тетраэтилсвинец
- •§ 20. Уксусная кислота
- •§ 21. Этиленгликоль
- •Глава V. Ядовитые и сильнодействующие вещества, изолируемые из биологического материала подкисленным этиловым спиртом или подкисленной водой
- •§ 1. Развитие методов выделения алкалоидов и других азотистых оснований из биологического материала
- •§ 2. Влияние рН среды на изолирование алкалоидов и других азотистых оснований из биологического материала
- •§ 3. Влияние состава извлекающих жидкостей на изолирование алкалоидов и других азотистых основании из биологического материала
- •§ 4. Влияние подкисленной воды и подкисленного спирта на извлечение примесей, переходящих в вытяжки из биологического материала
- •§ 5. Очистка вытяжек из биологического материала от примесей
- •§ 6. Экстракция алкалоидов и других токсических веществ из вытяжек
- •§ 7. Обнаружение ядовитых веществ, изолируемых подкисленной водой или подкисленным этиловым спиртом
- •§ 8. Количественное определение токсических веществ, изолированных подкисленной водой или подкисленным спиртом
- •§ 9. Метод выделения токсических веществ, основанный на изолировании их этиловым спиртом подкисленным щавелевой кислотой
- •§ 10. Метод выделения токсических веществ, основанный на изолировании их водой, подкисленной щавелевой кислотой
- •§ 11. Метод выделения токсических веществ, основанный на изолировании их водой, подкисленной серной кислотой
- •§ 12. Барбитураты и методы их исследования
- •§ 13. Барбамил
- •§ 14. Барбитал
- •§ 15. Фенобарбитал
- •§ 16. Бутобарбитал
- •§ 17. Этаминал-натрий
- •8.Обнаружение этаминала-натрия по уф- и ик-спектрам.
- •§ 18. Бензонал
- •§ 19. Гексенал
- •§ 20. Производные ксантина
- •§ 21. Кофеин
- •§ 22. Теобромин
- •§ 23. Теофиллин
- •§ 24. Наркотин
- •§ 25. Меконовая кислота
- •§ 26. Меконин
- •§ 27. Ноксирон
- •§ 28. Салициловая кислота
- •§ 29. Антипирин
- •§ 30. Амидопирин
- •§ 31. Фенацетин
- •§ 32. Хинин
- •§ 33. Опий и омнопон
- •§ 34. Морфин
- •§ 35. Кодеин
- •§ 36. Папаверин
- •§ 37. Галантамин
- •§ 38. Анабазин
- •§ 39. Никотин
- •§ 40. Ареколин
- •§ 41. Кониин
- •§ 42. Атропин
- •§ 43. Скополамин
- •§ 44. Кокаин
- •§ 45. Стрихнин
- •§ 46. Бруцин
- •§ 47. Резерпин
- •§ 48. Пахикарпин
- •§ 49. Секуренин
- •§ 50. Эфедрин
- •§ 51. Аконитин
- •§ 52. Новокаин
- •§ 53. Дикаин
- •§ 54. Аминазин
- •§ 55. Дипразин
- •§ 56. Тизерцин
- •§ 57. Хлордиазепоксид
- •§ 58. Диазепам
- •§ 59. Нитразепам
- •§ 60. Оксазепам
- •§ 61. Апоморфин
- •§ 62. Дионин
- •§ 63. Промедол
- •Глава VI. Вещества, изолируемые из объектов минерализацией биологического материала
- •§ 1. Связывание «металлических ядов» биологическим материалом
- •§ 2. Методы минерализации органических веществ
- •§ 3. Сухое озоление и сплавление органических веществ
- •§ 4. Окислители, применяемые для минерализации органических веществ
- •§ 5. Отбор и подготовка проб биологического материала для минерализации
- •§ 6. Разрушение биологического материала азотной и серной кислотами
- •§ 7. Разрушение биологического материала хлорной, азотной и серной кислотами
- •§ 8. Разрушение биологического материала пергидролем и серной кислотой
- •§ 9. Дробный метод и систематический ход анализа «металлических ядов»
- •§ 10. Маскировка ионов в дробном анализе
- •§ 11. Реактивы, применяемые в дробном анализе «металлических ядов» для маскировки ионов
- •§ 12. Реакции, применяемые в химико-токсикологическом анализе для обнаружения ионов металлов
- •§ 13. Соединения бария
- •§ 14. Соединения свинца
- •§ 15. Соединения висмута
- •§ 16. Соединения кадмия
- •§ 17. Соединения марганца
- •§ 18. Соединения меди
- •§ 19. Соединения мышьяка
- •§ 20. Соединения серебра
- •§ 21. Соединения сурьмы
- •§ 22. Соединения таллия
- •§ 23. Соединения хрома
- •§ 24, Соединения цинка
- •§ 25. Соединения ртути
- •§ 26. Количественное определение «металлических ядов» в минерализатах
- •§ 27. Количественное определение ртути
- •§ 28. Экстракционно-фотоколориметрическое определение меди
- •Глава VII. Вещества, изолируемые из биологического материала настаиванием исследуемых объектов с водой
- •Минеральные кислоты и щелочи
- •§ 1. Серная кислота
- •§ 2. Азотная кислота
- •§ 3. Соляная кислота
- •§ 4. Гидроксид калия
- •§ 5. Гидроксид натрия
- •§ 6. Аммиак
- •§ 7. Нитриты
- •Глава VIII. Ядохимикаты и методы их химико-токсикологического анализа
- •§ 1. Классификация ядохимикатов
- •§ 2. Гексахлорциклогексан (гхцг)
- •§ 3. Гептахлор
- •§ 4. Фосфорсодержащие органические соединения и методы их анализа
- •§ 5. Хлорофос
- •§ 6. Карбофос
- •§ 7. Метафос
- •§ 8. Карбарил
- •§ 9. Гранозан
- •Глава IX. Вещества, определяемые непосредственно в биологическом материале
- •§ 1. Оксид углерода (II)
- •§ 2. Спектроскопический метод обнаружения оксида углерода (II) в крови
- •§ 3. Химические методы обнаружения оксида углерода (II) в крови
- •§ 4. Количественное определение оксида углерода (II) в крови
- •Приложение 1. Приготовление реактивов
- •Приложение 2. Приготовление хроматографических пластинок
- •Список рекомендуемой литературы
§ 12. Фенол
Фенолпредставляет собой тонкие длинные игольчатыекристаллыили бесцветную кристаллическую массу со своеобразным запахом. Навоздухеон постепенно розовеет.Фенолрастворяется вводев соотношении 1 : 20, легко растворяется вэтиловом спирте, диэти-ловом эфире,хлороформе,жирных маслах,растворахедкихщелочей.

Применение. Действие наорганизм.Фенолприменяется в медицинской практике какдезинфицирующее средство. Он широко используется вхимическойпромышленности для получения многиххимическихсоединений (красителей,пластических масс, фармацевтических препаратов, средств защиты растений).
Фенолвсасывается в кровь через слизистые оболочки икожу, а затем распределяется в органах итканях.Фенол, поступивший ворганизмчерез пищевой канал, вызывает боли в желудке, рвоту, понос, иногда с примесями крови. Моча отравленныхфеноломимеет оливковый или оливково-черный цвет. При пероральном поступлении ворганизм10—15 гфеноланаступает смерть. После вскрытия трупов лиц, отравленныхфенолом, наибольшее количество его можно найти в почках, затем в печени, сердце, крови и головном мозгу.
Метаболизм.Частьфенолаворганизмесвязывается сбелками, а ча-сть — подвергаетсяокислениюс образованиемгидрохинонаипирокатехина. Несвязанныйфеноли егометаболиты(гидрохинон и пирокатехин) выделяются с мочой в виде конъюгатов с сульфатами иглюкуроновой кислотой.
Выделение фенола из биологического материала.Фенол, содержащийся в трупном материале, выделяют путемперегонкис водянымпаром, как и другиевеществаэтой группы ядов. В ряде случаев возникает необходимость производить обнаружение и количественное определениефенолав моче.
В моче людей и животных, отравленных фенолом, он может находиться в несвязанном виде и в виде конъюгатов с сульфатами илиглюкуроновой кислотой. Для изолирования несвязанногофенолаиз мочи ее подкисляют слабымрастворомуксусной кислоты, а затемфенолотгоняют с водянымпаром. Дистиллят, в который может переходить какфенол, так и частьуксусной кислоты, нейтрализуютгидрокарбонатом натрия, а затем из дистиллятафенолэкстрагируют органическимрастворителем. Полученную вытяжку используют для обнаружения и количественного определенияфенола.
Обнаружение фенола
Для обнаружения фенолаиспользуется часть третьего дистиллята, который вносят в делительную воронку, прибавляютрастворгидрокарбоната натриядо щелочной реакции. Содержимое делительной воронки 2—3 раза взбалтывают с новыми порциямидиэтилового эфирапо 10 мл. Эфирные вытяжки соединяют вместе и при комнатнойтемпературевыпаривают досуха. Сухой остаток растворяют в 2—3 млводы. Полученныйраствориспользуют для обнаруженияфенолапри помощи реакций образования трибромфенола,индофенола, а также реакций схлоридом железа(III), реактивом Миллона и др.
Реакция с бромной водой. От прибавления бромнойводыкфенолувыпадает осадок трибромфенола:

Выполнение реакции. К 0,5—1,0 мл исследуемогораствораприбавляют 3—5 капель бромнойводы. При наличиифенолав исследуемомраствореобразуется желтовато-белый осадок трибромфенола. Эту реакциюдаюткрезолы,анилини некоторые другие ароматическиеамины.
Приготовление реактива (см. Приложение 1, реактив 3).
Индофеноловая реакция. Приокислениисмесифеноловиаминов(в том числе и аммиака) образуютсяиндофенолы, имеющие соответствующую окраску:

При выполнении индофеноловой реакции в качестве окислителеймогут быть использованыгипохлорит натрия,хлорная известь, хлорная или бромнаявода,пероксид водородаи др.Окислителемтакже может бытькислородвоздуха.
Выполнение реакции. К 0,5—1,0 мл исследуемогораствораприбавляют 1 каплюанилинаи 2 млрастворагипохлорита натрия. Появление грязно-фиолетовой окраски указывает на наличиефенолав пробе. После прибавленияаммиакапоявляется устойчивая синяя окраска.
Индофеноловую реакцию даютфенолы, имеющие свободное параположение,крезолыи другие соединения, содержащие фенольную группу.
Приготовление реактива (см. Приложение 1, реактив 10).
Реакция Либермана.Эта реакция также основана на образованиииндофенола. В качестве реактивов нафенолыприменяютнитрит натрияисерную кислоту. При взаимодействиинитрита натрияисерной кислотыобразуетсяазотистая кислота, которая сфеноломобразует n -нитрозофенол, приизомеризациикоторого образуется n -хиноидоксим:

При взаимодействии хиноидоксима с избытком фенолаобразуетсяиндофенол, имеющий синюю окраску:

Выполнение реакции. 1—2 капли исследуемогораствора(лучшебратьрастворисследуемоговеществав диэтиловом эфире) вносят в маленький тигель и выпаривают досуха. К сухому остатку прибавляют каплю 1 %-го свежеприготовленногорастворанитрита натрияв концентрированнойсерной кислотеи смесь оставляют на несколько минут. После охлаждения смеси по каплям прибавляют 4 н.растворгидроксида натриядо щелочной реакции (по лакмусу). Появление синей окраски, которая может переходить в красную, а затем в зеленую, указывает на наличиефенолав пробе.Реакцию Либерманадаютнекоторыефенолы, эфирыфенолов,тиофени др. Недаютэтой реакциинитрофенолы, паразамещенныефенолыи др.
Реакция с хлоридом железа (III).От прибавленияхлорида железа(III) кфенолупоявляется окраска.
Выполнение реакции. 1—2 капли исследуемогорастворапомещают на фарфоровую пластинку или в маленькую фарфоровуючашкуи прибавляют 1—2 капли свежеприготовленного 5 %-горастворахлорида железа(III). При наличиифенолапоявляется фиолетовая или сине-фиолетовая окраска, исчезающая от прибавленияводы,спиртаи кислот.
С хлоридом железа(III)даютокраскукрезолы,оксипиридины, оксихинолин и ряд другихвеществ, содержащих фенольные группы. Состав и окраска образующихся соединений зависят от природы исследуемыхвеществ,растворителейи рН среды. о -Крезол и n -крезол схлоридом железа(III)даютсинюю окраску, а м -крезол — красно-фиолетовую.
Реакция с реактивом Миллона. При взаимодействиифенолас реактивом Миллона (смесь нитратов одно- и двухвалентнойртути, содержащая азотистую кислоту) появляется красная или оранжевая окраска. При малых количествахфеноловвозникает желтая окраска. Нагревание ускоряет эту реакцию. Вероятно, что при этой реакции вначале образуется 2-нитрозофенол, который переходит в 1,2-хинонмоноксим:

1,2-хинонмоноксим с ионамиртутиобразует окрашенное внутрикомплексное соединение:
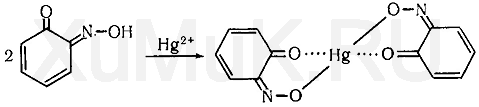
Выполнение реакции. В микротигель вносят 1—2 капли исследуемогораствора, прибавляют 1—2 капли реактива Миллона и оставляют на несколько минут. Если за это время не произойдет изменение окраски, то смесь нагревают докипенияи кипятят несколько минут. Появление красной окраски указывает на наличиефенолав пробе. Эту реакциюдаютнекоторыефенолы,анилин, эфирыфенолов, которые при нагревании образуютфенол. Эта реакция часто используется для обнаружения пара-замещенныхфенола, которые не могут быть обнаружены при помощиреакции Либермана.
Приготовление реактива (см. Приложение 1, реактив 39).
Реакция с бензальдегидом. При нагреваниифеноловв кислой среде сбензальдегидом(как и с рядом других альдегидов) образуется бесцветный продуктконденсации, приокислениикоторого возникает окраска. Концентрированнаясерная кислотапри этой реакции играет роль дегидратирующего и конденсирующеговещества, а также рольокислителя.
Выполнение реакции. В пробирку вносят 0,1—0,5 мл исследуемогораствора, 2 мл концентрированнойсерной кислотыи 1— 2 каплибензальдегида. При нагревании смеси докипенияпоявляется темно-красная окраска. После охлаждения смеси и прибавления к ней 10 млводыи 10 %-горастворагидроксида натриядо щелочной реакции (по лакмусу) окраска переходит в сине-фиолетовую. При взбалтывании этогорастворасдиэтиловым эфиромилихлороформомокраска переходит в слой органическогорастворителя. Эту реакциюдаютфеноли о-крезол. Другиекрезолынедаютэтой реакции.
Метод микродиффузии. Этот метод, основанный на реакции с реактивом Фолина — Чиокальто, применяется для обнаруженияфенолав моче, крови и гомогенатахтканей. Подробно этот метод описан выше (см. гл. III, § 3).
