
- •Содержание
- •§ 2. Краткий исторический очерк возникновения и развития отечественной токсикологической химии
- •Глава I. Общие вопросы химико-токсикологического анализа
- •§ 1. Объекты химико-токсикологического анализа. Вещественные доказательсва
- •§ 2. Особенности химико-токсикологического анализа
- •§ 3. Осмотр объектов исследования и определение некоторых их свойств
- •§ 4. Предварительные пробы в химико-токсикологическом анализе
- •§ 5. План химико-токсикологического анализа
- •§ 6. Организация органов судебно-медицинской и судебно-химической экспертизы в ссср
- •§ 7. Эксперт-химик
- •§ 8. Правила судебно-химической экспертизы вещественных доказательств
- •§ 9. Акт судебно-химической экспертизы вещественных доказательств
- •§ 10. Некоторые вопросы терминологии в токсикологической химии
- •§ 11. Классификация ядовитых и сильнодействующих веществ в токсикологической химии
- •Глава II. Отравления и некоторые вопросы токсикокинетики ядов
- •§ 1. Отравления и их классификация
- •§ 2. Пути поступления ядов в организм
- •§ 3. Всасывание ядов в организме
- •§ 4. Распределение ядов в организме
- •§ 5. Связывание ядов в организме
- •§ 6. Выделение ядов из организма
- •§ 7. Факторы, влияющие на токсичность химических соединений
- •§ 8. Методы детоксикации
- •§ 9. Метаболизм чужеродных соединений
- •§ 10. Окисление чужеродных соединений
- •§ 11. Восстановление чужеродных соединений
- •§ 12. Гидролиз чужеродных соединений
- •§ 13. Дезалкилирование, дезаминирование и десульфирование чужеродных соединений
- •§ 14. Другие метаболические превращения
- •§ 15. Реакции конъюгации
- •§ 16. Посмертные изменения лекарственных веществ и ядов в трупах
- •§ 17. Разложение биологического материала после наступления смерти
- •§ 18. Изменение ядов при разложении трупов
- •Глава III. Методы анализа, применяемые в токсикологической химии
- •§ 1. Метод экстракции
- •§ 2. Микрокристаллоскопический анализ
- •§ 3. Метод микродиффузии
- •Глава IV. Ядовитые и сильнодействующие вещества, изолируемые из биологического материала перегонкой с водяным паром
- •§ 1. Аппараты для перегонки с водяным паром
- •§2. Влияние рН среды на перегонку химических соединений с водяным паром
- •§ 3. Перегонка ядовитых веществ с водяным паром из подкисленного биологического материала
- •§ 4. Перегонка ядовитых веществ с водяным паром из подкисленного, а затем из подщелоченного биологического материала
- •§ 5. Фракционная перегонка веществ, содержащихся в дистиллятах
- •§ 6. Синильная кислота
- •§ 7. Формальдегид
- •§ 8. Метиловый спирт
- •§ 9. Этиловый спирт
- •§ 10. Изоамиловый спирт
- •§ 11. Ацетон
- •§ 12. Фенол
- •§ 13. Крезолы
- •§ 14. Хлороформ
- •§ 15. Хлоралгидрат
- •§ 16. Четыреххлористый углерод
- •§ 17. Дихлорэтан
- •§ 18. Реакции, позволяющие отличить хлорпроизводные друг от друга
- •§ 19. Тетраэтилсвинец
- •§ 20. Уксусная кислота
- •§ 21. Этиленгликоль
- •Глава V. Ядовитые и сильнодействующие вещества, изолируемые из биологического материала подкисленным этиловым спиртом или подкисленной водой
- •§ 1. Развитие методов выделения алкалоидов и других азотистых оснований из биологического материала
- •§ 2. Влияние рН среды на изолирование алкалоидов и других азотистых оснований из биологического материала
- •§ 3. Влияние состава извлекающих жидкостей на изолирование алкалоидов и других азотистых основании из биологического материала
- •§ 4. Влияние подкисленной воды и подкисленного спирта на извлечение примесей, переходящих в вытяжки из биологического материала
- •§ 5. Очистка вытяжек из биологического материала от примесей
- •§ 6. Экстракция алкалоидов и других токсических веществ из вытяжек
- •§ 7. Обнаружение ядовитых веществ, изолируемых подкисленной водой или подкисленным этиловым спиртом
- •§ 8. Количественное определение токсических веществ, изолированных подкисленной водой или подкисленным спиртом
- •§ 9. Метод выделения токсических веществ, основанный на изолировании их этиловым спиртом подкисленным щавелевой кислотой
- •§ 10. Метод выделения токсических веществ, основанный на изолировании их водой, подкисленной щавелевой кислотой
- •§ 11. Метод выделения токсических веществ, основанный на изолировании их водой, подкисленной серной кислотой
- •§ 12. Барбитураты и методы их исследования
- •§ 13. Барбамил
- •§ 14. Барбитал
- •§ 15. Фенобарбитал
- •§ 16. Бутобарбитал
- •§ 17. Этаминал-натрий
- •8.Обнаружение этаминала-натрия по уф- и ик-спектрам.
- •§ 18. Бензонал
- •§ 19. Гексенал
- •§ 20. Производные ксантина
- •§ 21. Кофеин
- •§ 22. Теобромин
- •§ 23. Теофиллин
- •§ 24. Наркотин
- •§ 25. Меконовая кислота
- •§ 26. Меконин
- •§ 27. Ноксирон
- •§ 28. Салициловая кислота
- •§ 29. Антипирин
- •§ 30. Амидопирин
- •§ 31. Фенацетин
- •§ 32. Хинин
- •§ 33. Опий и омнопон
- •§ 34. Морфин
- •§ 35. Кодеин
- •§ 36. Папаверин
- •§ 37. Галантамин
- •§ 38. Анабазин
- •§ 39. Никотин
- •§ 40. Ареколин
- •§ 41. Кониин
- •§ 42. Атропин
- •§ 43. Скополамин
- •§ 44. Кокаин
- •§ 45. Стрихнин
- •§ 46. Бруцин
- •§ 47. Резерпин
- •§ 48. Пахикарпин
- •§ 49. Секуренин
- •§ 50. Эфедрин
- •§ 51. Аконитин
- •§ 52. Новокаин
- •§ 53. Дикаин
- •§ 54. Аминазин
- •§ 55. Дипразин
- •§ 56. Тизерцин
- •§ 57. Хлордиазепоксид
- •§ 58. Диазепам
- •§ 59. Нитразепам
- •§ 60. Оксазепам
- •§ 61. Апоморфин
- •§ 62. Дионин
- •§ 63. Промедол
- •Глава VI. Вещества, изолируемые из объектов минерализацией биологического материала
- •§ 1. Связывание «металлических ядов» биологическим материалом
- •§ 2. Методы минерализации органических веществ
- •§ 3. Сухое озоление и сплавление органических веществ
- •§ 4. Окислители, применяемые для минерализации органических веществ
- •§ 5. Отбор и подготовка проб биологического материала для минерализации
- •§ 6. Разрушение биологического материала азотной и серной кислотами
- •§ 7. Разрушение биологического материала хлорной, азотной и серной кислотами
- •§ 8. Разрушение биологического материала пергидролем и серной кислотой
- •§ 9. Дробный метод и систематический ход анализа «металлических ядов»
- •§ 10. Маскировка ионов в дробном анализе
- •§ 11. Реактивы, применяемые в дробном анализе «металлических ядов» для маскировки ионов
- •§ 12. Реакции, применяемые в химико-токсикологическом анализе для обнаружения ионов металлов
- •§ 13. Соединения бария
- •§ 14. Соединения свинца
- •§ 15. Соединения висмута
- •§ 16. Соединения кадмия
- •§ 17. Соединения марганца
- •§ 18. Соединения меди
- •§ 19. Соединения мышьяка
- •§ 20. Соединения серебра
- •§ 21. Соединения сурьмы
- •§ 22. Соединения таллия
- •§ 23. Соединения хрома
- •§ 24, Соединения цинка
- •§ 25. Соединения ртути
- •§ 26. Количественное определение «металлических ядов» в минерализатах
- •§ 27. Количественное определение ртути
- •§ 28. Экстракционно-фотоколориметрическое определение меди
- •Глава VII. Вещества, изолируемые из биологического материала настаиванием исследуемых объектов с водой
- •Минеральные кислоты и щелочи
- •§ 1. Серная кислота
- •§ 2. Азотная кислота
- •§ 3. Соляная кислота
- •§ 4. Гидроксид калия
- •§ 5. Гидроксид натрия
- •§ 6. Аммиак
- •§ 7. Нитриты
- •Глава VIII. Ядохимикаты и методы их химико-токсикологического анализа
- •§ 1. Классификация ядохимикатов
- •§ 2. Гексахлорциклогексан (гхцг)
- •§ 3. Гептахлор
- •§ 4. Фосфорсодержащие органические соединения и методы их анализа
- •§ 5. Хлорофос
- •§ 6. Карбофос
- •§ 7. Метафос
- •§ 8. Карбарил
- •§ 9. Гранозан
- •Глава IX. Вещества, определяемые непосредственно в биологическом материале
- •§ 1. Оксид углерода (II)
- •§ 2. Спектроскопический метод обнаружения оксида углерода (II) в крови
- •§ 3. Химические методы обнаружения оксида углерода (II) в крови
- •§ 4. Количественное определение оксида углерода (II) в крови
- •Приложение 1. Приготовление реактивов
- •Приложение 2. Приготовление хроматографических пластинок
- •Список рекомендуемой литературы
§ 5. Хлорофос
![]()
![]()
![]()
![]() Все
объявления
Все
объявления
ЯндексДирект
Дать объявление
Низкотемпературные камеры
низкотемпературные морозильники с температурным режимом -24С, -55С, -85С
Адрес и телефон· www.winecoolers.ru
![]()

Хлорофос (дилокс, диптерекс, рицифон, тувон, трихлорофон) — 0,0-диметил- (2, 2, 2-трихлор-1-оксиэтил)-фосфонат — принадлежит к широко применяемым в сельском хозяйстве фосфорорганическим соединениям(ФОС).
Хлорофос—белый кристаллический порошок(т. пл. 84 °С). Он растворяется вводе,бензоле,хлороформеи других органическихрастворителях, хуже — в парафиновыхуглеводородах.
Хлорофос медленно разлагается в кислой среде и более быстро — в щелочной. Он относительно быстро разлагается в разбавленных растворахна свету. При разложении хлорофоса в кислой среде образуетсяметиловый спирти О-метил-(2, 2, 2-трихлор-1-оксиэтил)-фосфорная кислота.
В щелочной среде при разложении хлорофоса образуется довольно токсичное соединение О,О-диметил-О-(2,2-дихлорвинил)-фосфат (ДДВФ):
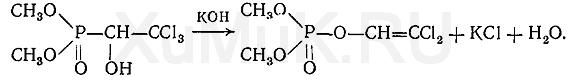
В растворахпродукты разложения хлорофоса подвергаются дальнейшим превращениям. Разрушение хлорофоса усиливается в присутствииокислителей, а такжежелеза. Поэтому этот препарат нельзя хранить в железной таре.
Технический хлорофос — это кристаллическая или пастообразная масса, содержащая около 80 % действующего вещества. При хранении кристаллизуется. Этот препарат выпускается в виде 80 %-го смачивающегопорошкаили в виде гранул. Он применяется как контактный или кишечныйинсектициддля обработки садов, виноградников, зерновых, бахчевых и др. 0,1— 0,3 %-йрастворхлорофоса применяется для борьбы с мухами,паразитамичеловека и животных, для обработки жилых помещений и т. д.
Хлорофос относится к ядохимикатам средней токсичности. Проявляет раздражающее действие накожу, понижаетактивностьхолинэстеразы в крови. Более выраженный холинэстераз-ный эффект имеет продукт разложения хлорофоса — ДДВФ. При хронических отравлениях хлорофосом наблюдается нарушение функции печени, заболевание сердечно-сосудистой системы и др.
Выделение хлорофоса из биологического материала. В колбу вместимостью 500 мл вносят 100 г измельченного биологического материала и 150 млводы, подкисленнойсерной кислотойдо рН = 2,0...2,5. Смесь оставляют на 2 ч, часто перемешивая, затем процеживают черезмарлю. К биоматериалу еще два раза прибавляютводу, подкисленную до рН = 2,0...2,5 (по 75 мл) и каждый раз настаивают по 1 ч, а затем сливают водные вытяжки.
Объединенные кислые водные вытяжки центрифугируют. Центрифугат переносят в делительную воронку, прибавляют 30 мл хлороформаи смесь взбалтывают 10 мин. Хлороформную вытяжку сливают. Хлорофос из кислой водной вытяжки еще 4 раза экстрагируютхлороформом(по 30 мл).
Хлороформные вытяжки соединяют и выпаривают при комнатной температуредосуха. Сухой остаток растворяют в 5 млводы, затемрастворфильтруют через бумажный фильтр. Фильтрат используют для обнаружения хлорофоса.
Обнаружение хлорофоса
Для обнаружения хлорофоса применяют цветные реакции, холинэстеразную пробу и метод хроматографии.
Реакция с пиридином и щелочью (реакция Фудживара).В пробирку вносят 1 мл исследуемогораствора, 1 млпиридинаи 1 мл 30 %-горастворагидроксида натрия. Смесь нагревают на кипящей водяной бане 5 мин. При наличии хлорофоса в пробе появляется красная или розовая окраска. Предел обнаружения: 10 мкг хлорофоса.
Эту реакцию даеттакже ряд хлорсодержащихсоединений алифатическогоряда (см. гл. IV, § 14).
Реакция с резорцином.В пробирку вносят 1 мл исследуемогораствора, 2 капли 1 %-горастворарезорцинав 20 %-мрастворекарбоната натрияили 1 %-мрастворегидроксида натрия. Через 10 мин появляется розовая окраска, а через 15—30 мин наблюдается желто-зеленаяфлуоресценцияраствора. Окраска ифлуоресценциярастворадостигают максимума через 1—2 ч после прибавления реактивов к исследуемомураствору. Через 4—6 часов розовая окраска переходит в оранжевую, а затем в желтую.Флуоресценциярастворасохраняется в течение нескольких суток. Предел обнаружения: 40 мкг хлорофоса в пробе.
Для обеспечения возможности протекания реакции рН должно равняться 9—11.
Реакция образования изонитрила.В пробирку вносят 0,01— 0,03 г исследуемоговеществаи 1 млэтилового спирта. Смесь взбалтывают, затем прибавляют 2 мл 10 %-го спиртовогорастворагидроксида натрияи 1 каплюанилина. При нагревании смеси ощущается характерный запахизонитрила.
Реакция неспецифична. Ее даютхлороформ, ДДВФ и некоторые другие хлорсодержащиевещества.
Реакция с о -толидином. В фарфоровую чашкувносят 0,2— 0,5 мл водного или спиртовогораствораисследуемоговещества, 1 мл 0,5 %-горастворао -толидина вацетонеи 1 мл смесирастворовпероксида водородаигидроксида натрия. В присутствии хлорофоса появляется желтая или оранжевая окраска.
Эту реакцию даютметафос, тиофос и др.
Приготовление смеси пероксида водорода и щелочи (см. Приложение 1, реактив 71).
Реакция с 2,4-динитрофенилгидразином. В пробирку вносят 1—10 капель исследуемогораствораи 2 капли 1 н.растворагидроксида натрия. Через 20 мин прибавляют 1 каплю 0,1 %-гораствора2,4-динитрофенилгидразина в 4 н.растворесоляной кислоты. Пробирку выдерживают в кипящей водяной бане 30 мин. После этого смесь охлаждают, прибавляют 1 каплю 4 н.растворагидроксида натрияи 0,5 млэтилового спирта. При наличии хлорофоса в пробе появляется синяя или сине-фиолетовая окраска.
Эту реакцию даютДДВФ, тиофос и др.
Реакция с ацетоном. В пробирку вносят 0,1—0,5 млраствораисследуемоговеществавэтиловом спирте, прибавляют 1 млацетонаи 0,5 мл 0,5 н. спиртовогорастворагидроксида натрия. При наличии хлорофоса в пробе через 5—15 мин появляется розовая окраска, переходящая в оранжевую.
Холинэстеразная проба. Хлорофос понижает активностьацетилхолинэстеразы, которая теряет способность разлагатьацетилхолин. Выполнение этой пробы описано выше (см. гл. VIII, § 4).
Обнаружение хлорофоса методом хроматографии. На пластинку, покрытую тонким слоемсиликагеляКСК, закрепленнымгипсом, наносят каплю спиртовогораствораисследуемоговеществаи каплюраствора«свидетеля». Пятна подсушивают навоздухе. Затем пластинку вносят в камеру, насыщеннуюпарамисистемырастворителей(смесь равных объемов н -гексана и ацетона). После того как системарастворителейподнимется на пластинке на 10 см вышелиниистарта, пластинку вынимают из камеры, подсушивают навоздухеи опрыскивают смесью 2 %-го водногорастворарезорцинаи 10 %-горастворакарбоната натрия, взятых в соотношении 2 : 3. Подсушенную пластинку нагревают 7—10 мин в сушильном шкафу при 100 °С. При этом пятна на пластинке приобретают оранжевую окраску.
