
- •Міністерство освіти науки
- •Лабораторна робота №1 здобування кислот, гідроксидів та солей
- •1.1 Загальні відомості
- •1.1.1 Здобування та властивості оксидів
- •1.1.2 Здобування та властивості гідроксидів
- •1.1.3 Здобування та властивості кислот
- •1.1.4 Здобування та властивості солей
- •1.2 Завдання для самостійного розв’язання:
- •1.3 Обладнання та реактиви
- •1.4 Вказівки до техніки безпеки
- •1.5 Порядок проведення лабораторної роботи
- •Лабораторна робота №2 визначення еквівалента металу
- •2.1 Загальні відомості
- •2.1.1 Взаємозв'язок між основними фізичними величинами, що використовуються в хімії
- •2.2 Завдання для самостійного розв’язання
- •2.2.1 Розв’язати задачі
- •2.2.2 Визначити дані (?) для запропонованого варіанту
- •2.3 Обладнання та реактиви
- •2.4 Вказівки до техніки безпеки
- •2.5 Порядок проведення лабораторної роботи
- •Лабораторна робота № 3 окисно-відновні реакції
- •3.1 Загальні відомості
- •3.1.1 Окислення і відновлення. Класифікація окисно-відновних реакцій.
- •3.1.2 Метод електронного балансу
- •3.2 Завдання для самостійного розв’язання
- •3.2.1 Відповісти на запитання та виконати завдання
- •3.3 Реактиви та обладнання
- •3.4 Вказівки до техніки безпеки
- •3.5 Порядок проведення лабораторної роботи
- •Лабораторна робота №4 закономірності перебігу хімічних процесів
- •4.1. Загальні відомості
- •4.1.1. Енергетика хімічних процесів.
- •4.1.2. Основи хімічної кінетики
- •4.1.3. Хімічна рівновага
- •4.2. Завдання для самостійного розв’язання
- •4.2.1. Відповісти на запитання
- •4.2.2. Розв’язати задачі
- •4.3. Реактиви та обладнання
- •4.4. Вказівки до техніки безпеки
- •4.5 Порядок проведення лабораторної роботи
- •Лабораторна робота № 5 розчини
- •5.1 Загальні відомості
- •5.1.1. Загальна характеристика розчинів
- •5.1.2. Розчини електролітів
- •5.2 Завдання для самостійного розв'язання
- •5.2.1. Відповісти на запитання, виконати завдання
- •5.3 Реактиви та обладнання
- •5.4 Вказівки до техніки безпеки
- •5.5 Порядок проведення лабораторної роботи
- •Лабораторна робота №6 гальванічні елементи та електроліз
- •6.1 Загальні відомості
- •6.1.1 Електродні потенціали. Гальванічні елементи.
- •6.1.2 Електроліз
- •6.2 Завдання для самостійного розв’язання
- •6.3 Прилади та реактиви
- •6.4 Вказівки з техніки безпеки
- •6.5 Порядок проведення лабораторної роботи
- •Лабораторна робота №7 корозія та захист металів
- •7.1. Загальні відомості
- •7.2. Завдання для самостійного розв’язання
- •7.3. Реактиви та обладнання
- •7.4. Вказівки до техніки безпеки
- •7.5. Порядок виконання роботи
- •Загальна характеристика металів та їх сполук
- •8.1. Загальні відомості
- •8.2. Завдання для самостійного розв’язання
- •8.3. Реактиви та обладнання
- •8.4. Вказівки щодо техніки безпеки
- •8.5. Порядок виконання лабораторної роботи
- •Легкі конструкційні матеріали та їх властивості
- •9.1 Загальні відомості
- •9.2 Завдання для самостійного розв’язання
- •9.3 Вказівки до техніки безпеки
- •9.4 Реактиви та обладнання
- •9.5 Порядок проведення лабораторної роботи
- •Література
- •Додаток б Стандартні термодинамічні величини речовин
- •Додаток в Стандартні електродні потенціали е0 в при 250с
- •Додаток г Розчинність кислот, основ та солей у воді
Легкі конструкційні матеріали та їх властивості
Мета роборти:ознайомитися із методами добування, властивостями металів та іх сполук магнію, алюмінію, титану.
9.1 Загальні відомості
9.1.1 Деякі властивості металів
|
|
Вале-нтні елек-трони |
Е˚, В |
Гус-тина, г/см³ |
Tпл.,˚С |
Вміст в земній корі, % |
Харак-терні ступені окисне-ння |
Природні сполуки |
|
Магній |
2S² |
-2,36 |
1,74 |
650 |
1,87 |
0, +2 |
MgCl2, KCl, CaCO3, MgCO3 |
|
Алюмі-ній |
3S²3р |
-1,62 |
2,7 |
660 |
7,57 |
0, +3 |
Al2O3, Na3AlF3 |
|
Титан
|
4S²3d² |
-1,28 |
4,49 |
167065·10ˉ2 |
|
0, +2, +3, +4 |
TiO2, FeTiO3, CaTiO3 |
Сріблясто-білі, легкі, пластичні метали, стійкі до атмосферної корозії. Магній, алюміній, титан здатні утворювати сплави з цінними властивостями:: легкі, тверді, міцні, пластичні, хімічно стійкі, мало кородують. Сплави застосовують в авіа-, ракето-, судобудуванні, громадському будівництві, військовій справі, транспортному машинобудуванні. Сплави магнію, алюмінію, титану займають перше місце по використанню їх як легких конструкційних матеріалів.
Найважливіші сплави:
Mg-Al-Zn; дюралюмінійAl-Cu (4%) → по 0,5%Mg, Mn, Fe, Si(міцність цьому сплаву надають інтерметалічні сполуки, наприкладAl2Cu).
Збільшення кількості магнію до 5-10% підвищує корозійну стійкість сплаву, механічні властивості, жаростійкість.
9.1.2 Здобування
1) Електрометалургійний спосіб – електроліз розплавів солей
катод: Mg²+2eˉ→Mg˚
Al³+3eˉ→Al˚
2) Металотермічний спосіб здобування титану
TiO2+2Cl2+2C→TiCl4+2CO
TiCl4+2Mg→Ti+2MgCl2
9.1.3 Хімічні властивості:
в ряду Mg-Al-Тізменьшується хімічна активність металів.
реагують з неметалами:
2Mg+O2→2MgO; магній оксид
2Al+3Cl2→2AlCl3; алюміній хлорид
2Ti+N2→2TiN; титан(III) нітрид.
при нагріванні реакційна здатність збільшується.
з водою при нагріванні:
Mg+2H2O→Mg(OH)2+H2
2Al(Hg)+6H2O→2Al(OH)3+3H2; Al(Нg)- амальгама;
Ti+2H2O→TiO2+2H2
розчиняються в кислотах
Mg0+2H+→Mg²++H20
10Al+36HNO3=10Al(NO3)3+3N2+18H2O
2Ti+12HF=2H3[TiF6]+3H2
Оксиди та гідроксиди магнію мають основний характер властивостей, алюмінію-амфотерний; сполуки титану ІІІ – мають більше основні властивості; титану ІV – амфотерні
Mg → MgO → Mg(OH)2
основний оксид основа
Al → Al2О3 → Al(OH)3
амфотерний оксидН[Al(OH)4]
амфотерний гідроксид
Т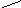 іО2
→ Ті(ОН)4– амфотерний
гідроксид
іО2
→ Ті(ОН)4– амфотерний
гідроксид
Ті
Т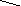 і(ОН)3
→ ТіС13
і(ОН)3
→ ТіС13
Сполуки титану(ІІІ) – сильні відновники
Ті³ + -1еˉ→ Ті4+
9.2 Завдання для самостійного розв’язання
9.2.1 Виконати завдання
1. Порівняти будову атомів, металічні властивості, хімічну активність металів магнію, алюмінію, титану
2. Скласти рівняння реакцій в молекулярному, йонному, електронному видах для здійснення перетворень по схемі, назвати речовини
а) Mg→MgCl2→Mg(OH)2→MgBr2→Mg→Mg(NO3)2
б) Al→AlN→Al(OH)3→Al2O3→KAlO2→Al(NO3)3
3. При прожарюванні металічного титану на повітрі утворюється білий порошок титан (ІV) оксиду, який розчиняється в концентрованій сульфатній кислоті і сплавляється з лугами. Скласти рівняння реакцій: а) прожарювання титану на повітрі; б) розчинення титан (ІV) оксиду в сульфатній кислоті; в) сплавлення титан (ІV) оксиду з лугом.
9.2.2 Розв’язати задачі
1. Чи можливо алюмотермічним способом добути залізо з ферум (ІІІ) оксиду при температурі 1500К? Відповідь обгрунтувати розрахунком енергії Гіббса за даної температури.
2. Титан (ІІІ) гідроксид відновлює нітрати до амоніаку. Скласти рівняння реакції в молекулярному та електронному видах взаємодії титан (ІІІ) гідроксиду з натрій нітратом в лужному середовиші. Розрахувати об’єм амоніаку (н.у.), який виділяється, якщо в реакцію вступає 0,1 моль Ті(ОН)3.
(0,28 л)
3. Вивести молекулярну формулу інтерметалічної сполуки магнію з цинком, яка відноситься до бертолідів і містить 42,48% магнію.
