
- •1 Основні поняття і закони хімії Теоретична частина
- •Лабораторна робота № 1 Визначення молекулярної маси газу
- •Виконання досліду
- •Обробка результатів досліду
- •Лабораторна робота № 2 Визначення молекулярної маси еквівалентів металу
- •Виконання досліду
- •Обробка результатів досліду
- •Контрольні запитанная
- •2 Енергетика хімічних реакцій Теоретична частина
- •Лабораторна робота № 3 Визначення теплоти хімічної реакції
- •Виконання досліду
- •Контрольні запитання
- •3 Хімічна кінетика та хімічна рівновага Теоретична частина
- •3.1 Швидкість хімічної реакції
- •3.2 Кінетика оборотних реакцій
- •Фактори, які впливають на зміщення рівноваги.
- •Лабораторна робота 4 Хімічна кінетика і хімічна рівновага
- •Виконання дослідів.
- •Контрольні запитання
- •4 Розчини
- •4.1 Гідроліз розчинів солей Теоретична частина
- •Лабораторна робота 5 Гідроліз солей
- •Виконання досліду
- •Контрольні запитання
- •4.2 Концентрація розчинів Теоретична частина
- •Лабораторна робота № 6 Готування розчину заданої концентрації з навішення твердої речовини
- •Виконання досліду
- •Контрольні запитання
- •5 Твердість води та методи ії усунення Теоретична частина
- •Методи усунення твердості води
- •Лабораторна робота № 7 Визначення твердості води за допомогою Трилону б
- •Виконання досліду
- •Контрольні запитання
- •6 Окисно-відновні реакції Теоретична частина
- •Лабораторна робота № 8 Окисно-відновні реакції
- •Виконання досліду
- •Контрольні запитання
- •7 Хімічні джерела струму Теоретична частина
- •Лабораторна робота № 9 Хімічні джерела струму (гальванічні елементи)
- •Виконання дослідів
- •Контрольні запитання
- •8 Корозія металів Теоретична частина
- •8.1 Захист металів і сплавів від корозії
- •Легування
- •Захисні покриття
- •Електрохімічний захист
- •Зміна властивостей корозійного середовища
- •Раціональне конструювання
- •Лабораторна робота № 10 Корозія металів. Методи захисту металів від корозії
- •Виконання дослідів
- •Контрольні запитання
- •9 Електроліз Теоретична частина
- •Лабораторна робота №11 Електроліз
- •Контрольні запитання
- •Методичні вказівки
Контрольні запитання
Дайте визначення окисно-відновним реакціям.
Що в окисно-відновник реакціях є окисником та відновником?
Назвіть типи окисно-відновник реакцій.
Методом електронного балансу підберіть коефіцієнти в схемах окисно-відновних реакцій:
KClO3 + KI + H2SO4 → KCl + I2 + K2SO4 + H2O
KMnO4 + NO + H2O → MnO2 + NO2 + KOH
K2Cr2O7 + (NH4)2S + H2O → Cr(OH)3 + S + NH3 + KOH
Bi2S3 + HNO3 → Bi(NO3)3 + NO + S + H2O
7 Хімічні джерела струму Теоретична частина
Хімічні джерела струму (ХДС) – це такі пристрої, в яких при протіканні хімічних реакцій утворюється струм. Ці пристрої бувають 3-х типів: одноразової дії, багатократної дії, безперервної дії.
В результаті взаємодії метал-розчин електроліту, метал набуває електричний заряд; на межі виникає подвійний електричний шар і виникає різниця ел. потенціалів.
|
|
|
(7.1) |
![]() рівноважний
електродний потенціал;
рівноважний
електродний потенціал;
![]() стандартний
електродний потенціал;
стандартний
електродний потенціал;
R
– газова постійна; R=8,31![]()
Т – температура по Кельвіну;
n – ступінь окислення металу (електрони);
F – число Фарадея; F=96500 кл.
Катод – електрод, на якому відбувається процес відновлення.
Анод – електрод, на якому відбувається процес окислення.
|
|
|
(7.2) |
![]() эл.
потенціал катода.
эл.
потенціал катода.
![]() эл.
потенціал анода.
эл.
потенціал анода.
Лабораторна робота № 9 Хімічні джерела струму (гальванічні елементи)
Правила техніки безпеки: дотримуватися загальних правил безпеки при роботі в хімічних лабораторіях.
Необхідні прилади і реактиви: 2 стаканчика, цинкова пластинка, мідна пластинка, електролітичний місток, гальванометр, 1М розчини сульфату цинку та сульфату міді, 0,01М розчин сульфату цинку.
Виконання дослідів
Дослід1. Складання мідно-цинкового гальванічного елементу
Занурити цинкову пластинку в стаканчик з 1М раствором сульфату цинку, а мідну пластинку в стаканчик з 1М розчином сульфату міді. З'єднати розчини електролітним містком, а до пластинок підключити гальванометр. Спостерігати відхилення стрілки гальванометра, яке обумовлене виникненням електричного струму унаслідок різних значень стандартних електродных потенціалів електродів.
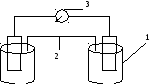 Zn
(анод)
Cu
(катод)
Zn
(анод)
Cu
(катод)
ZnSO4 CuSO4
1–микростаканчики; 2 – електролитичний місток;
3 – гальванометр.
Рисунок 7.1 – Схема гальванічного елементу
Зміряти е.д.с. гальванічного елементу. Розімкнути ланцюг.
Скласти схему гальванічного елементу. Зробити малюнок приладу. Написати рівняння хімічних реакцій, що протікають на електродах, і сумарне рівняння хімічної реакції, в результаті якої виникає електричний струм. Порівняти теоретичне значення е.д.с. гальванічного елементу з практичним. Пояснити причину відмінності цих значень.
Дослід 2. Складання концентраційного гальванічного елементу.
Наповнити стаканчики розчинами сульфату цинку різної концентрації: перший – розчином концентрації 1 моль/л, другий- 0,01моль/л. З'єднати стаканчики електролітним містком. Занурити в кожен стаканчик цинкові електроди і з'єднати їх дротом з гальванометром.
Чи відхиляється стрілка гальванометра?
Користуючись таблицею 7.1 Стандартних електродних потенціалів і рівнянням Нернста, обчислити потенціал кожного електроду.
Таблиця 7.1 - Стандартні потенциали металевих електродів
|
Электрод |
Электродна реакція |
E0, B |
|
Li+/Li |
Li+ + e = Li |
-3,045 |
|
Rb+/Rb |
Rb+ + e = Rb |
-2,925 |
|
K+/K |
K+ + e = K |
-2,925 |
|
Cs+/Cs |
Cs+ + e = Cs |
-2,923 |
|
Ba2+/Ba |
Ba2+ + 2e = Ba |
-2,906 |
|
Ca2+/Ca |
Ca2+ + 2e = Ca |
-2,866 |
|
Na+/Na
|
Na+ + e = Na |
-2,714
|
|
Mg2+/Mg
|
Mg2+ + 2e = Mg
|
-2,363
|
|
Be2+/Be
|
Be2+ + 2e = Be
|
-1,847
|
|
Al3+/Al
|
A13+ + 3e = Al
|
-1,662
|
|
Ti2+/Ti
|
Ti2++2e=Ti
|
-1,628
|
|
V2+/V
|
V2++2e=V
|
-1,186
|
|
Mn2+/Mn
|
Mn2++2e=Mn
|
-1,180
|
|
Cr2+/Cr
|
Cr2+ + 2e = Cr
|
-0,913
|
|
Zn2+/Zn
|
Zn2++2e=Zn
|
-0,763
|
|
Cr3+/Cr
|
Cr3++3e=Cr
|
-0,744
|
|
Fe2+/Fe
|
Fe2+ + 2e = Fe
|
-0,440
|
|
Cd2+/Cd
|
Cd2++2e=Cd
|
-0,403
|
|
Co2+/Co
|
Co2+ + 2e = Co
|
-0,277
|
|
Ni2+/Ni
|
Ni2++2e=Ni
|
-0,250
|
Продовження таблиці 7.1
|
Электрод |
Электродна реакція |
E0, B |
|
Sn2+/Sn
|
Sn2+ + 2e = Sn
|
-0,136
|
|
Pb2+/Pb
|
Pb2++2e=Pb
|
-0,126
|
|
Fe3+/Fe
|
Fe3++3e=Fe
|
-0,036
|
|
H+/H2
|
H+ + e = ½H2
|
+0,000
|
|
Cu2+/Cu
|
Cu2++2e=Cu
|
+0,337
|
|
Cu+/Cu
|
Cu++e=Cu
|
+0,521
|
|
Ag+/Ag
|
Ag++e=Ag
|
+0,799
|
|
Hg2+/Hg
|
Hg2++2e=Hg
|
+0,854
|
|
Pd2+/Pd
|
Pd2+ + 2e= Pd
|
+0,987
|
|
Pt2+/Pt
|
Pt2+ + 2e = Pt
|
+1,190
|
|
Au3+/Au
|
Au3+ + 3e = Au
|
+1,498
|
|
Au+/Au
|
Au++e=Au
|
+1,691
|
