
- •ЗДРАВСТВУЙТЕ!
- •Лекция 13. РАСПРЕДЕЛЕНИЕ ГАЗОВЫХ МОЛЕКУЛ ПО СКОРОСТЯМ И ЭНЕРГИЯМ
- •1. Скорости газовых молекул. Опыт Штерна.
- •Экспериментально впервые скорости молекул были измерены в 1920 г. Штерном. За этот опыт
- •2. Вероятность события. Понятие о распределении молекул газа по скоростям
- •Например: на переписи населения, когда указывается возраст (20 лет) – это не значит,
- •Мы будем искать число частиц (∆n), скорости которых лежат в определённом интервале значения
- •Итак:
- •молекулы газа в единице объёма иметь скорость, заключённую в единичном интервале, включающем заданную
- •А1 – постоянная равная
- •Очевидно, что и dny
- •Если собрать вместе все молекулы в единице объёма, скорости которых
- •Объём этого шарового слоя
- •Отсюда следует закон Максвелла –
- •Приdυ 1 получаем плотность вероятности, или функцию распределения
- •Из графика видно, что при «малых» υ, т.е. при
- •Наиболее вероятная, средне квадратичная и средняя арифметическая скорости молекул газа
- •Скорость, соответствующая максимуму распределения есть наиболее вероятная скорость (рис. 13.7). Величину
- •Среднюю квадратичную скорость найдем используя соотношение
- •Средняя арифметическая скорость υср
- •Полезно знать, что
- •Опыта Штерна
- •В 1920 году физиком Отто Штерном (1888-1969) впервые были экспериментально определены скорости частиц
- •В стенке внутреннего цилиндра была сделана узкая продольная щель, через которую проникали движущиеся
- •Цилиндры начинали вращать с постоянной угловой скоростью. Теперь атомы, прошедшие сквозь прорезь, оседали
- •Зная величины радиусов цилиндров, скорость их вращения и величину смещения легко найти скорость
- •Зависимость функции распределения Максвелла от массы и температуры газа
- •Формула Максвелла для относительных скоростей
Итак: |
|
∆n=nf(υ)∆υ |
(13.6) |
или перейдя к пределу |
|
dn=nf(υ)dυ, |
(13.7) |
где f(υ) – функция распределения. |
|
Трудность вычисления (13.7) – в |
нахождении |
именно f(υ). Физический смысл f(υ) в том, что это отношение числа молекул, скорости которых лежат в определенном интервале скоростей, к общему числу молекул в единичном интервале скоростей: dv = 1, т.е.
f (υ) dn |
|
n |
(13.8) |
|
Таким образом, f(υ) – имеет смысл вероятности. То есть f(υ) показывает, какова вероятность любой

молекулы газа в единице объёма иметь скорость, заключённую в единичном интервале, включающем заданную скорость υ. В этом случае f(υ) называют плотностью вероятности.
3. Функция распределения Максвелла
Мы воспользуемся результатами этого вывода. Скорость – векторная величина. Для x-ой составляющей скорости dnx= nf(υx)dυx, тогда
|
dn |
|
|
1 |
m |
1 |
|
mυx |
|
mυx |
(13.8) |
|||
|
|
|
2 |
|||||||||||
f (υx ) |
|
x |
|
|
|
|
|
|
e 2kT |
A1e 2kT , |
|
|||
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|||||||||
|
ndυx |
|
π |
2kT |
|
|
|
|
|
|||||

А1 – постоянная равная |
|||||||
|
1 |
1 |
|
||||
|
m 2 |
. |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|||||
|
|
π |
2kT |
|
|||
Графическое изображение функции показано на рис 13.1. Видно, что доля молекул со скоростью υх =
0 не равна нулю.
Рис 13.1
При υх = 0, f(υх=0) = А1 (в этом физический смысл
постоянной А). Приведённое выражение описывает распределение молекул газа по x-ым компонентам скорости.
Очевидно, что и dny |
|
|
mυ2y |
|
dn |
|
|
|
mυz2 |
||
A e |
2kT |
и |
z |
A e |
2kT . |
||||||
|
|
|
|
|
|||||||
|
|
|
|
|
|
||||||
|
ndυy |
1 |
|
|
|
ndυz |
1 |
|
|
||
|
|
|
|
|
|
|
|
||||
Вероятность того, что скорость молекулы одновременно удовлетворяет трём условиям: x – компонента скорости лежит в интервале от υх до υх + dυх; y – компонента, в интервале
от υy до υy + dυy; z – компонента, в интервале от υz до υz + dυz будет равна произведению
вероятностей каждого из условий (событий) в отдельности!
|
dnxyz |
A3e |
m xyz2 |
dυ |
dυ |
|
dυ |
|
, |
|
То есть |
2kT |
y |
z |
|||||||
|
||||||||||
|
n |
1 |
|
x |
|
|
(13.9) |
|||
|
|
|
|
|
|
|
|
|||
Этой формуле можно |
дать |
геометрическое |
||||||||
истолкование: dnxyz – это число молекул в паралле- лепипеде со сторонами dυx, dυy, dυz, то есть в объёме dV = dυxdυydυz, находящемся на расстоянии v от начала координат в пространстве скоростей. Эта величина (dnxyz)
не может зависеть от направления вектора скорости. Поэтому надо получить функцию распределения молекул по скоростям независимо от их направления, то есть по абсолютному значению скорости.

Если собрать вместе все молекулы в единице объёма, скорости которых
|
заключены в интервале |
|
от υ до υ+dυ (рис. 13.2) |
|
по всем направлениям, |
Рис 13.2 |
и выпустить их, |
|
то они окажутся через одну секунду в шаровом слое толщиной dυ и радиусом υ. Этот шаровой слой складывается из тех параллелепипедов, о которых говориться выше.
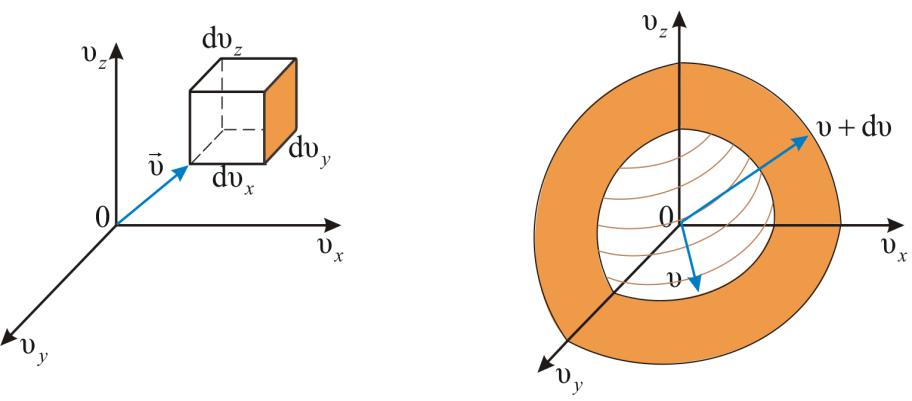
Рис 13.3

Рис. 13.4 |
Рис. 13.5 |

Объём этого шарового слоя
d = 4 2d , |
(13.10) |
тогда общее число молекул в слое
|
n |
|
m |
|
3/ 2 |
mυ2 |
|
dn |
|
e 2kT dΩ. |
|
||||
|
|
|
|
|
(13.11) |
||
π3/ 2 |
|
|
|||||
|
|
2kT |
|
|
|
||
Отсюда следует закон Максвелла –
распределение молекул по абсолютным значениям скоростей:
dn |
|
4 |
m 3/ 2 |
mυ2 |
υ |
2 |
dυ, |
(2.3.3) |
||||||
n |
|
|
|
|
|
|
|
|
e |
2kT |
|
|
||
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
||||||||||
|
|
π 2kT |
|
|
|
|
|
|
||||||
|
dn |
|
– доля всех частиц единичного |
|||||||||||
|
где |
|
||||||||||||
|
n |
|
|
|
|
|
|
|
|
|
|
|
|
|
объёма, скорости которых лежат в интервале |
||||||||||||||
|
|
υ dυ. |
от υ до |
|
|
|
|
|
||||||
