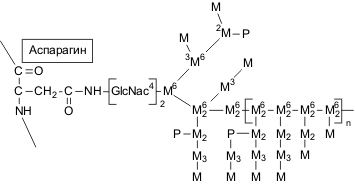Маннаны
Маннаны – класс природных гомо- и гетерополисахаридов, в состав макромолекул которых входят звенья остатков D-маннозы.
Распространение в природе
Маннаны встречаются в высших (древесина хвойных пород, 10 – 12% от веса сухой массы) и низших растениях, водорослях, микроорганизмах (грибах, дрожжах (Hansenula holstii) и др.), выполняя функции структурных и резервных полисахаридов. Подобно целлюлозе маннаны в качестве структурных полисахаридов входят в состав клеточных стенок, участвуют в построении защитных оболочек плодов и семян (например, семян бобовых, скорлупы орехов и др.). Некоторые маннаны запасаются в клеточных стенках эндосперма в качестве углеводного энергетического резерва, например, в клетках однодольных растений (луковицы лилиецветных, клубни орхидных, ирисовых и др.). Дрожжи Hansenula holstii во время роста на углеводном субстрате выделяют водорастворимый маннан, частично (на 20%) этерифицированный фосфорной кислотой.
Структура и свойства
Маннаны характеризуются большим разнообразием структур, физико-химических свойств и биологических функций. Они бывают линейного и разветвленного строения. Способны удерживать значительное количество воды и, благодаря этому, служат регулятором водного баланса семян при прорастании. Известно, что маннаны не токсичны, некоторые проявляют антикоагуляционную активность.
Представители
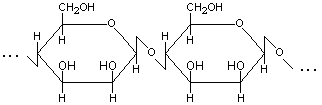
1. Маннан – линейный гомополисахарид, макромолекулы которого построены из остатков -D-маннопиранозы, связанных -(1→4)-гликозидными связями (рис.1).
|
|
|
Рис.1. Структурная формула макромолекулы маннана. |
Маннан входит в состав гемицеллюлолоз клеточных стенок некоторых высших растений (оболочки плодов и семян), водорослей и др.
Маннан не растворяется в воде при
комнатной температуре. При нагревании
(Т = 60 - 70)
можно получить 1%-ный водный раствор
полисахарида. При прогревании этого
раствора при Т = 60 - 70
в течение трех дней маннан кристаллизуется.
Кристаллы маннана можно получить и
кристаллизацией из других сред, например,
из смеси диметиламин+диметилсульфоксид+NaOH
(25+70+5). Кристаллы маннана имеют форму
палочек и являются оптически активными.
Величины удельного оптического вращения
растворов кристаллического маннана в
6%-ном NaOH следующие: для
маннана, выделенного из каменного ореха,
![]() = – 46
град., для маннана, полученного из
древесины сосны,
= – 46
град., для маннана, полученного из
древесины сосны,
![]() = – 41
град.
= – 41
град.
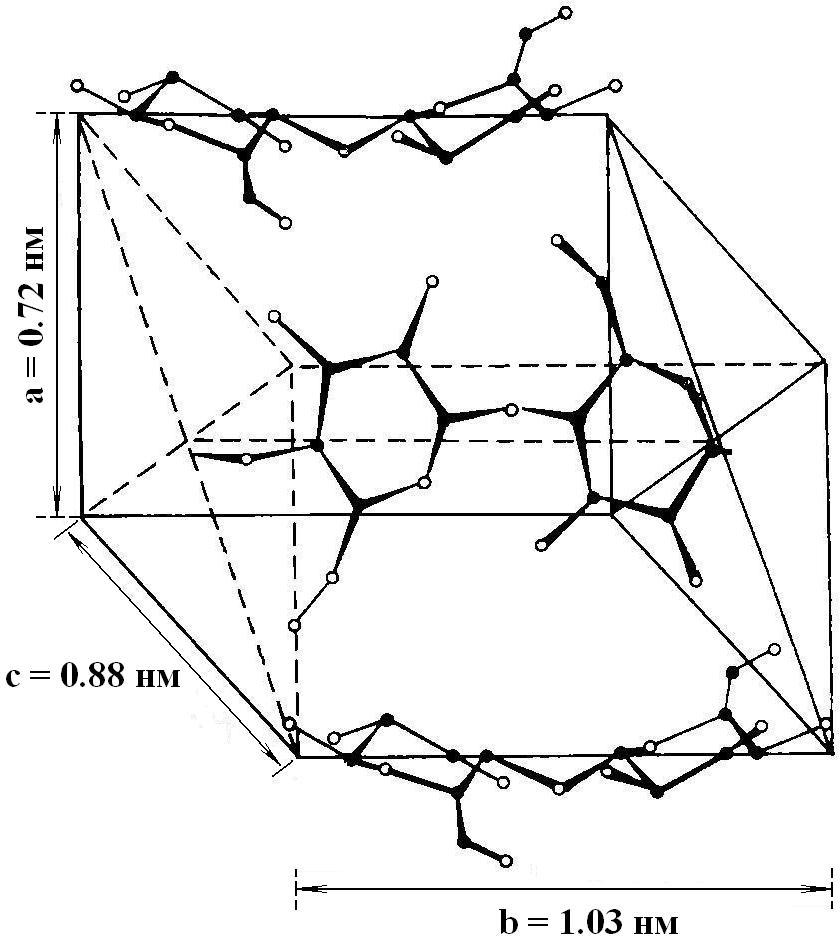
Кристаллиты маннана в поле зрения электронного микроскопа представляют собой пластинчатые многослойные кристаллы толщиной ~100Å. Элементарная ячейка пространственно-структурной организации кристалла маннана приведена на рис.2.
|
|
|
Рис.2. Схематическое изображение элементарной ячейки кристалла маннана. |
Маннан – полиморфный полисахарид, поэтому в выделяемых образцах полимера присутствуют и кристаллическая и аморфная фазы.
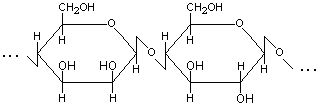
2. Глюкоманнан – линейный гетерополисахарид, макромолекулы которого построены из звеньев -D-маннопиранозы и -D-глюкопиранозы, связанных -(1→4)-гликозидными связями (рис.3).
|
|
|
Рис.3. Структурная формула макромолекулы глюкоманнана. |
Некоторые гидроксильные группы содержат ацетильные остатки. Растворяется в воде, благодаря чему глюкоманнан часто относят к группе растительных слизей. Глюкоманнан встречается в природе как компонент гемицеллюлоз древесины.
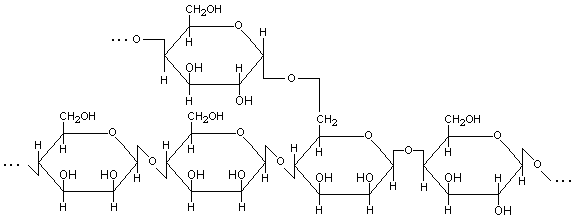
3. Галактоманнан – разветвленный гетерополисахарид. Основная линейная цепь построена главным образом из звеньев остатков -D-маннопиранозы, но встречаются также и звенья остатков -D-галактопиранозы, связанных -(1→4)- и -(1→6)-гликозидными связями. К линейной цепи -(1→6)-гликозидными связями присоединены боковые цепи из звеньев остатков -D-галактопиранозы, связанных -(1→4)-гликозидными связями (рис.4).
|
|
|
Рис.4. Предположительная структурная формула макромолекулы галактоманнана. |
Некоторые галактоманнаны могут быть построены из фрагментов -D-маннопиранозы и -D-галактопиранозы, соединенных -(1→6)-гликозидными связями. Такие галактоманнаны, как правило, имеют сильно разветвленное строение. Боковые цепи присоединены в положение С2 остатков маннозы и положение С2 и С4 остатков галактозы.
Сульфатированные галактоманнаны обладают антикоагуляционной активностью. Они увеличивают тромбиновое время и снижают функциональную активность тромбоцитов.
4. Галактоглюкоманнан – разветвленный гетерополисахарид. Макромолекулы основной цепи построены из звеньев -D-маннопиранозы и -D-глюкопиранозы, связанных -(1→4)-гликозидными связями (рис.5). Соотношение звеньев остатков -D-маннопиранозы и -D-глюкопиранозы у разных образцов варьирует в широких пределах. К линейной цепи -(1→6)-гликозидными связями присоединены остатки -D-галактопиранозы. Звенья остатков -D-галактопиранозы в боковых цепях соединены преимущественно -(1→4)-гликозидными связями, но могут встречаться и -(1→4)-гликозидные связи (рис.5). Соотношение между остатками трех моносахаридов в галактоглюкоманнанах может варьировать в широких пределах.
Галактоглюкоманнаны встречаются в природе в качестве компонентов гемицеллюлоз хвойной и лиственной древесины, а также в качестве резервных веществ семян бобовых.
|
|
|
Рис.5. Предположительная структурная формула макромолекулы галактоглюкоманнана. |
Галактоглюкоманнаны семян бобовых, в частности, гуаран (гуаровая камедь) из измельченного эндосперма семян гуара [Cyamofsis tetragonoloba (guar gum)] семейства бобовых (семена содержат до 70% камеди) или полисахарид цареградских рожков [Ceratonia siliqua (locust bean gum)], производят в промышленных масштабах и широко используют в качестве загустителей и стабилизаторов суспензий и эмульсий, в первую очередь в пищевой, бумажной, текстильной и нефтедобывающей промышленности. Например, мировое производствово гуарана составляет 60 000 - 90 000 т/год.
5. Маннопротеины – сложные углевод-белковые комплексы. Полисахаридный фрагмент маннопротеина имеет разветвленное строение. Основная линейная цепь построена из остатков -D-маннопиранозы и -D-галактопиранозы, связанных -(1→6)-гликозидными связями. Степень полимеризации основной цепи n ~ 350. Многочисленные боковые ответвления представлены короткими олигосахаридными цепочками из звеньев -D-маннопиранозы, -D-глюкопиранозы или -D-галактопиранозы, связанных -(1→2)- или -(1→3)-гликозидными связями. Концевое звено (невосстанавливающий остаток маннозы) боковой цепи чаще всего присоединено -(1→3)-гликозидной связью. Боковые цепи соединены с основной цепью -(1→2)-гликозидными связями. Некоторые олигосахариды боковых цепей присоединены фосфодиэфирными связями.
Углеводные цепи маннопротеина присоединены N-гликозидной связью через остаток N,N-диацетилхитобиозы к амидным группам остатков аспарагина белковой части углевод-белкового комплекса.
Маннопротеины содержатся, в основном, в грибах. Наиболее изучены маннопротеины дрожжей, в частности, компонент клеточных стенок пекарских дрожжей Saccharomyces cerevisiae. В жестких условиях щелочной экстракции, применяемой для выделения данных маннопротеинов, белковая часть молекул разрушается и выделяется разветвленный полисахаридный фрагмент маннопротеина.
Рассмотрим строение манно-белкового комплекса на примере маннопротеина аскомицетовых дрожжей Saccharomyces cerevisiae. Около 40% массы клеточной стенки аскомицетовых дрожжей приходится на маннопротеины, небольшое количество N-ацетилглюкозамина и остатков фосфорной кислоты. Маннопротеины Saccharomyces cerevisiae разделяются на группы по характеру связи присоединения звеньев остатков маннана к молекулам белка: между полисахаридной и белковой частью. Известны три типа таких связей: O-гликозилирование, N-гликозилирование и присоединение с помощью гликозил-фосфоинозитольного «якоря».
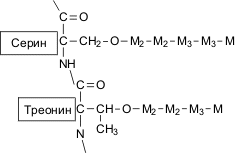
О-гликозилирование: короткие неразветвленные маннозные цепи присоединены к молекуле белка посредством О-гликозидной связи между остатком маннозы и гидроксильной группой серина или треонина (рис.5). О-связанные полисахаридные цепочки содержат от одного до пяти звеньев остатков маннопиранозы. Количество звеньев маннозы, присоединенной к макромолекулам белков таким способом, может составлять до 12% от общего числа маннозных остатков в маннопротеинах клеточной стенки. Звенья остатков маннозы связаны между собой -(1→3)- и -(1→2)-гликозидными связями.
|
|
|
Рис.5. Структура О-связанных олигосахаридных цепей манопротеинов; Мi – звенья остатков маннозы. Индекс обозначает тип гликозидной связи: М2 – -(1→2)-, М3 – -(1→3)-гликозидная связь. |
N-гликозилирование: разветвленные маннозные цепи присоединяются к макромолекуле белка через хитобиозный мостик при помощи N-гликозидной связи между остатком N-ацетилглюкозамина и β-амидным азотом аспарагина (рис.6). Высокоразветвленные длинные маннозные цепи таких маннопротеинов неоднородны по строению и состоят из внутренней части – так называемого кора, в который входит 12–15 маннозных единиц и вариабельной по своим размерам внешней цепи. Последняя образована из звеньев остатков маннозы, соединенных -(1→6)-гликозидными связями в центральной цепи, к которой -(1→2)-гликозидными связями присоединены короткие олигосахаридные цепи, построенные из звеньев остатков маннозы, связанных -(1→2)- и -(1→3)-гликозидными связями (рис.6).
|
|
|
Рис.6. Структура N-связанных полисахаридных цепей манопротеинов. Индекс обозначает тип гликозидной связи. Пояснение в тексте. |
Связь с помощью гликозил-фосфоинозитольного «якоря». Некоторые белки клеточной стенки содержат на С-конце так называемый GPI-якорь (гликозилфосфоинозитольный якорь). В отличие от N- и О-связанных цепей GPI-якорь присоединен к макромолекуле белка через фосфоэтаноламин концевым нередуцирующим звеном полисахаридной цепочки. С помощью такого «якоря» белки «закрепляются» в цитоплазматической мембране клетки.
|
|
|
Рис.7. Структура GPI-«якоря» маннопротеинов клеточной стенки. |
Маннопротеины различных дрожжей отличаются степенью разветвленности, типами связей основной и боковых цепей, наличием остатков -D-маннопиранозы, содержанием остатков фосфорной кислоты и др. Считается, что структура маннопротеина определяет свойства поверхности клеток дрожжей, в частности их антигенную специфичность.