
- •Хитин Распространение в природе
- •Получение
- •Химическое строение и молекулярная структура
- •Физические свойства
- •Химические свойства
- •Хитозан Химическое строение и молекулярная структура
- •Физические свойства
- •Химические свойства
- •Физико-химические свойства хитозана
- •Применение хитина и хитозана
- •Литература
Химическое строение и молекулярная структура
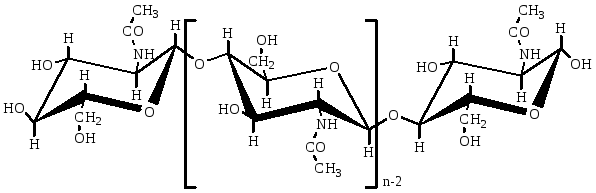
Хитин представляет собой линейный гомополисахарид, неразветвленные цепи которого состоят из элементарных звеньев остатков 2-ацетамидо-2-дезокси-β-D-глюкопиранозы (N-ацетил-β-D-глюкозы), соединенныхβ-(1→4)-гликозидной связью(рис.2).

Рис.2.Структурная формула макромолекулы хитина.
Имеется, таким образом, аналогия между строением хитина и целлюлозы (см. раздел «Целлюлоза»), однако в отличие от целлюлозы в качестве заместителя у второго углеродного атома элементарного звена имеется не гидроксильная, а ацетамидная группа. При этом макромолекулы нативного (природного) хитина обычно содержат небольшое количество звеньев со свободными первичными аминогруппами.
Энергетически выгодной конформацией элементарного звена макромолекулы хитина является конформация кресла С1:
Хитин, выделенный из биомассы животного происхождения, в силу специфики получения не является однородным по химическому составу и строению. Поскольку хитин не встречается в природе в свободном состоянии, а находится в виде комплекса с различными соединениями (белками, минеральными составляющими и др.), то выделенный из сырья хитин содержит примесные количества этих веществ. Наиболее трудно удаляемым компонентом являются фрагменты белка, ковалентно связанного с хитином. Поэтому полученный в промышленных условиях хитин является, по существу, гликопротеином.
Физические свойства
Большая длина и ограниченная гибкость макромолекулы хитина являются предпосылками для образования сложных надмолекулярных структур в тканях живых организмов. Основным элементом такой структуры являются фибриллы – высокоориентированные агрегаты макромолекул диаметром 25-50 нм, в свою очередь состоящие из микрофибрилл диаметром 2.5-2.8 нм. Такая структура обеспечивает выполнение важной биологической функции армирования (повышения механической прочности) содержащих хитин тканей.
Благодаря регулярности строения полимерной цепи хитина формируется высокоупорядоченная структура, обладающая признаками, характерными для кристаллического фазового состоянияполимеров. При этом кристаллические области структуры хитина могут существовать в трехкристаллографических(структурных)модификациях, отличающихся расположением молекулярных цепей в элементарной ячейке кристаллита (полиморфные модификации).
Наиболее распространенная модификация (присущая в основном хитину членистоногих, а также некоторых грибов) – α-хитин. Плотная упаковка макромолекул, характерная для элементарной ячейки α-хитина (рис.3), обеспечивается так называемым антипараллельным их расположением (противоположное направление атомов в расположенных рядом цепях).
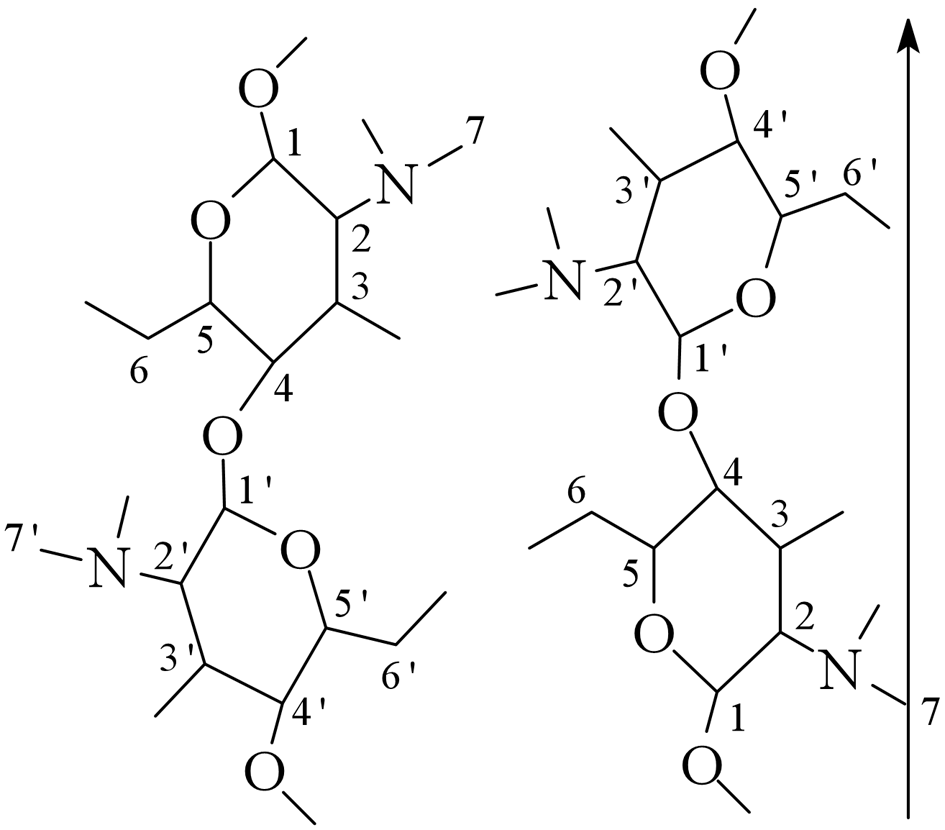
Рис.3.Взаимное расположение макромолекул в структурной модификации α-хитина
β-Хитинсуществует в виде относительно неустойчивых кристаллогидратов с параллельным расположением цепей в элементарной ячейке. Наконец, в ячейкеγ-хитинаимеются две цепи, расположенные параллельно, и одна – антипараллельно по отношению к ним. При этом все три модификации могут существовать в одном организме, что указывает на различие в выполняемых ими биологических функциях.
Специфика полимерного состояния хитина, как и других высокомолекулярных соединений, обусловливает невозможность существования этого полимера как однофазной системы (полная кристалличность). Однако содержание кристаллических областей в хитине достаточно велико и составляет в зависимости от происхождения и способа выделения 60-85%. При этом фиксация взаимного расположения макромолекул хитина обеспечивается системой внутри-имежмолекулярных водородных связей: ОН-группа у С3элементарного звена включена в водородную связь с атомом кислорода в цикле соседнего элементарного звена; ОН-группа у С6может быть связана водородными связями каквнутримолекулярно– с атомом кислорода гликозидной связи и (или) атомом азота ацетамидной группы, таки межмолекулярно- с ОН-группой у С6соседней макромолекулы (см. рис.3). При этом последняя может образовывать водородные связи с молекулами кристаллизационной воды.
Благодаря сравнительно высокой жесткости
полимерной цепи и значительной
интенсивности межмолекулярного
взаимодействия хитин растворяется в
сравнительно ограниченном количестве
растворителей – концентрированных
минеральных кислотах (соляной, серной,
азотной, фосфорной), безводной муравьиной
кислоте, гексафторизопропаноле и
гексафторацетоне, растворах диметилацетамида
и диметилсульфоксида в присутствии Li+(5-10%). В большинстве этих растворителей
происходит деструкция полимера, что
затрудняет определение истинного
значения молекулярной массы и характера
молекулярно-массового распределения.
Имеющиеся данные свидетельствуют о
том, что выделенный, в частности, из
панцирей ракообразных хитин представляет
собой высокомолекулярный полимер с
молекулярной массой![]() 2 - 2.5∙106Да (степень полимеризации 10 - 14∙103).
2 - 2.5∙106Да (степень полимеризации 10 - 14∙103).
