-
У
скільки раз зміниться швидкість
прямої і зворотної реакції в системі
2SO2+O2
2SO3(г),
якщо об’єм газової суміші зменшити
в 3 рази? В яку сторону зміститься
рівновага системи?
-
Хімічна
рівновага реакції CO2
+ H2
CO + H2O
установилась при таких концентраціях
реагуючих речовин (моль/л): С(СО2)
= 7; С(Н2)
= 5; С(СО) = 10; С(Н2О)
= 14. Рівновага системи була порушена
через зменшення концентрації Н2О
до 11 моль/л. Обчисліть, якими стали
нові рівноважні концентрації реагуючих
речовин після зміщення рівноваги?
-
Реакція
проходить за рівнянням А2+В2=
2АВ. Початкова концентрація речовини
А дорівнює 0,8 моль/л, а речовини В - 1
моль/л. Через деякий час концентрація
речовини А зменшилась до 0,5 моль/л.
Якою в цей час була концентрація
речовини В?
-
Реакція
протікає за рівнянням 2А
В. Вихідна концентрація речовини А
дорівнює 0,2 моль/л. Константа рівноваги
реакції КС=0,5.
Обчисліть рівноважні концентрації
реагуючих речовин.
|
-
Визначити
як зміниться швидкість реакції
утворення аміаку з азоту та водню,
якщо збільшити концентрації вихідних
речовин удвічі?
-
Хімічна
рівновага реакції СOCl2
CO + Cl2
установилась при концентраціях
реагуючих речовин (моль/л): С(COCl2)
= 10; C(CO) = 2; C(Cl2)
= 4. У рівноважну систему додали хлор
в кількості 4 моль/л. Визначте нові
рівноважні концентрації реагуючих
речовин після зміщення рівноваги.
-
Реакція
проходить за рівнянням А + В
С + D.Рівноважна
концентрація речовини В = 0,5 моль/л, С
= 0,2 моль/л. Константа рівноваги реакції
0,04. Визначте вихідні концентрації А
і В.
-
Константа
рівноваги реакції N2
+ 3H2
2NH3
KC=0,1
при 673 К.Рівноважні концентрації
(моль/л): С(Н2)=0,6
і С(NH3)=0,18.
Обчисліть вихідну і рівноважну
концентрацію азоту.
|
-
Реакція
відбувається за рівнянням 2NO
+ O2
2NO2.
Вихідні концентрації реагуючих
речовин були (моль/л): С(NO)=0,8,
C(O2)=0,6.
Як зміниться швидкість реакції, якщо
концентрацію кисню збільшити до 0,9
моль/л, а концентрацію нітроген(ІІ)
оксиду до 1,2 моль/л?
-
Хімічна
рівновага реакції CO2
+ H2
CO
+ H2O
установилась при таких концентраціях
реагуючих речовин (моль/л): С(СО2)
= 5; С(Н2)
= 8; С(СО) = 12; С(Н2О)
= 10. Рівновага системи була порушена
через зменшення концентрації Н2
до 5 моль/л. Обчисліть, якими стали
нові рівноважні концентрації реагуючих
речовин після зміщення рівноваги?
-
Константа
рівноваги гомогенної системи
СО(г)+Н2О(г)
СО2(г)+Н2(г)
при 850С
дорівнює 1. Обчисліть концентрації
всіх речовин при рівновазі, якщо
вихідні концентрації СО і Н2О
відповідно становлять 3 моль/л і 2
моль/л.
-
Константа
рівноваги гомогенної системи
СО(г)+Н2О(г)
СО2(г)+Н2(г)
при 850С
дорівнює 1. Обчисліть концентрації
всіх речовин при рівновазі, якщо
вихідні концентрації СО і Н2О
відповідно становлять 3 моль/л і 2
моль/л.
|
-
У
стані рівноваги системи N2
+ 3H2
2NH3
концентрації реагуючих речовин були:
С(N2)
= 0,3; C(H2)
= 0,9; C(NH3)
= 0,4. Обчисліть,
як зміниться швидкість прямої і
зворотної реакції, якщо тиск збільшити
в 5 разів? У якому напрямку зміститься
рівновага?
-
Хімічна
рівновага реакції CO2
+ H2
CO + H2O
установилась при таких концентраціях
реагуючих речовин (моль/л): С(СО2)
= 8; С(Н2)
= 6; С(СО) = 12; С(Н2О)
= 8. Рівновага системи була порушена
через зменшення концентрації СО до
8 моль/л. Обчисліть, якими стали нові
рівноважні концентрації реагуючих
речовин після зміщення рівноваги?
-
Реакція
проходить за рівнянням А + В
С + D.
Рівноважна концентрація речовини В
= 0,5 моль/л, С = 0,2 моль/л. Константа
рівноваги реакції 0,04. Визначте вихідні
концентрації А і В.
-
Константа
рівноваги реакції N2
+ 3H2
2NH3
KC=0,1
при 673 К. Рівноважні концентрації
(моль/л): С(Н2)=0,6
і С(NH3)=0,18.
Обчисліть вихідну і рівноважну
концентрацію азоту.
|
-
Як
зміниться швидкість реакції 2Fe + 3Cl2
2FeCl3,
якщо тиск у системі збільшити в 5
разів?
-
Хімічна
рівновага реакції СOCl2
CO + Cl2
установилась при концентраціях
реагуючих речовин (моль/л): С(COCl2)
= 8; C(CO) = 4; C(Cl2)
= 6. У рівноважну систему додали СOCl2
в кількості 4 моль/л. Визначте нові
рівноважні концентрації реагуючих
речовин після зміщення рівноваги.
-
Знайдіть
концентрації вихідних речовин у
реакції H2
+ I2
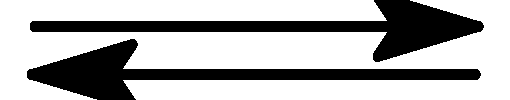 2НI, якщо рівноважні концентрації HI –
0,25 моль/л, I2
– 0,05 моль/л, Н2
– 0,15 моль/л.
2НI, якщо рівноважні концентрації HI –
0,25 моль/л, I2
– 0,05 моль/л, Н2
– 0,15 моль/л.
-
Суміш
оксиду вуглецю (ІІ) і водяної пари, що
містить 50% СО і 50% Н2О
(проценти за обємом),
пропустили при 1400 К над залізним
каталізатором. Константа рівноваги
реакції СО + Н2О
= СО2
+ Н2
дорівнює 0,5. Обчислити вихід продуктів
і процентний (за обємом)
склад рівноважної газової суміші.
|
-
У
скільки разів зросте швидкість
взаємодії водню з бромом у газовій
фазі, якщо концентрації вихідних
речовин збільшити у 3 рази?
-
Хімічна
рівновага реакції СOCl2
CO + Cl2
установилась при концентраціях
реагуючих речовин (моль/л): С(COCl2)
= 12; C(CO) = 8; C(Cl2)
= 10. У рівноважну систему додали СО в
кількості 4 моль/л. Визначте нові
рівноважні концентрації реагуючих
речовин після зміщення рівноваги.
-
Знайдіть
концентрації вихідних речовин у
реакції С + Н2О
 СО + Н2,
якщо рівноважні концентрації СО – 4
моль/л, С – 2 моль/л, Н2О
– 1 моль/л.
СО + Н2,
якщо рівноважні концентрації СО – 4
моль/л, С – 2 моль/л, Н2О
– 1 моль/л.
-
Реакція
проходить за рівнянням А + В
 С
+ D.
Рівноважна концентрація речовини В
= 0,5 моль/л, С = 0,2 моль/л. Константа
рівноваги реакції 0,04. Визначте вихідні
концентрації А і В. С
+ D.
Рівноважна концентрація речовини В
= 0,5 моль/л, С = 0,2 моль/л. Константа
рівноваги реакції 0,04. Визначте вихідні
концентрації А і В.
|
-
Реакція
відбувається за рівнянням 2NO
+ O2
2NO2.
Вихідні концентрації реагуючих
речовин були (моль/л): С(NO)=0,8,
C(O2)=0,6.
Як зміниться швидкість реакції, якщо
концентрацію кисню збільшити до 0,9
моль/л, а концентрацію нітроген(ІІ)
оксиду до 1,2 моль/л?
-
Хімічна
рівновага реакції CO2
+ H2
CO
+ H2O
установилась
при таких концентраціях реагуючих
речовин (моль/л): С(СО2)
= 9; С(Н2)
= 4; С(СО) = 8; С(Н2О)
= 6. Рівновага системи була порушена
через зменшення концентрації СО2
до 7 моль/л. Обчисліть, якими стали
нові рівноважні концентрації реагуючих
речовин після зміщення рівноваги?
-
Реакція
проходить за рівнянням А2+В2
2АВ. Початкова концентрація речовини
А дорівнює 0,8 моль/л, а речовини В - 1
моль/л. Через деякий час концентрація
речовини А зменшилась до 0,5 моль/л.
Якою в цей час була концентрація
речовини В?
-
Константа
рівноваги гомогенної системи
СО(г)+Н2О(г)
О2(г)+Н2(г)
при 850С
дорівнює 1. Обчисліть концентрації
всіх речовин при рівновазі, якщо
вихідні концентрації СО і Н2О
відповідно становлять 3 моль/л і 2
моль/л.
|
-
У
скільки разів слід збільшити
концентрацію водню в реакції утворення
аміаку (амоніаку NH3)
з простих речовин, щоб її швидкість
зросла в 125 разів?
-
Хімічна
рівновага реакції CO2
+
H2
CO
+ H2O
установилась
при таких концентраціях реагуючих
речовин (моль/л): С(СО2)
= 12; С(Н2)
= 8; С(СО) = 12; С(Н2О)
= 10. Рівновага системи була порушена
через зменшення концентрації Н2
до 6 моль/л. Обчисліть, якими стали
нові рівноважні концентрації реагуючих
речовин після зміщення рівноваги?
-
При синтезі
фосгену СО + Cl2
 COCl2
рівновага встановлюється при таких
концентраціях реагуючих речовин
(моль/л): С(Cl2)
= 2,5; C(CO) = 1,8; C(COCl2)
= 3,2. Визначте вихідні концентрації
карбон(ІІ) оксиду та хлору.
COCl2
рівновага встановлюється при таких
концентраціях реагуючих речовин
(моль/л): С(Cl2)
= 2,5; C(CO) = 1,8; C(COCl2)
= 3,2. Визначте вихідні концентрації
карбон(ІІ) оксиду та хлору.
-
Константа
рівноваги реакції N2
+ 3H2
NH3
KC=0,1
при 673 К.Рівноважні концентрації
(моль/л): С(Н2)=0,6
і С(NH3)=0,18.
Обчисліть вихідну і рівноважну
концентрацію азоту.
|
-
Як
зміниться швидкість реакції, що
проходить за рівнянням N2
+ O2
 2NO, якщо тиск збільшити в 4 рази?
2NO, якщо тиск збільшити в 4 рази?
-
Хімічна
рівновага реакції СOCl2
CO
+ Cl2
установилась
при концентраціях реагуючих речовин
(моль/л): С(COCl2)
= 13; C(CO)
= 6; C(Cl2)
= 2. У
рівноважну систему додали хлор в
кількості 4 моль/л. Визначте нові
рівноважні концентрації реагуючих
речовин після зміщення рівноваги.
-
Вихідні
концентрації карбон(ІІ) оксиду та
парів води відповідно рівні 0,08 моль/л.
Обчисліть рівноважні концентрації
СО, Н2О,
Н2
у системі СО + Н2О
 СО2
+ Н2,
якщо рівноважна концентрація СО
становить 0,05 моль/л.
СО2
+ Н2,
якщо рівноважна концентрація СО
становить 0,05 моль/л.
-
Рівновага
в системі 2NO2
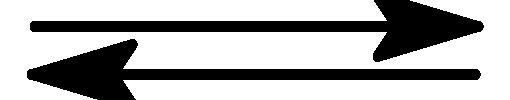 2NO + O2
при деякій температурі встановилася
при концентраціях NO2
– 2,06 моль/л, NO – 2,24 моль/л, O2
– 2,12 моль/л. Визначити константу
рівноваги і обчисліть вихідну
концентрацію NO2.
2NO + O2
при деякій температурі встановилася
при концентраціях NO2
– 2,06 моль/л, NO – 2,24 моль/л, O2
– 2,12 моль/л. Визначити константу
рівноваги і обчисліть вихідну
концентрацію NO2.
|
-
Визначити
як зміниться швидкість реакції
утворення аміаку з азоту та водню,
якщо збільшити концентрації вихідних
речовин удвічі?
-
Хімічна
рівновага реакції СOCl2
CO
+ Cl2
установилась
при концентраціях реагуючих речовин
(моль/л): С(COCl2)
= 6; C(CO)
= 12; C(Cl2)
= 10. З
рівноважної системи вивели хлор в
кількості 4 моль/л. Визначте нові
рівноважні концентрації реагуючих
речовин після зміщення рівноваги.
-
Вихідні
концентрації кожної з речовин у суміші
складають 1 моль/л: А + В
 С + D. Після встановлення рівноваги
концентрація речовини D становила
1,5 моль/л. Визначити константу рівноваги.
С + D. Після встановлення рівноваги
концентрація речовини D становила
1,5 моль/л. Визначити константу рівноваги.
-
Реакція
проходить за рівнянням А + В
С + D.
Рівноважна концентрація речовини В
= 0,5 моль/л, С = 0,2 моль/л. Константа
рівноваги реакції 0,04. Визначте вихідні
концентрації А і В.
|

