
- •ХИМИЧЕСКАЯ И ПОСТТРАНСЛЯЦИОННАЯ
- •Модификаций много, а память и время ограничены. Продолжаем обсуждать
- •ОБРАТИМОЕ АЦЕТИЛИРОВАНИЕ. Используют, например, при ограничении фрагментации белков с помощью сериновых протеаз
- •Сериновые протеазы. Механизм ковалентного катализа.
- •РЕАКЦИИ НУКЛЕОФИЛЬНОГО ПРИСОЕДИНЕНИЯ-ОТЩЕПЛЕНИЯ
- •В зависимости от рН при взаимодействии соединений, содержащих карбонильную группу, реакция может остановиться
- •АСПАРТАТ АМИНОТРАНСФЕРАЗА – катализирует реакцию переаминирования между аспартатом и альфа-кетоглутаратом
- •АСПАРТАТ АМИНОТРАНСФЕРАЗЫ – катализирует реакцию переаминирования между оксалоацетатом
- •Неферментативное гликозилирование (гликирование) белков
- •НЕФЕРМЕНТАТИВНОЕ ГЛИКОЗИЛИРОВАНИЕ БЕЛКОВ
- •Коллаген – основной белковый элемент межклеточного матрикса (семейство близкородственных фибриллярных белков). Функции межклеточного
- •Коллаген – основной белок соединительной ткани
- •МУЛЬТИМОДИФИКАЦИЯ
- •ГИСТОНОВЫЙ КОД
- •РЕАКЦИИ НУКЛЕОФИЛЬНОГО ЗАМЕЩЕНИЯ (по конечному результату)
- •АЛКИЛИРОВАНИЕ ФУНКЦИОНАЛЬНЫХ ГРУПП БЕЛКОВ
- ••Было показано, что в гистоне Н3 триметилированный Lys4 необходим для активации процесса транскрипции,
- •АЛКИЛИРУЮЩИЕ РЕАГЕНТЫ
- •АЛКИЛИРОВАНИЕ БЕЛКОВ (реакция по боковому радикалу остатка лизина)
- •Вспомним схему синтеза S-аденозилметионина. С вашей точки зрения по какому механизму протекает реакция
- •Вспомним, что может произойти, если будет повышаться уровень гомоцистеина. Это наблюдается при развитии,
- •N-Homocysteinylation of proteins
- •ДЕМЕТИЛИРОВАНИЕ ОСТАТКА МОДИФИЦИРОВАННОГО ЛИЗИНА
- •ДЕМЕТИЛИРОВАНИЕ ДИ- И МОНОМЕТИЛИРОВАННЫХ ОСТАТКОВ ЛИЗИНА В ГИСТОНАХ, КАТАЛИЗИРУЕМОЕ
- •ДЕМЕТИЛИРОВАНИЕ ТРИ-, ДИ- И МОНОМЕТИЛИРОВАННЫХ ОСТАТКОВ ЛИЗИНА В ГИСТОНАХ, КАТАЛИЗИРУЕМОЕ ГИСТОНДЕМИТИЛАЗОЙ, ФУНКЦИОНИРУЮЩЕЙ В
- ••Таким образом, метилирование-диметилирование наряду с ацетилированием-деацетилированием определенных аминокислотных остатков в гистонах является одним
- •N-метилирование по остаткам Lys и Arg в гистонах; введение фрагментов, содержащих изопренильные группы
- ••Изопренилированию подвергаются белки семейств Ras, Rab, Rho (продукты протоонкогенов ras, rab, rho, участвующие
- •Белок, обладая большим сродством к липидным мембранам, служит уникальным местом опознавания для определенных
- •Наблюдается дальнейший процессинг: протеолитическое удаление Суs-А-А-Х-протеазой трипептида А-А-Х с С-конца и карбоксиметилирование остатка
- •Молекулярные механизмы формирования и движения пузырьков
- •Rab-белки участвуют в транспорте пузырьков в клетке
- ••Для каждой внутриклеточной мембраны существуют специфические Rab-белки, которые обеспечивают определенное направление пузырьков. От
- •• CAAX мотив запускает три последовательных ферментативных
- •ВЗАИМОДЕЙСТВИЕ С АЛКИЛИРУЮЩИМИ РЕАГЕНТАМИ
- •ХИМИОТЕРАПИЯ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ
- •ADP-РИБОЗИЛИРОВАНИЕ
- •ГЛИКОЗИЛИРОВАНИЕ БЕЛКОВ
- •N-гликозилирование белков происходит по карбоксамидному атому азота остатка аспарагина в последовательности Asn-X-Ser/Thr. Образование
- •карбоний-ион изображается как резонансный гибрид двух состояний, в одном из которых (оксоний-ион)
- •РЕАКЦИИ ЭЛЕКТРОФИЛЬНОГО ЗАМЕЩЕНИЯ
- ••Тироглобулин – гликопротеин с молекулярной массой 660 кДа, содержит 115 остатков тирозина, синтезируется
- ••В крови йодтиронины находятся в связанной форме в комплексе с тироксинсвязывающим белком. Только
- •Тиреоглобулин с Т4
- •Химические модификации
- •Химические модификации
НЕФЕРМЕНТАТИВНОЕ ГЛИКОЗИЛИРОВАНИЕ БЕЛКОВ
•Гликирование белков представляет собой эндогенное неферментативное присоединение остатков восстанавливающих сахаров, присутствующих в крови, к боковым радикалам лизина или аргинина в составе белка. Процесс гликирования можно условно разделить на раннюю и позднюю стадии. На первой стадии гликирования происходит нуклеофильная атака карбонильной группы глюкозы -аминогруппой лизина, в результате которой
образуется лабильное основание Шиффа – N гликозилимин
(1). Образование основания Шиффа – процесс относительно быстрый и обратимый. Далее происходит перегруппировка N гликозилимина с образованием продукта Амадори – 1 амино 1 дезоксифруктозы (2). Скорость этого процесса ниже, чем скорость образования гликозилимина, но существенно выше, чем скорость гидролиза основания Шиффа, поэтому белки, содержащие остатки 1 амино 1 дезоксифруктозы, накапливаются в крови.
•При сахарном диабете наблюдается повышенный уровень гликированного альбумина и гемоглобина (диагностика - ЦНМТ, Санитис и другие центры).
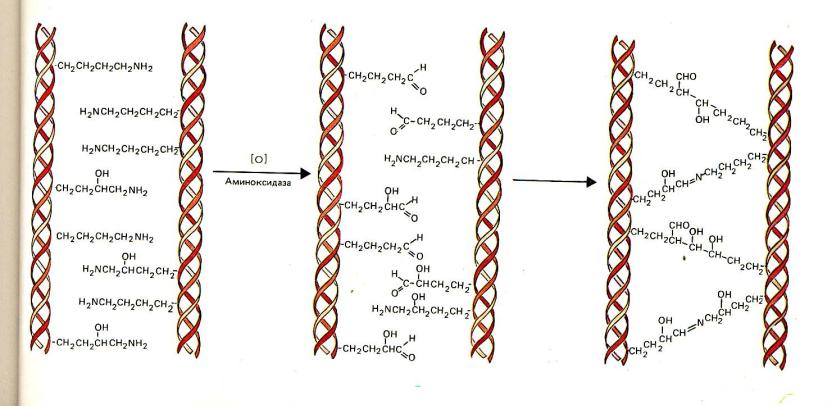
Коллаген – основной белковый элемент межклеточного матрикса (семейство близкородственных фибриллярных белков). Функции межклеточного матрикса: образует каркас органов и тканей; является универсальным «биологическим» клеем; участвует в регуляции водно- солевого обмена; образует высокоспециализированные структуры (кости, зубы, хрящи, сухожилия, базальные мембраны).
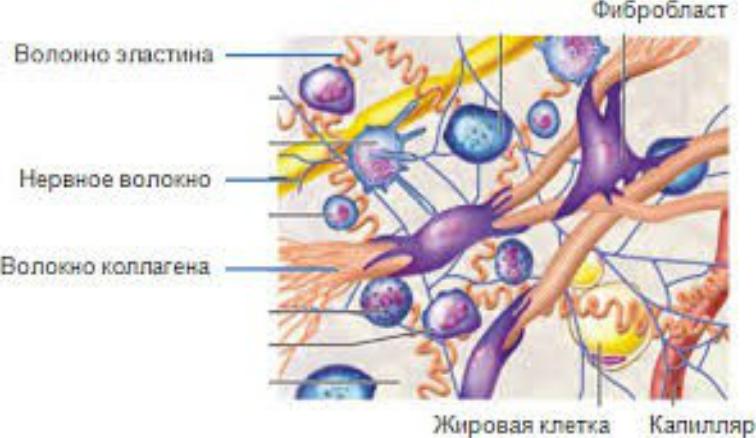
Коллаген – основной белок соединительной ткани


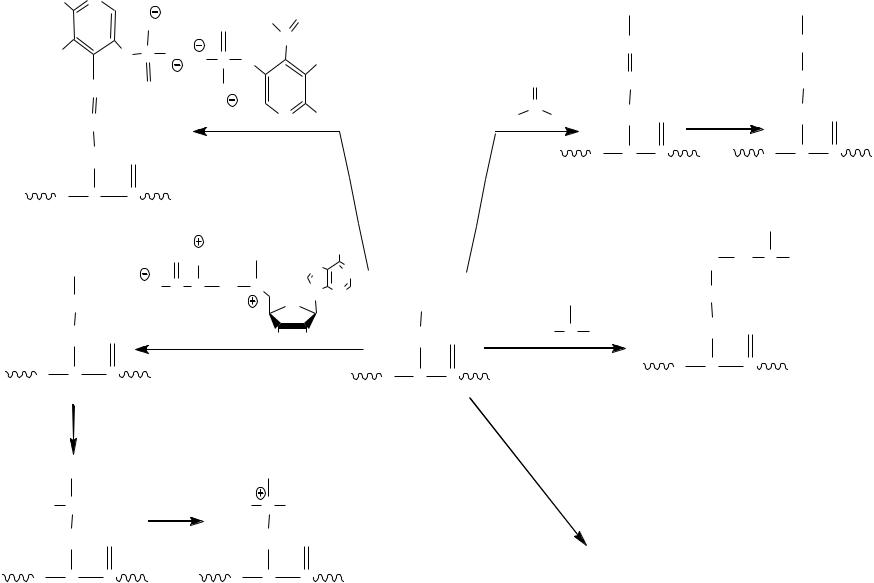
МУЛЬТИМОДИФИКАЦИЯ

H3C |
N |
|
|
|
H |
O |
|
|
|
O |
O |
||
|
|
|
|
|
C |
|
HO |
|
C |
P O |
O P |
H2 |
OH |
|
C |
|||||
|
HC |
H2 |
|
|
|
|
|
|
O |
O |
|
|
|
|
N |
|
|
|
N |
CH3 |
|
(CH2)4 O |
|
|
|
|
|
N |
C |
C |
|
|
|
|
H |
H |
|
|
|
|
|
|
CH3 |
O |
NH |
CH3 |
|
NH2 |
|
|
3 H2 |
|
N |
N |
|
|
NH |
O C |
C C |
S |
N |
N |
|
|
H |
O |
|
|
|
|
(CH2)4 O |
|
OH |
OH |
|
|
N |
C |
C |
|
|
|
|
H |
H |
|
|
|
|
|
|
CH3 |
|
|
CH3 |
|
H3C |
N |
|
H3C N |
CH3 |
|
|
(CH2)4 O |
|
(CH2)4 O |
||
N |
C |
C |
N |
C |
C |
H |
H |
|
H |
H |
|
|
|
|
|
|
R |
|
|
|
|
R |
|
|
|
|
|
CH |
|
|
|
|
CH2 |
|
|
|
O |
|
N |
|
|
|
|
HN |
|
|
|
R C H |
|
(H2C)4 |
O |
NaBH4 |
|
(H2C)4 O |
|
|
|
|
pH 9 |
N |
C |
C |
|
|
N |
C C |
|
|
|
|
H |
H |
|
|
|
H |
H |
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
H2C |
H2 |
|
|
|
|
|
|
|
|
|
C |
N |
R |
|
|
NH2 |
|
|
CH3 |
|
|
NH |
|
|
|
|
|
|
|
|
|
|
|
|
||
(H C) |
O |
ClH2CH2C |
N R |
|
|
(CH2)4 O |
|
|||
2 |
4 |
|
|
|
|
|
|
|
|
|
N |
C |
C |
|
|
|
N |
C |
C |
|
|
|
|
|
H |
H |
|
|
|
|||
H |
H |
|
|
|
|
|
|
|
|
|
неферментативное гликозилирование
ГИСТОНОВЫЙ КОД
•В целом под «гистоновым кодом» подразумевается весь набор модификаций аминокислотных остатков в N- и С-концевых последовательностях гистонов (фосфорилирование, ацетилирование, метилирование, ADP-рибозилирование), определяющий функциональное состояние гена в отношении процессов репликации и транскрипции.
•Фосфорилирование и ацетилирование мы уже рассмотрели. Далее речь пойдет о реакциях алкилирования (например, метилирование остатков лизина и аргинина). И, как вы уже знаете, реакции алкилирования мы относим к реакциям нуклеофильного замещения.
РЕАКЦИИ НУКЛЕОФИЛЬНОГО ЗАМЕЩЕНИЯ (по конечному результату)
•ВИД ПЕРЕНОСИМЫХ ЧАСТИЦ: Алкильные остатки
•SN1 и SN2 (механизмы)
•SN1-реакция – мономолекулярное нуклеофильное замещение. Реакция, протекающая через алкильный карбокатион. Несогласованный двухстадийный процесс.
•SN2-реакция – Бимолекулярное нуклеофильное замещение. Согласованный процесс, т.е. одностадийная реакция, в которой исходное соединение и продукт разделяет только переходное состояние.
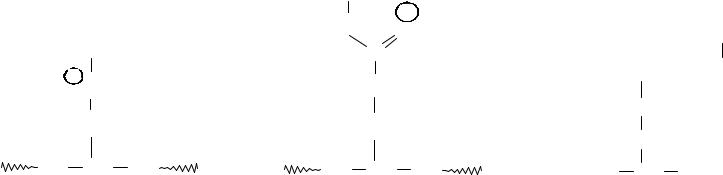
АЛКИЛИРОВАНИЕ ФУНКЦИОНАЛЬНЫХ ГРУПП БЕЛКОВ
•Распространенной группой посттрансляционной модификации является алкилирование. К этому типу модификации относится метилирование по остаткам лизина и аргинина и изопренилирование.
• |
CH3 |
+ |
|
|
NH |
||
|
NH2 |
||
CH3 |
C |
||
|
|||
+ NH2 |
NH |
|
|
(CH2)4 |
(CH ) |
||
|
|
2 3 |
|
NH CH CO |
NH CH CO |
||
CH3 (CH2-CH=C-CH2)nH
S
CH2






 NH CH CO
NH CH CO






